名校
解题方法
1 . 二氯亚砜(SOCl2)是一种无色易挥发液体,与水剧烈水解生成两种气体,常用作脱水剂,其熔点—105℃,沸点79℃,140℃以上时易分解。
(1)用硫黄(用S表示)、液氯和三氧化硫为原料在一定条件合成氯化亚砜,原子利用率达100%,则三者的物质的量比为_______________ 。写出SOCl2吸收水蒸气的化学方程式:_______________________________ 。
(2)甲同学设计下图装置用ZnCl2·xH2O晶体制取无水ZnCl2,回收剩余的SOCl2并验证生成物中含有SO2(夹持及加热装置略)。
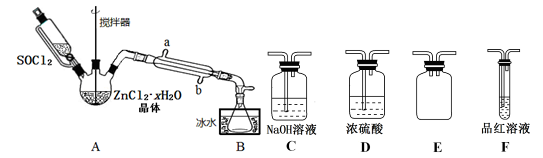
①装置的连接顺序为A→B→____ →___ →___ →____ 。
②冷凝管的进水口是_______________ 。(填“a”或“b”)
③实验结束,为检测ZnCl2·xH2O晶体是否完全脱水,称取蒸干后的固体ag溶于水,加入足量稀硝酸和硝酸银溶液,过滤洗涤干燥,称得固体为bg。若 =
=___ (保留一位小数),即可证明ZnCl2·xH2O晶体已完全脱水。
④乙同学认为直接将ZnCl2·xH2O晶体置于坩埚中加热灼烧即可得到无水ZnCl2,但大家说此方法不行,请解释原因______________________ 。
(3)丙同学认为SOCl2还可用作由FeCl3·6H2O制取无水FeCl3的脱水剂,但丁同学认为该实验会发生氧化还原反应。戊同学设计了如下实验方案判断丁同学的观点:取少量FeCl3 •6H2O于试管中,加入SOCl2,振荡使两种物质充分反应;再往试管中加水溶解,滴加KSCN溶液,若没有明显现象,则证明脱水过程中发生了氧化还原反应。按照戊同学的思路方法,还可以选择证明__________ 或______________ (填离子符号)是否存在证明该过程是否发生了氧化还原反应。
(1)用硫黄(用S表示)、液氯和三氧化硫为原料在一定条件合成氯化亚砜,原子利用率达100%,则三者的物质的量比为
(2)甲同学设计下图装置用ZnCl2·xH2O晶体制取无水ZnCl2,回收剩余的SOCl2并验证生成物中含有SO2(夹持及加热装置略)。

①装置的连接顺序为A→B→
②冷凝管的进水口是
③实验结束,为检测ZnCl2·xH2O晶体是否完全脱水,称取蒸干后的固体ag溶于水,加入足量稀硝酸和硝酸银溶液,过滤洗涤干燥,称得固体为bg。若
 =
=④乙同学认为直接将ZnCl2·xH2O晶体置于坩埚中加热灼烧即可得到无水ZnCl2,但大家说此方法不行,请解释原因
(3)丙同学认为SOCl2还可用作由FeCl3·6H2O制取无水FeCl3的脱水剂,但丁同学认为该实验会发生氧化还原反应。戊同学设计了如下实验方案判断丁同学的观点:取少量FeCl3 •6H2O于试管中,加入SOCl2,振荡使两种物质充分反应;再往试管中加水溶解,滴加KSCN溶液,若没有明显现象,则证明脱水过程中发生了氧化还原反应。按照戊同学的思路方法,还可以选择证明
您最近一年使用:0次
解题方法
2 . 某小组探究SO2的漂白原理及铜和浓硫酸反应的最低浓度,装置如图所示,部分装置省略。实验发现,装置B中溶液变红色,不褪色;装置C中溶液为红色,装置D中溶液褪色。向烧瓶中加入200mL18.4mol/L浓硫酸,充分反应直至装置A中反应停止。
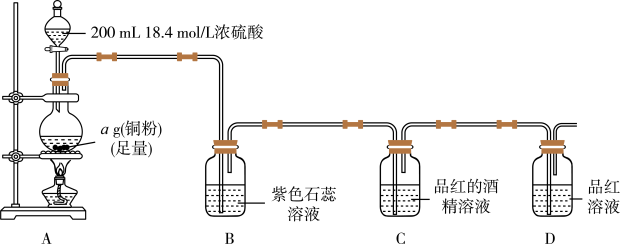
回答下列问题:
(1)装置A中发生反应的化学方程式为_______ 。
(2)根据装置C、D中出现的现象,对漂白品红的粒子提出如下猜想:
猜想1:H2SO3;猜想2:HSO ;猜想3:
;猜想3:_______ 。
针对猜想2设计简单实验探究漂白原理:_______ 。
(3)实验完毕后,甲同学设计如下实验测定剩余硫酸浓度(不考虑体积变化,假设锌与稀硫酸反应只产生氢气):

①实验部分操作:(a)调平量气管和烧杯的液面;(b)冷却至室温;(c)读数。
正确的先后操作顺序是_______ (填字母)。
②已知开始时量气管读数为V1mL,最终读数为V2mL(均折合成标准状况)。
则铜与浓硫酸发生反应的最低硫酸浓度为_______ mol/L。
(4)乙同学分析上述实验后,设计如下实验方案:
方案1:过滤、洗涤、低温干燥,称过量铜粉的质量(不考虑副产物)。
方案2:取25mL残留溶液,滴加甲基橙作指示剂,用标准NaOH溶液滴定H2SO4。
丙同学分析上述方案,认为方案_______ (填“1”或“2”)可行。请你帮丙同学分析不可行方案的理由:_______ 。
(5)丁同学采用滴定法测定硫酸最低浓度。取烧杯中剩余混合液20.00mL于锥形瓶中,滴加指示剂,用cmol/L标准EDTA(用Na4Y表示)溶液滴定至终点时消耗滴定液xmL。
已知:滴定反应为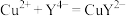 。
。
该浓硫酸的最低浓度为_______ mol/L。若滴定管没有用EDTA溶液润洗,测得结果_______ (填“偏高”“偏低”或“无影响”)。

回答下列问题:
(1)装置A中发生反应的化学方程式为
(2)根据装置C、D中出现的现象,对漂白品红的粒子提出如下猜想:
猜想1:H2SO3;猜想2:HSO
 ;猜想3:
;猜想3:针对猜想2设计简单实验探究漂白原理:
(3)实验完毕后,甲同学设计如下实验测定剩余硫酸浓度(不考虑体积变化,假设锌与稀硫酸反应只产生氢气):

①实验部分操作:(a)调平量气管和烧杯的液面;(b)冷却至室温;(c)读数。
正确的先后操作顺序是
②已知开始时量气管读数为V1mL,最终读数为V2mL(均折合成标准状况)。
则铜与浓硫酸发生反应的最低硫酸浓度为
(4)乙同学分析上述实验后,设计如下实验方案:
方案1:过滤、洗涤、低温干燥,称过量铜粉的质量(不考虑副产物)。
方案2:取25mL残留溶液,滴加甲基橙作指示剂,用标准NaOH溶液滴定H2SO4。
丙同学分析上述方案,认为方案
(5)丁同学采用滴定法测定硫酸最低浓度。取烧杯中剩余混合液20.00mL于锥形瓶中,滴加指示剂,用cmol/L标准EDTA(用Na4Y表示)溶液滴定至终点时消耗滴定液xmL。
已知:滴定反应为
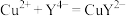 。
。该浓硫酸的最低浓度为
您最近一年使用:0次
2022-12-23更新
|
208次组卷
|
3卷引用: 河南省湘豫名校联考2022-2023学年高三上学期12月期末摸底考试化学试题
河南省湘豫名校联考2022-2023学年高三上学期12月期末摸底考试化学试题 (已下线)河南省湘豫名校联考2022-2023学年高三上学期12月期末摸底考试变式汇编(17-21)河南省郑州市等3地2022-2023学年高三上学期12月月考化学试题



