16. 读下而关于氨气的科普短文,并回答相关问题。
氨气(NH
3)是密度比空气小,极易溶于水、无色的刺激性气体,对黏膜有刺激作用。氨气易液化,常温下加压到1MPa,或者常压下温度降到-33℃,均可将其液化。
氨气(NH
3)在生产中的应用十分广泛:常用来制化肥和硝酸,科学家们发现它还是一种很有前景的燃料,它燃烧时生成氮气(N
2)和水(H
2O)。
氨气(NH
3)价格低、制造技术成熟,便于普及使用,传统的工业合成氨气是将氮气(N
2)和氢气(H
2)在20-50MPa的高压和500℃的高温条件下,用铁作催化剂合成氨。德国化学家格哈德·埃特尔在研究中取得了非凡的成就,揭示了氮气与氢气在催化剂表面合成氨气的反应过程。
如图为该过程的微观示意图(图中“

”表示氮原子,“

”表示氢原子,“
”表示催化剂)
(一)根据短文回答问题:
(1)氨气的物理性质有
______(写一点)。
(2)从微观角度看,氨气是由
______构成(填具体的微粒名称)。
(3)氨气燃烧的化学方程式为
______。
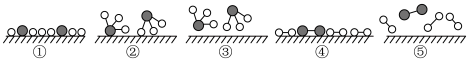
(4)从上文微观示意图可知,传统工业合成氨气的工艺中,氮气与氢气在催化剂表面合成氨气过程合理的顺序是______。
| A.⑤④①③② | B.④⑤①②③ | C.④⑤①③② | D.⑤④①②③ |
(5)氨的合成和运输过程中应注意______(填序号)。
| A.防止接触明火 |
| B.工作人员佩戴防护设备 |
| C.呼吸道疾病患者不宜从事该行业 |
(二)某化学兴趣小组为探究氨分子的运动情况,在课本实验图甲的基础上进行改进,如图乙进行实验:在T形管的粗玻璃管里,固定一根湿润的酚酞滤纸条,将浓氨水加入左侧试管中观察实验现象。再换一根湿润的酚酞滤纸条,微微加热试管,观察。

(6)一会儿,观察到
______(填“ab”或“bc”)段酚酞滤纸条先变成红色。
(7)微微加热试管中的浓氨水,酚酞滤纸条变红的速率会
______(填“变慢”或“加快”)。