13. 同学们往盛有NaOH溶液的试管中通入CO
2,未看到明显现象,于是对NaOH与CO
2是否发生反应进行了探究利拓展实验。
活动一:
(1)甲同学设计了如图1所示实验(装置气密性良好),观察到的实验现象为
_____。
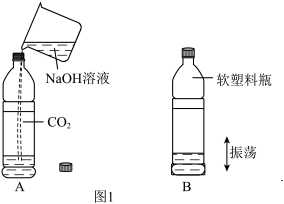
(2)甲同学认为上述实验操作及现象足以证明氢氧化钠与二氧化碳发生了反应,其他同学均认为不合理,理由是
_______。
活动二:
(3)取活动一结束后软塑料瓶中的液体于三支试管中,分别进行如图2所示实验。当观察到三支试管中有明显现象时,均证明氢氧化钠和二氧化碳发生了反应。A、B、C试管中的现象分别为
______,试管中反应的化学反应方程式为
______(任写其一)。

活动三:活动二结束后,同学们将三支试管中的剩余物倒入一个洁净的大烧杯中进行废液回收,搅拌静置后发现烧杯内上层为无色清液,下层有白色沉淀,如图3。

(4)上层清液中一定不会大量存在的离子是
_____。
(5)为检验上层清液中是否存在大量OH
-和CO

,同学们按下列表格进行试验,请完善表格。
| 实验步骤 | 实验现象 | 实验结论 |
| ①取烧杯中上层清液少许于试管中,滴加Ba(NO3)2溶液 | 无明显现象 | ______ |
| ②另取烧杯中上层清液少许于试管中,滴加______(指示剂除外) | _______ | 有大量OH- |
活动四:同学们将久置而变质的氢氧化钠样品与稀硫酸反应,欲通过测定CO
2的质量,从而计算碳酸钠的质量分数。他们设计了如图4所示装置进行实验(装置气密性良好)。
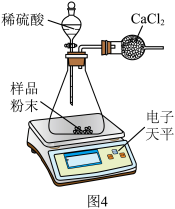
查阅文献得知:无水CaCl
2只吸收水而不吸收二氧化碳。
(6)①盛装药品后,称得总质量为m
1。
②逐滴加入稀硫酸至不再产生气泡。待电子天平读数不再改变时,称得总质量为m
2。同学们将(m
1-m
2)作为CO
2质量,计算碳酸钠的质量分数,你认为计算得到的值与真实值比较
_______(填“偏大”、“偏小”或“不变”),理由是
______。