山东省济南市平阴县第一中学2021-2022学年高一上学期10月阶段检测化学试题
山东
高一
阶段练习
2021-10-31
232次
整体难度:
适中
考查范围:
认识化学科学、常见无机物及其应用、化学实验基础
山东省济南市平阴县第一中学2021-2022学年高一上学期10月阶段检测化学试题
山东
高一
阶段练习
2021-10-31
232次
整体难度:
适中
考查范围:
认识化学科学、常见无机物及其应用、化学实验基础
一、单选题 添加题型下试题
单选题
|
较易(0.85)
名校
解题方法
1. 2016年诺贝尔化学奖授予三位科学家,以表彰他们在“分子机器的设计与合成” 的重大贡献。他们利用原子、分子的组合,构建分子水平上的机器。下列说法不正确的是
| A.化学是一门具有创造性的科学,化学的特征是认识分子和制造分子 |
| B.化学是在原子、分子的水平上研究物质的一门自然科学 |
| C.化学可以利用化学变化制造出新的原子和新的分子 |
| D.化学家可以在微观层面操纵分子和原子,组装分子材料 |
您最近一年使用:0次
2020-10-15更新
|
129次组卷
|
4卷引用:山东省六校2020-2021学年高一上学期阶段性联合考试化学试题
单选题
|
较易(0.85)
解题方法
2. 下列关于钠的叙述中,不正确的是
| A.钠加入到稀盐酸溶液中,溶液质量增加 |
| B.实验室未用完的金属钠应放回原试剂瓶 |
| C.钠在氯气中燃烧,产生黄色火焰 |
| D.金属钠着火,可以用泡沫灭火器灭火 |
您最近一年使用:0次
2020-10-15更新
|
154次组卷
|
5卷引用:山东省六校2020-2021学年高一上学期阶段性联合考试化学试题
单选题
|
较易(0.85)
名校
解题方法
3. 下列有关氯气的说法正确的是
| A.Fe可在Cl2中剧烈燃烧,生成物溶于水后呈现红褐色 |
| B.氯气有毒,为了防止污染环境,多余的氯气可以用饱和NaCl溶液吸收 |
| C.检验HCl气体中是否混有Cl2的方法是将气体通入硝酸银溶液 |
| D.氯气泄漏,可用浸透肥皂液的毛巾捂住口鼻,向高处转移 |
您最近一年使用:0次
2020-10-15更新
|
428次组卷
|
7卷引用:山东省六校2020-2021学年高一上学期阶段性联合考试化学试题
单选题
|
适中(0.65)
4. NA是阿伏加德罗常数的值。下列说法正确的是
| A.1molNa2O2固体中含离子总数为4NA |
| B.标准状况下2NA个SO3的体积为44.8L |
| C.常温下,4.8gO2和O3组成的混合气体中所含有原子数为0.3NA |
| D.0.1mol·L-1Na2CO3溶液中Na+数为0.2NA |
【知识点】 阿伏加德罗常数的应用解读 三氧化硫 过氧化钠
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
5. 下列关于钠及其化合物的叙述中,正确的是
| A.Na2O、Na2O2与水反应实验现象相同 |
| B.钠钾合金熔点低,可做原子反应堆的导热剂 |
| C.钠投入硫酸铜溶液中可以观察到红色物质出现 |
| D.长距离运输鱼苗,最好在水中加入一定量的Na2O2,以起到供氧和杀菌的作用 |
您最近一年使用:0次
单选题
|
较易(0.85)
解题方法
6. 某同学使用氯气消毒过的自来水进行溶液的配制,对实验结果无影响的是
①NaCl溶液 ②NaHCO3溶液 ③AgNO3溶液 ④FeCl3溶液 ⑤NaOH溶液
①NaCl溶液 ②NaHCO3溶液 ③AgNO3溶液 ④FeCl3溶液 ⑤NaOH溶液
| A.①④ | B.④⑤ | C.①④⑤ | D.①②③⑤ |
您最近一年使用:0次
2020-10-15更新
|
122次组卷
|
2卷引用:山东省六校2020-2021学年高一上学期阶段性联合考试化学试题
单选题
|
适中(0.65)
名校
解题方法
7. 正确的实验操作是实验成功的重要因素,下列实验操作正确的是
 | 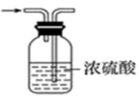 | 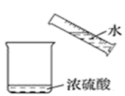 |  |
| ①闻气体气味 | ②干燥氯气 | ③稀释浓硫酸 | ④证明Cl2可与NaOH反应 |
| A.①② | B.②③ | C.①④ | D.③④ |
您最近一年使用:0次
2021-10-24更新
|
172次组卷
|
2卷引用:山东省济南市平阴县第一中学2021-2022学年高一上学期10月阶段检测化学试题
单选题
|
适中(0.65)
8. 下列叙述中,正确的是
| A.等物质的量浓度的盐酸和硫酸中,H+的物质的量浓度也相等 |
| B.标准状况下,22.4LHCl气体溶于100mL水后形成的溶液物质的量浓度为10mol·L-1 |
| C.同温同压下,等质量的SO2和CO2物质的量之比为16:11 |
| D.常温常压下,2.24LN2含有的氮原子数小于0.2NA |
您最近一年使用:0次
单选题
|
较易(0.85)
解题方法
9. 1g NH3中含有a个原子,则阿伏加 德罗常数可表示为
A. mol-1 mol-1 | B.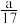 mol-1 mol-1 | C. mol-1 mol-1 | D. mol-1 mol-1 |
您最近一年使用:0次
2020-10-15更新
|
179次组卷
|
4卷引用:山东省六校2020-2021学年高一上学期阶段性联合考试化学试题
单选题
|
较易(0.85)
解题方法
10. 下列说法正确的是
| A.元素在自然界中都既有游离态又有化合态 |
| B.碱性氧化物一定是金属氧化物,酸性氧化物不一定是非金属氧化物 |
| C.根据化合物中含氢数目的多少,把化合物分为一元酸、二元酸、三元酸等 |
| D.根据是否只含一种元素将物质分为单质和化合物 |
【知识点】 单质和化合物解读 酸、碱、盐、氧化物的概念及其相互联系解读
您最近一年使用:0次
2021-10-24更新
|
145次组卷
|
2卷引用:山东省济南市平阴县第一中学2021-2022学年高一上学期10月阶段检测化学试题
单选题
|
较易(0.85)
名校
解题方法
11. 下列变化不能通过一步化学反应实现的是( )
| A.BaCl2→BaSO4 | B.CuO→Cu(OH)2 | C.NaOH→Na2SO3 | D.MgSO4→Mg(OH)2 |
您最近一年使用:0次
2020-09-10更新
|
2514次组卷
|
31卷引用:贵州省桐梓县育才中学2019-2020学年高二上学期开学考试化学试题
贵州省桐梓县育才中学2019-2020学年高二上学期开学考试化学试题辽宁省阜新市海州高级中学2019-2020学年高一10月月考化学试题2020年春季苏教版高中化学必修1专题一《化学家眼中的物质世界》测试卷云南省昭通市巧家县第四中学2019-2020学年高一上学期期末考试化学试题江苏省启东中学2020-2021学年高一上学期期初考试化学试题人教版(2019)高一必修第一册第一章 物质及其变化 第一节 物质的分类及转化课时2 物质的转化(已下线)1.1.2 物质的转化(重点练)-2020-2021学年高一化学上学期十分钟同步课堂专练(人教版2019必修第一册)高一必修第一册(苏教2019版)专题1 第一单元 物质及其反应的分类(已下线)【浙江新东方】hzomo化学001云南省昆明师范专科学校附属中学2020-2021学年高一上学期期中考试化学试题广西岑溪市2020-2021学年高二上学期期中考试化学(理)试题(已下线)【浙江新东方】【2020】【高一上】【期中】【hd-lp414】【化学】新疆维吾尔族自治区哈密市第十五中学2020-2021学年高一上学期期末考试化学试题辽宁省庄河市高级中学2021-2022学年高一10月月考化学试题山东省济南市平阴县第一中学2021-2022学年高一上学期10月阶段检测化学试题福建省南安市侨光中学2021-2022学年高一上学期第一次阶段考化学试题甘肃省甘南舟曲县第一中学2021-2022学年高一上学期第一次月考化学试卷黑龙江省海林市朝鲜族中学2020-2021学年高一上学期第一次月考化学试题新疆维吾尔自治区疏勒县2022 届高三第一次调研测试化学试题(已下线)专题05元素及其化合物-2022年高考真题+模拟题汇编(全国卷)(已下线)专题05元素及其化合物-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题05元素及其化合物-五年(2018~2022)高考真题汇编(全国卷)(已下线)衔接点05 物质间的相互转化-2022年初升高化学无忧衔接青海省西宁市湟中区多巴高级中学2021-2022学年高一下学期第一次月考化学试题江苏省淮安市涟水县第一中学2022-2023学年高一上学期第二次阶段检测化学试题河南省许昌市鄢陵县职业教育中心2021—2022学年高一上学期升学班第一次月考化学试题广西梧州市藤县第七中学2021-2022学年高一10月月考化学试题黑龙江省佳木斯市第八中学2021-2022学年高一上学期期中考试化学试题吉林省舒兰市第十八中学校2022-2023学年高一上学期期中考试化学试题(已下线)第2讲 物质的转化-【暑假自学课】2023年新高一暑假精品课(苏教版2019必修第一册)广东省梅州市大埔县虎山中学2023-2024学年高一上学期11月期中化学试题
单选题
|
较易(0.85)
解题方法
12. 下列叙述中不正确的是
| A.在豆浆里加入盐卤做豆腐利用了胶体聚沉的原理 |
| B.当可见光束照射蛋白质溶液时,在侧面可看到光亮的“通路” |
| C.根据分散系的稳定性大小将混合物分为胶体、溶液和浊液 |
| D.电泳实验说明了胶体微粒带电荷 |
您最近一年使用:0次
二、多选题 添加题型下试题
多选题
|
适中(0.65)
13. 下列判断正确的是
| A.200mL1mol·L-1FeCl3溶液和100mL3mol·L-1的NH4Cl溶液中Cl-物质的量浓度相等 |
| B.探究物质性质的基本程序:观察外观→做实验并观察实验现象→分析解释,得出结论 |
| C.2gH2和CO的混合气体充分燃烧,产物被Na2O2完全吸收,Na2O2固体增重2g |
| D.2mol水的摩尔质量是1mol水的摩尔质量的2倍 |
您最近一年使用:0次
三、单选题 添加题型下试题
单选题
|
容易(0.94)
解题方法
14. 下列说法正确的是
| A.向久置的氯水中滴加紫色石蕊试液,现象先变红后褪色 |
| B.新制的氯水能使有色布条褪色,说明氯气有漂白性 |
| C.为了提高漂白粉的漂白效果,使用时可以滴加少量的稀盐酸 |
| D.氯气能与铁反应,所以液氯不易存放在钢瓶中 |
您最近一年使用:0次
2020-10-15更新
|
326次组卷
|
5卷引用:山东省六校2020-2021学年高一上学期阶段性联合考试化学试题
四、多选题 添加题型下试题
多选题
|
容易(0.94)
解题方法
15. 下列关于物质分类的正确组合是
酸性氧化物 | 碱性氧化物 | 酸 | 碱 | 盐 | |
A | CO2 | SiO2 | H2SO4 | Na2CO3 | NaHCO3 |
B | CO | Na2O | HCl | NaOH | NaCl |
C | SO2 | CuO | CH3COOH | KOH | KNO3 |
D | SO3 | CaO | HNO3 | Ca(OH)2 | CaCO3 |
| A.A | B.B | C.C | D.D |
【知识点】 无机物质的分类 酸、碱、盐、氧化物的概念及其相互联系解读
您最近一年使用:0次
五、填空题 添加题型下试题
填空题
|
较易(0.85)
16. 回答下列问题
(1)化合物A分子组成可用OxFy表示。30mLA气体在一定条件下能分解生成15mLO2和30mLF2(在同温同压下),A的化学式是___________ 。
(2)1.5molCH3COOH所含氧原子数跟___________ gH2O所含氧原子数相等。
(3)实验室现有Fe2(SO4)3溶液100mL,SO 的物质的量浓度为0.45mol·L-1,则Fe3+的物质的量浓度为
的物质的量浓度为0.45mol·L-1,则Fe3+的物质的量浓度为___________ mol·L-1,含有Fe2(SO4)3的物质的量为___________ mol。
(4)N2和CH4的混合气体11g,在标准状况下的体积为11.2L,则混合气体的平均摩尔质量为___________ ,混合气体中N2和CH4的物质的量之比为___________ 。
(1)化合物A分子组成可用OxFy表示。30mLA气体在一定条件下能分解生成15mLO2和30mLF2(在同温同压下),A的化学式是
(2)1.5molCH3COOH所含氧原子数跟
(3)实验室现有Fe2(SO4)3溶液100mL,SO
 的物质的量浓度为0.45mol·L-1,则Fe3+的物质的量浓度为
的物质的量浓度为0.45mol·L-1,则Fe3+的物质的量浓度为(4)N2和CH4的混合气体11g,在标准状况下的体积为11.2L,则混合气体的平均摩尔质量为
您最近一年使用:0次
六、解答题 添加题型下试题
解答题-实验探究题
|
适中(0.65)
名校
解题方法
17. 某校化学兴趣小组为研究氯气的性质并模拟工业制备漂白粉,设计了下列装置进行实验。已知:装置A 中反应为 KClO3+6HCl(浓) = KCl+3Cl2↑+3H2O;

(1)写出B装置中反应的化学方程式______________________________ 。实验结束后,立即将B中溶液滴几滴在蓝色石蕊试纸上,可观察到的现象是_______________________ 。
(2)装置C的实验目的是验证氯气是否具有漂白性,为此C中 I、II、III 处依次放入的物质正确的是____________ 。①干燥的有色布条 ②湿润的有色布条 ③浓硫酸 ④碱石灰(固体氢氧化钠和氧化钙组成的混合物)
A.①④② B.①③② C.②③① D.②④①
(3)待 E 中物质完全反应后,经过一系列加工处理得到漂白粉样品,反应化学方程式__________________________________ ,漂白粉有效成分为____________ (填化学式)。
(4)F 装置的作用是__________________ ,盛放的试剂是____________________ 。
(5)装置A中反应生成标准状况下氯气的体积为13.44L,则需消耗KClO3的物质的量为__________ mol。

(1)写出B装置中反应的化学方程式
(2)装置C的实验目的是验证氯气是否具有漂白性,为此C中 I、II、III 处依次放入的物质正确的是
A.①④② B.①③② C.②③① D.②④①
(3)待 E 中物质完全反应后,经过一系列加工处理得到漂白粉样品,反应化学方程式
(4)F 装置的作用是
(5)装置A中反应生成标准状况下氯气的体积为13.44L,则需消耗KClO3的物质的量为
您最近一年使用:0次
2020-10-15更新
|
228次组卷
|
4卷引用:山东省六校2020-2021学年高一上学期阶段性联合考试化学试题
山东省六校2020-2021学年高一上学期阶段性联合考试化学试题山东省济南市平阴县第一中学2021-2022学年高一上学期10月阶段检测化学试题(已下线)第11讲 氧化还原反应的应用和配平-【暑假自学课】2022年新高一化学暑假精品课(鲁科版2019必修第一册)江苏省无锡市江苏省太湖高级中学2022年高一上学期期中考试化学试题
解答题-实验探究题
|
适中(0.65)
名校
解题方法
18. 实验室常用浓盐酸的质量分数为36.5%,密度为1.20 g/cm3。
(1)此盐酸的物质的量浓度为_____ 。
(2)需要230 mL3.0 mol·L-1的盐酸,配制时需以上浓盐酸的体积为_____ mL。
(3)上述实验中所用到的玻璃仪器有烧杯、玻璃棒、量筒以及_____ (两种仪器)。
(4)用浓盐酸配制3.00 mol·L-1稀盐酸,操作步骤的正确顺序是________ (填字母代号)。
a.计算需要浓盐酸的体积
b.用量筒量取浓盐酸
c.将烧杯中的溶液注入所需容积的容量瓶中,瓶用少量蒸馏水洗涤烧杯和玻璃棒2~3次,洗涤液也注入容量瓶
d.把量好体积的浓盐酸倒入烧杯中,加适量蒸馏水稀释,冷却
e.盖好瓶塞,反复上下颠倒,摇匀
f.继续向容量瓶中加蒸馏水至刻度线下1~2 cm处,改用某仪器小心滴加蒸馏水至凹液面与刻度线相平
(5)下列操作使溶液物质的量浓度偏高的是:________ 。
A.量取浓盐酸时仰视刻度线
B.容量瓶洗净后未经干燥处理
C.未冷却至室温就转移定容
D.将洗涤量筒的洗涤液转移到容量瓶中
E.定容时俯视刻度线
F.摇匀后立即观察,发现溶液未达到刻度线,再加几滴蒸馏水至刻度线
(1)此盐酸的物质的量浓度为
(2)需要230 mL3.0 mol·L-1的盐酸,配制时需以上浓盐酸的体积为
(3)上述实验中所用到的玻璃仪器有烧杯、玻璃棒、量筒以及
(4)用浓盐酸配制3.00 mol·L-1稀盐酸,操作步骤的正确顺序是
a.计算需要浓盐酸的体积
b.用量筒量取浓盐酸
c.将烧杯中的溶液注入所需容积的容量瓶中,瓶用少量蒸馏水洗涤烧杯和玻璃棒2~3次,洗涤液也注入容量瓶
d.把量好体积的浓盐酸倒入烧杯中,加适量蒸馏水稀释,冷却
e.盖好瓶塞,反复上下颠倒,摇匀
f.继续向容量瓶中加蒸馏水至刻度线下1~2 cm处,改用某仪器小心滴加蒸馏水至凹液面与刻度线相平
(5)下列操作使溶液物质的量浓度偏高的是:
A.量取浓盐酸时仰视刻度线
B.容量瓶洗净后未经干燥处理
C.未冷却至室温就转移定容
D.将洗涤量筒的洗涤液转移到容量瓶中
E.定容时俯视刻度线
F.摇匀后立即观察,发现溶液未达到刻度线,再加几滴蒸馏水至刻度线
您最近一年使用:0次
2020-10-22更新
|
385次组卷
|
4卷引用:山东省枣庄市第三中学2020-2021学年高一上学期10月月考化学试题
山东省枣庄市第三中学2020-2021学年高一上学期10月月考化学试题(已下线)专题03 溶液——备战2021年高考化学纠错笔记(已下线)专题02 物质的量在化学实验中的应用(热点讲义)-2022届高考化学一轮复习热点题型归纳与变式训练山东省济南市平阴县第一中学2021-2022学年高一上学期10月阶段检测化学试题
解答题-实验探究题
|
适中(0.65)
名校
解题方法
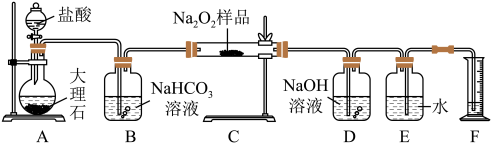
19. 过氧化钠常作漂白剂、杀菌剂、消毒剂。过氧化钠保存不当容易吸收空气中CO2而变质。某课外活动小组为了粗略测定过氧化钠的纯度,他们称取a g样品,并设计用如图装置来测定过氧化钠的质量分数。
①将仪器连接好以后,必须进行的第一步操作是_____ 。
②B装置出来的气体是否需要干燥______ (填“是”或“否”)。
③D中NaOH溶液的作用_________ 。
④实验结束时,读取实验中生成气体的体积时,不合理的是_____ 。
a.直接读取气体体积,不需冷却到室温
b.上下移动量筒,使得E、F中液面高度相同
c.视线与凹液面的最低点相平读取量筒中水的体积
⑤读出量筒内水的体积后,折算成标准状况下氧气的体积为V mL,则样品中过氧化钠的质量分数为____ 。
⑥实验完成后E到F之间导管内残留水的体积会使测量结果________ (填“偏大”“偏小”或“不影响”)。
①将仪器连接好以后,必须进行的第一步操作是
②B装置出来的气体是否需要干燥
③D中NaOH溶液的作用
④实验结束时,读取实验中生成气体的体积时,不合理的是
a.直接读取气体体积,不需冷却到室温
b.上下移动量筒,使得E、F中液面高度相同
c.视线与凹液面的最低点相平读取量筒中水的体积
⑤读出量筒内水的体积后,折算成标准状况下氧气的体积为V mL,则样品中过氧化钠的质量分数为
⑥实验完成后E到F之间导管内残留水的体积会使测量结果
您最近一年使用:0次
2019-12-18更新
|
128次组卷
|
2卷引用:江西省上饶市上饶中学2019-2020学年高一上学期第二次月考化学(零奥班)试题
七、填空题 添加题型下试题
填空题
|
适中(0.65)
解题方法
20. 已知铝是一种能够和强碱溶液反应生成氢气的一种特殊金属,其反应的化学方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑,现向500mLNaOH溶液中投入10.8gAl,二者恰好完全反应,计算:
(1)Al的物质的量为___________ mol。
(2)参加反应的NaOH的物质的量为___________ mol;溶液的物质的量浓度___________ mol·L-1。
(3)生成的H2在标准状况下的体积为___________ L;含有的电子数为___________ 。
(1)Al的物质的量为
(2)参加反应的NaOH的物质的量为
(3)生成的H2在标准状况下的体积为
您最近一年使用:0次
试卷分析
整体难度:适中
考查范围:认识化学科学、常见无机物及其应用、化学实验基础
试卷题型(共 20题)
题型
数量
单选题
13
多选题
2
填空题
2
解答题
3
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 化学科学特点 化学研究基本方法 | |
| 2 | 0.85 | 钠 钠的化学性质 过氧化钠 | |
| 3 | 0.85 | 氯气的物理性质 氯气的化学性质 氯气与碱溶液反应 | |
| 4 | 0.65 | 阿伏加德罗常数的应用 三氧化硫 过氧化钠 | |
| 5 | 0.65 | 钠单质的保存与用途 钠与盐溶液的反应 过氧化钠与水的反应 | |
| 6 | 0.85 | 氯水的性质 | |
| 7 | 0.65 | 氯气与碱溶液反应 硫酸 化学实验基础操作 物质分离、提纯的常见化学方法 | |
| 8 | 0.65 | 气体摩尔体积 阿伏加德罗定律 物质的量浓度的计算 根据n=m/M进行相关计算 | |
| 9 | 0.85 | 阿伏加德罗常数的求算 根据n=m/M进行相关计算 结合物质结构基础知识与NA相关推算 | |
| 10 | 0.85 | 单质和化合物 酸、碱、盐、氧化物的概念及其相互联系 | |
| 11 | 0.85 | 物质的转化 含硫化合物之间的转化 含镁化合物 氧化铜 | |
| 12 | 0.85 | 胶体 分散系概念及其分类 胶体的定义及分类 胶体的性质和应用 | |
| 14 | 0.94 | 氯气与金属单质的反应 新制氯水与久置氯水的区别 漂白粉和漂粉精的用途 | |
| 二、多选题 | |||
| 13 | 0.65 | 摩尔质量 物质的量有关计算 过氧化钠与水的反应 过氧化钠和二氧化碳反应 | |
| 15 | 0.94 | 无机物质的分类 酸、碱、盐、氧化物的概念及其相互联系 | |
| 三、填空题 | |||
| 16 | 0.85 | 阿伏加德罗定律的应用 根据n=m/M进行相关计算 以N=m·NA/M为中心的有关基本粒子的推算 依据物质的量浓度公式的基础计算 | |
| 20 | 0.65 | 物质的量浓度的计算 根据n=m/M进行相关计算 化学方程式计算中物质的量的运用 | |
| 四、解答题 | |||
| 17 | 0.65 | 化学方程式计算中物质的量的运用 氯气的制法 氯气的实验室制法 综合实验设计与评价 | 实验探究题 |
| 18 | 0.65 | 物质的量浓度计算-溶液配制有关计算 配制一定物质的量浓度的溶液的步骤、操作 配制一定物质的量浓度的溶液实验的误差分析 配制一定物质的量浓度的溶液实验的仪器 | 实验探究题 |
| 19 | 0.65 | 过氧化钠和二氧化碳反应 常见气体的制备与收集 探究物质组成或测量物质的含量 综合实验设计与评价 | 实验探究题 |



