2015-2016学年山东省桓台二中高二6月月考化学试卷
山东
高二
阶段练习
2017-07-27
212次
整体难度:
适中
考查范围:
认识化学科学、常见无机物及其应用、化学实验基础
一、单选题 添加题型下试题
| A.“雨后彩虹”是一种自然现象,与胶体的知识有关 |
| B.“农夫山泉”纯净水不含任何化学成分 |
| C.“通风橱”是一种负责任的防污染手段,可使有害气体得到转化或吸收 |
| D.长期盛放NaOH溶液的滴瓶不易打开,是因为NaOH与瓶中的CO2反应使瓶内气体减少形成“负压”之故 |
【知识点】 分散系
| A.硅是人类将太阳能转变为电能的常用材料 |
| B.工艺师利用盐酸刻蚀石英制作艺术品 |
| C.水晶项链和餐桌上的瓷盘都是硅酸盐制品 |
| D.粗硅制备单晶硅不涉及氧化还原反应 |
【知识点】 碳族元素及其化合物
| A.硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物 |
| B.蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质 |
| C.Mg、Al、Cu可以分别用置换法、直接加热法和电解法冶炼得到 |
| D.天然气、乙醇和水煤气分别属于化石能源、不可再生能源和二次能源 |
【知识点】 物质的分类
| A.刚落下的酸雨酸性逐渐增强,是由于雨水所含成分被不断氧化的原因 |
| B.阳离子只能得到电子被还原,阴离子只能失去电子被氧化 |
| C.加热NH4Cl晶体时,将湿润的红色石蕊试纸靠近试管口,检验NH3的生成 |
| D.钠原子在反应中失去的电子比铝原子少,故钠的金属性在理论上应弱于铝的金属性 |
【知识点】 钠及其化合物
| A.1molNa2O2与CO2反应产生,转移的电子数为4NA |
| B.标准状况下,11.2L H2O中含有的电子数为5NA |
| C.1mol/L Al2(SO4)3溶液中含Al3+数为2NA |
| D.常温常压下,14g N2所含的原子数目为NA |
【知识点】 化学计量
| A.钠与水反应:2Na+2H2O=2Na+ +2OH-+H2↑ |
| B.向碳酸氢钠溶液中滴加盐酸:2H+ +CO32-=H2O+CO2↑ |
| C.氯气与水反应:Cl2+H2O=2H+ +Cl-+ClO- |
| D.向溴化亚铁溶液中通入少量氯气:Cl2+2Br-=2Cl-+Br2 |
【知识点】 离子反应的发生及书写
| A.Al3+、NH4+、AlO2-、Cl- |
| B.Cu2+、Fe2+、ClO-、SO42- |
| C.Na+、Ca2+、HCO3-、OH- |
| D.Cu2+、Fe3+、Cl-、NO3- |
【知识点】 离子共存
| A.气体质量 | B.气体的物质的量 | C.分子总数 | D.原子数 |
| A.烧杯中有铜、无铁 | B.烧杯中有铁、无铜 |
| C.烧杯中铁、铜都有 | D.烧杯中铁、铜都无 |
【知识点】 Fe、Cu与Fe3+反应几种情况分析及判断
| A.有2个氧原子 | B.有1个氧原子 |
| C.有1个A原子 | D.有2个A原子 |
【知识点】 阿伏加德罗定律的应用解读 无机综合推断
| 代号 | 实验内容 | 实验目的 |
| A | Cl2、Br2分别与H2反应 | 比较氯与溴的非金属性强弱 |
| B | 向饱和Na2SiO3溶液中通入二氧化碳 | 比较碳与硅的非金属性强弱 |
| C | 把碳酸钠与亚硫酸钠放置在空气中 | 比较碳与硫的还原性强弱 |
| D | 向氯化铜溶液中加入铁丝 | 比较铁与铜的还原性强弱 |
| A.A | B.B | C.C | D.D |
【知识点】 化学实验基础
| A.实验①能够证明Cl-具有还原性 |
| B.上述实验能够证明氧化性:Cl2 >Br2 |
| C.上述实验能够证明氧化性:MnO4->Cl2 >Fe3+ >I2 |
| D.由上述实验不能判断氯气能使湿润的淀粉KI试纸变蓝 |
【知识点】 氧化还原反应基本概念 氧化还原反应的规律解读

| A.装置①是洗气装置,可以除去氯气中的氯化氢 |
| B.实验室可以用装置②制取氨气 |
| C.实验室用装置③做“喷泉”实验不能成功 |
| D.装置④中X若为四氯化碳,可用于吸收氨气,并防止倒吸 |
二、填空题 添加题型下试题
(2)某混合溶液中可能含有的离子如下表所示:
| 可能大量含有的阳离子 | H+、Mg2+、Al3+、NH4+、Fe3+ |
| 可能大量含有的阴离子 | Cl-、Br-、CO32-、AlO2- |
为探究其成分,进行了以下探究实验。
甲同学取一定量的混合溶液,向其中逐滴加入氢氧化钠溶液,产生沉淀的物质的量(n)与加入氢氧化钠溶液的体积(V)的关系如图所示。

①该溶液中一定含有的阳离子是
②请写出沉淀减少过程中发生反应的离子方程式
【知识点】 离子反应
三、解答题 添加题型下试题
(1)你认为两同学的观点中正确的是
A.酸性高锰酸钾溶液
B.氢氧化钠溶液
C.四氯化碳
D.硫氰化钾溶液
E.硝酸银溶液
判断:请用原理不同的两种方法加以验证,将选用的试剂编号及实验中观察到的现象填入下表:
| 选用试剂 | 实验现象 | |
| 第一种方法 | ||
| 第二种方法 |
(2)若选用淀粉碘化钾溶液判断两个同学的观点哪个正确,是否可行?若可行,本问不需回答,若不可行请说明原因:
(3)若要把溶解于水中的Br2单质分离出来,所需要的主要玻璃仪器是
该操作的名称是
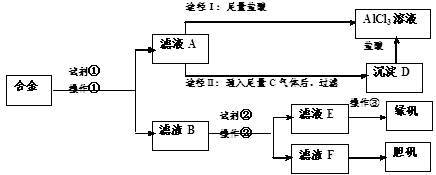
试回答下列问题:
(1)所加试剂①、②分别是
(2)操作①的名称为
(3)由滤液A制AlCl3溶液有途径Ⅰ和途径Ⅱ两种,你认为合理的是
写出A→D反应离子方程式:
(4)操作③的名称是
(5)丙同学提出可将方案中最初溶解合金的试剂①改为盐酸,重新设计方案,也能得到三种物质,你认为后者的方案比原方案是否更合理:
【知识点】 物质分离、提纯综合应用解读

Ⅱ.下图是用过量的铜与40mL稀硝酸在100mL烧瓶中反应制取一氧化氮气体的实验装置图,请回答下列问题:


(1)请在右框中画出气体收集装置的装置图。
(2)①从烧瓶中取出少量反应后的溶液,滴入少量氨水,写出该反应的离子方程式:
②反应结束后,能否采取向烧瓶中再加入稀硫酸的方式,再获得一氧化氮气体?如果可以,请写出反应的离子方程式,如果不可以,请说明理由:
(3)检查上图装置气密性的操作是:

(1)除杂操作是加入氢氧化钙,调节溶液的pH为8.0~8.5,以除去溶液中的少量Al3+、Fe3+。检验Fe(OH)3是否沉淀完全的实验操作是
(2)酸化操作是加入盐酸,调节溶液的pH约为4.0,其目的有:①将溶液中的少量Ca(OH)2转化为CaCl2;②防止Ca2+在蒸发时水解;③
(3)测定样品中Cl-含量的方法是:a.称取0.7500g样品,溶解,在250 mL容量瓶中定容;b.量取25.00 mL待测溶液于锥形瓶中;c.用0.05000mol/LAgNO3溶液滴定至终点,消耗AgNO3溶液体积的平均值为20.39 mL。
①步骤a中进行定容操作时视线应
②上述测定过程中需用溶液润洗的仪器有
③计算上述样品中CaCl2·2H2O的质量分数为
④若用上述方法测定的样品中CaCl2·2H2O的质量分数偏高(测定过程中产生的误差可忽略),某同学认为偏高的原因可能是样品中存在少量的NaCl,要验证该同学的观点应进行的实验为
【知识点】 化学实验基础
试卷分析
试卷题型(共 19题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.64 | 分散系 | |
| 2 | 0.64 | 碳族元素及其化合物 | |
| 3 | 0.64 | 物质的分类 | |
| 4 | 0.64 | 钠及其化合物 | |
| 5 | 0.64 | 化学计量 | |
| 6 | 0.64 | 离子反应的发生及书写 | |
| 7 | 0.64 | 离子共存 | |
| 8 | 0.65 | 离子的检验 常见阳离子的检验 常见阴离子的检验 | |
| 9 | 0.64 | 化学计量 阿伏加德罗定律 | |
| 10 | 0.65 | Fe、Cu与Fe3+反应几种情况分析及判断 | |
| 11 | 0.65 | 阿伏加德罗定律的应用 无机综合推断 | |
| 12 | 0.64 | 化学实验基础 | |
| 13 | 0.4 | 氧化还原反应基本概念 氧化还原反应的规律 | |
| 14 | 0.64 | 化学实验基础 卤素及其化合物 | |
| 二、填空题 | |||
| 15 | 0.15 | 离子反应 | |
| 三、解答题 | |||
| 16 | 0.4 | 综合实验设计与评价 | 实验探究题 |
| 17 | 0.4 | 物质分离、提纯综合应用 | 实验探究题 |
| 18 | 0.4 | 常见无机物的制备 | 实验探究题 |
| 19 | 0.4 | 化学实验基础 | 实验探究题 |



