2024届四川省南充市高三下学期适应性考试(二诊)理综试题-高中化学
四川
高三
二模
2024-04-03
414次
整体难度:
适中
考查范围:
有机化学基础、化学与STSE、认识化学科学、化学反应原理、常见无机物及其应用、化学实验基础、物质结构与性质
2024届四川省南充市高三下学期适应性考试(二诊)理综试题-高中化学
四川
高三
二模
2024-04-03
414次
整体难度:
适中
考查范围:
有机化学基础、化学与STSE、认识化学科学、化学反应原理、常见无机物及其应用、化学实验基础、物质结构与性质
一、单选题 添加题型下试题
单选题
|
适中(0.65)
解题方法
1. 化学与生活密不可分。下列说法正确的是
| A.用BaCO3作X射线透视肠胃的内服药剂 | B.棉花、麻和蚕丝均为碳水化合物 |
| C.活性炭具有除异味和杀菌作用 | D.使用含氟牙膏能预防龋齿 |
您最近一年使用:0次
单选题
|
适中(0.65)
2. 葡萄酒中含有 、
、 、
、 、
、 等多种成分,设NA为阿伏加德罗常数的值,下列说法正确的是
等多种成分,设NA为阿伏加德罗常数的值,下列说法正确的是
 、
、 、
、 、
、 等多种成分,设NA为阿伏加德罗常数的值,下列说法正确的是
等多种成分,设NA为阿伏加德罗常数的值,下列说法正确的是A. 溶液的pH为1 溶液的pH为1 |
B.100g46%的 溶液中,含H―O键数为NA 溶液中,含H―O键数为NA |
C.1mol 与1mol 与1mol 完全反应转移的电子数为4 NA 完全反应转移的电子数为4 NA |
D.标准状况下,22.4L 中含氧原子数大于NA 中含氧原子数大于NA |
【知识点】 物质结构基础与NA相关推算解读 溶液pH的计算
您最近一年使用:0次
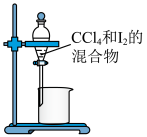
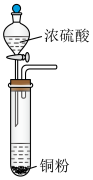
4. 下列实验能达到实验目的的是
| A | B |
|
|
分离 和 和 的混合物 的混合物 | 制取少量 气体 气体 |
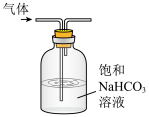
| C | D |
|
|
证明混合溶液中有少量 | 除去 气体中的少量 气体中的少量 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中(0.65)
5. 过二硫酸铵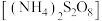 可用作氧化剂、漂白剂。利用电解法制备过二硫酸铵和过氧化氢的装置如图所示,下列说法错误的是
可用作氧化剂、漂白剂。利用电解法制备过二硫酸铵和过氧化氢的装置如图所示,下列说法错误的是
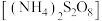 可用作氧化剂、漂白剂。利用电解法制备过二硫酸铵和过氧化氢的装置如图所示,下列说法错误的是
可用作氧化剂、漂白剂。利用电解法制备过二硫酸铵和过氧化氢的装置如图所示,下列说法错误的是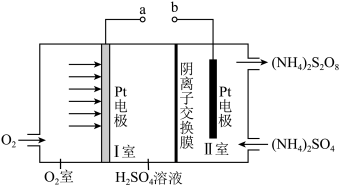
| A.过二硫酸铵中硫的化合价为+7价 |
| B.b连接电源的正极 |
C.I室Pt电极反应式为 |
D.标准状况下,22.4L 参与反应,理论上产生1mol 参与反应,理论上产生1mol |
您最近一年使用:0次
单选题
|
适中(0.65)
名校
解题方法
6. X、Y、Z、W是原子序数依次增大的四种短周期元素,X氢化物的水溶液可用于刻蚀玻璃,Y是地壳中含量最高的金属元素,Z原子的核外电子数是X最外层电子数的2倍,W的单质是制作黑火药的原料之一。下列结论正确的是( )
| A.工业上通过电解法获取Y的单质 |
| B.简单氢化物的沸点:X<W |
| C.简单离子半径大小:X>Y>W |
| D.最高价氧化物水化物的酸性:Z>W |
您最近一年使用:0次
2022-04-11更新
|
876次组卷
|
6卷引用:安徽省合肥市2022届高三第二次教学质量检测理综化学试题
安徽省合肥市2022届高三第二次教学质量检测理综化学试题(已下线)押全国卷理综第10题 元素周期表 元素周期律-备战2022年高考化学临考题号押题(课标全国卷)四川省南充市2022届高三适应性考试(三诊)理综化学试题四川省内江市第六中学2022-2023学年高二下学期第一次月考(创新班)化学试题2024届四川省南充市高三下学期适应性考试(二诊)理综试题-高中化学2024届四川省成都石室中学高三下学期5月高考适应性考试(一)理科综合试卷-高中化学
7. 一定温度下,AgCl和Ag2C2O4两种难溶化合物的溶解平衡曲线如图所示,下列说法中错误的是
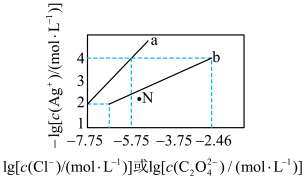
| A.a代表AgCl溶解平衡图像 |
| B.N点为Ag2C2O4的过饱和溶液 |
C.该温度下,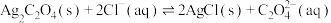 的平衡常数为10-0.71 的平衡常数为10-0.71 |
| D.向NaCl、Na2C2O4均为0.1 mol/L的混合溶液中滴加AgNO3溶液,Cl-先沉淀 |
【知识点】 难溶电解质的溶解平衡 溶度积常数相关计算解读
您最近一年使用:0次
二、解答题 添加题型下试题
解答题-实验探究题
|
较难(0.4)
解题方法
8. 某化学兴趣小组探究 与
与 溶液的反应,装置如下图:
溶液的反应,装置如下图:
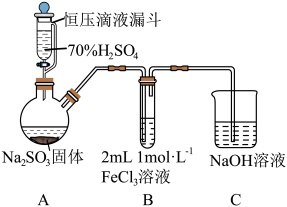
(1)该实验不用98%硫酸制取 的原因为
的原因为_______ 。
(2)【预测】 与
与 溶液反应可能出现的现象为溶液由黄色变成浅绿色,则浅绿色离子为
溶液反应可能出现的现象为溶液由黄色变成浅绿色,则浅绿色离子为_______ 。
(3)【实验探究】向装置B中溶液通入 至饱和,溶液立即由黄色变成红色。
至饱和,溶液立即由黄色变成红色。
①甲同学认为溶液变红的原因是通入 后,
后, 水解程度增大,形成
水解程度增大,形成 胶体,乙同学进行了实验操作:
胶体,乙同学进行了实验操作:_______ ,否定了该推论。
②静置5min后,溶液从红色恢复黄色。丙同学取适量该溶液,滴加盐酸酸化的 溶液,产生白色沉淀,则该同学认为
溶液,产生白色沉淀,则该同学认为 与
与 发生氧化还原反应,丁同学认为该操作不严谨,应把A装置换成如图装置,则通入氮气的目的为
发生氧化还原反应,丁同学认为该操作不严谨,应把A装置换成如图装置,则通入氮气的目的为_______ 。
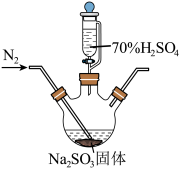
(4)【查阅资料】 能与S(Ⅳ)微粒形成红色配合物。
能与S(Ⅳ)微粒形成红色配合物。
①分析 的水溶液成分,猜想与
的水溶液成分,猜想与 形成配合物呈红色的含S(Ⅳ)微粒有:
形成配合物呈红色的含S(Ⅳ)微粒有: 、
、 、
、_______ 、_______ ,进行如下实验:
②根据实验I现象,可以推测红色物质与_______ 、_______ 无关 (填微粒化学式) 。
③对比实验I、II现象,pH越_______ (填“大”或“小”),配位反应进行的程度越大。
【实验结论】 的水溶液与
的水溶液与 溶液也可以发生配位反应。
溶液也可以发生配位反应。
 与
与 溶液的反应,装置如下图:
溶液的反应,装置如下图:
(1)该实验不用98%硫酸制取
 的原因为
的原因为(2)【预测】
 与
与 溶液反应可能出现的现象为溶液由黄色变成浅绿色,则浅绿色离子为
溶液反应可能出现的现象为溶液由黄色变成浅绿色,则浅绿色离子为(3)【实验探究】向装置B中溶液通入
 至饱和,溶液立即由黄色变成红色。
至饱和,溶液立即由黄色变成红色。①甲同学认为溶液变红的原因是通入
 后,
后, 水解程度增大,形成
水解程度增大,形成 胶体,乙同学进行了实验操作:
胶体,乙同学进行了实验操作:②静置5min后,溶液从红色恢复黄色。丙同学取适量该溶液,滴加盐酸酸化的
 溶液,产生白色沉淀,则该同学认为
溶液,产生白色沉淀,则该同学认为 与
与 发生氧化还原反应,丁同学认为该操作不严谨,应把A装置换成如图装置,则通入氮气的目的为
发生氧化还原反应,丁同学认为该操作不严谨,应把A装置换成如图装置,则通入氮气的目的为
(4)【查阅资料】
 能与S(Ⅳ)微粒形成红色配合物。
能与S(Ⅳ)微粒形成红色配合物。①分析
 的水溶液成分,猜想与
的水溶液成分,猜想与 形成配合物呈红色的含S(Ⅳ)微粒有:
形成配合物呈红色的含S(Ⅳ)微粒有: 、
、 、
、| 序号 | 实验 | 加入试剂 | 现象 |
| I | 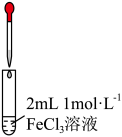 | 2mL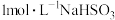 溶液,再滴加几滴盐酸 溶液,再滴加几滴盐酸 | 溶液变成红色,比(3)中溶液红色深;滴加盐酸后,溶液颜色由红色变成黄色 |
| II | 2mL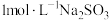 溶液 溶液 | 溶液变成红色,比Ⅰ中溶液红色深 |
③对比实验I、II现象,pH越
【实验结论】
 的水溶液与
的水溶液与 溶液也可以发生配位反应。
溶液也可以发生配位反应。
您最近一年使用:0次
解答题-原理综合题
|
较难(0.4)
9. Haber法是工业上常使用的合成氨技术,对该技术的改进一直是科学家探索的重要课题,其反应原理为:

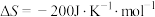 。回答下列问题:
。回答下列问题:
(1)已知:

1molN―H键断裂吸收的能量等于_______ kJ(保留一位小数),合成氨反应在常温(T=298K)下_______ (填“能”或“不能”)自发进行。
(2)将1.00mol 和3.00mol
和3.00mol 充入到容积为3L的恒容密闭容器中模拟反应,测得数据如下图所示。
充入到容积为3L的恒容密闭容器中模拟反应,测得数据如下图所示。

①图甲中反应达到平衡时的平均反应速率
_______ 。
②图乙的平衡体系中A、B、C三点的平衡常数 、
、 、
、 间的大小关系是
间的大小关系是_______ 。
(3)针对反应速率与平衡产率之间的矛盾,我国科学家研究发现采用M―LiH(M表示金属)复合催化剂能在较低的温度下合成 ,可有效缓解这一矛盾。300℃时,实验测得不同催化剂反应速率(用单位时间内每克催化剂所获得的
,可有效缓解这一矛盾。300℃时,实验测得不同催化剂反应速率(用单位时间内每克催化剂所获得的 的物质的量表示)如图所示:
的物质的量表示)如图所示:

①无LiH,催化效率最高的金属是_______ 。
②有LiH,反应速率明显增大。文献报道了M―LiH可能的催化历程经如下三步完成。
第ⅰ步: (在M表面解离)
(在M表面解离)
第ⅱ步:
第ⅲ步:_______ 。
(4)工业上需考虑多种因素提高合成氨产率,其措施有:加入合适的催化剂、调控适宜温度、_______ 、_______ 。


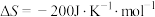 。回答下列问题:
。回答下列问题:(1)已知:

1molN―H键断裂吸收的能量等于
(2)将1.00mol
 和3.00mol
和3.00mol 充入到容积为3L的恒容密闭容器中模拟反应,测得数据如下图所示。
充入到容积为3L的恒容密闭容器中模拟反应,测得数据如下图所示。
①图甲中反应达到平衡时的平均反应速率

②图乙的平衡体系中A、B、C三点的平衡常数
 、
、 、
、 间的大小关系是
间的大小关系是(3)针对反应速率与平衡产率之间的矛盾,我国科学家研究发现采用M―LiH(M表示金属)复合催化剂能在较低的温度下合成
 ,可有效缓解这一矛盾。300℃时,实验测得不同催化剂反应速率(用单位时间内每克催化剂所获得的
,可有效缓解这一矛盾。300℃时,实验测得不同催化剂反应速率(用单位时间内每克催化剂所获得的 的物质的量表示)如图所示:
的物质的量表示)如图所示:
①无LiH,催化效率最高的金属是
②有LiH,反应速率明显增大。文献报道了M―LiH可能的催化历程经如下三步完成。
第ⅰ步:
 (在M表面解离)
(在M表面解离)第ⅱ步:

第ⅲ步:
(4)工业上需考虑多种因素提高合成氨产率,其措施有:加入合适的催化剂、调控适宜温度、
您最近一年使用:0次
解答题-工业流程题
|
适中(0.65)
解题方法
10. 一种废旧磷酸铁锂正极片(主要成分为LiFePO4、FePO4、Al和石墨)的闭环回收工艺流程如图所示:
②滤饼成分为Fe3(PO4)2·8H2O。
回答下列问题:
(1)碱溶前,可将废电池正极片进行机械活化处理,使颗粒直径减小,目的是_______ 。
(2)向滤液①中通入过量二氧化碳,可以回收铝,该反应的离子方程式为_______ 。
(3)酸浸过程中加入C6H8O6的目的是_______ 。
(4)将不同pH下得到的滤饼溶于盐酸,稀释至一定比例后测算Fe、P物质的量比 ,结果见下表,由此得出,沉淀的最佳pH为
,结果见下表,由此得出,沉淀的最佳pH为_______ 。
(5)调节pH时,氨水不宜加入过量,原因是随着氨水浓度的增大,会产生_______ 杂质;若该步骤中Fe元素沉淀完全,滤液③中除H、O外,还大量含有的元素有_______ 。
(6)真空管烧结时,加入葡萄糖的作用是_______ 。

②滤饼成分为Fe3(PO4)2·8H2O。
回答下列问题:
(1)碱溶前,可将废电池正极片进行机械活化处理,使颗粒直径减小,目的是
(2)向滤液①中通入过量二氧化碳,可以回收铝,该反应的离子方程式为
(3)酸浸过程中加入C6H8O6的目的是
(4)将不同pH下得到的滤饼溶于盐酸,稀释至一定比例后测算Fe、P物质的量比
 ,结果见下表,由此得出,沉淀的最佳pH为
,结果见下表,由此得出,沉淀的最佳pH为| pH | 6.0 | 6.5 | 7.0 | 8.0 | 9.0 |
 | 1.54 | 1.50 | 1.49 | 1.47 | 1.47 |
(6)真空管烧结时,加入葡萄糖的作用是
您最近一年使用:0次
解答题-结构与性质
|
适中(0.65)
解题方法
11. 早在2000多年前我国已掌握铜镍合金的冶炼,但直到250年前才有科学家制得单质镍。回答下列问题:
(1)基态镍原子的价电子排布式为_______ 。基态铜、镍原子的第二电离能分别为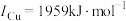 、
、 、
、 的原因是
的原因是_______ 。
(2)丁二铜肟常用于检验 。在稀氨水介质中,丁二酮肟与
。在稀氨水介质中,丁二酮肟与 反应生成鲜红色沉淀,其结构如图所示,该物质中:
反应生成鲜红色沉淀,其结构如图所示,该物质中:

①非金属元素电负性由大到小的顺序为_______ 。
②氢氧原子间存在_______ 作用。
③ 的配位数为
的配位数为_______ 。
④已知: 和N位于同一平面。可采用配合物的杂化轨道理论进行解释:
和N位于同一平面。可采用配合物的杂化轨道理论进行解释: 原有d电子可违反洪特规则进行重排,再利用外层空轨道杂化后接受N原子提供的孤对电子。则推测
原有d电子可违反洪特规则进行重排,再利用外层空轨道杂化后接受N原子提供的孤对电子。则推测 采用的杂化轨道类型为
采用的杂化轨道类型为_______ (填字母标号)。
A. B.
B. C.
C. D.
D.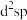
(3)二元铜镍固溶体称为普通白铜,其晶胞结构如图。
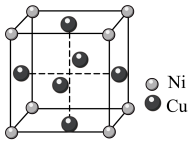
已知立方晶胞边长为acm,阿伏加德罗常数为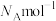 。
。
①该晶体类型为_______ ,Cu与Cu之间的最近距离为_______ pm。
②该晶体密度为_______  (用含
(用含 、a的式子表示)。
、a的式子表示)。
(1)基态镍原子的价电子排布式为
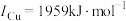 、
、 、
、 的原因是
的原因是(2)丁二铜肟常用于检验
 。在稀氨水介质中,丁二酮肟与
。在稀氨水介质中,丁二酮肟与 反应生成鲜红色沉淀,其结构如图所示,该物质中:
反应生成鲜红色沉淀,其结构如图所示,该物质中:
①非金属元素电负性由大到小的顺序为
②氢氧原子间存在
③
 的配位数为
的配位数为④已知:
 和N位于同一平面。可采用配合物的杂化轨道理论进行解释:
和N位于同一平面。可采用配合物的杂化轨道理论进行解释: 原有d电子可违反洪特规则进行重排,再利用外层空轨道杂化后接受N原子提供的孤对电子。则推测
原有d电子可违反洪特规则进行重排,再利用外层空轨道杂化后接受N原子提供的孤对电子。则推测 采用的杂化轨道类型为
采用的杂化轨道类型为A.
 B.
B. C.
C. D.
D.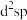
(3)二元铜镍固溶体称为普通白铜,其晶胞结构如图。

已知立方晶胞边长为acm,阿伏加德罗常数为
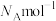 。
。①该晶体类型为
②该晶体密度为
 (用含
(用含 、a的式子表示)。
、a的式子表示)。
您最近一年使用:0次
解答题-有机推断题
|
适中(0.65)
12. 卡巴拉汀可用于治疗阿尔茨海默病,其中间体F的合成路线如下(部分试剂和条件略去):
(1)A的分子式为_______ 。由B生成C的反应类型为_______ 。
(2)C中含氮官能团的名称是_______ 。
(3)利用Eschweiler-Clarke反应(N-甲基化的一个经典反应)使C生成D,其第一步反应为: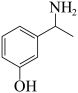
 ,有机产物X为
,有机产物X为_______ (写结构简式)。
(4)碳原子上连有4个不同的原子或基团时,该碳称为手性碳。每分子D中含手性碳原子_____ 个。
(5)E的结构简式为_______ 。
(6)在A的芳香族同分异构体中,同时满足下列条件的共有_______ 种;
①能发生银镜反应:②能与 溶液发生显色反应。
溶液发生显色反应。
其中,核磁共振氢谱为5组峰,且峰面积比为2∶2∶2∶1∶1的同分异构体的结构简式为______ 。

(1)A的分子式为
(2)C中含氮官能团的名称是
(3)利用Eschweiler-Clarke反应(N-甲基化的一个经典反应)使C生成D,其第一步反应为:

 ,有机产物X为
,有机产物X为(4)碳原子上连有4个不同的原子或基团时,该碳称为手性碳。每分子D中含手性碳原子
(5)E的结构简式为
(6)在A的芳香族同分异构体中,同时满足下列条件的共有
①能发生银镜反应:②能与
 溶液发生显色反应。
溶液发生显色反应。其中,核磁共振氢谱为5组峰,且峰面积比为2∶2∶2∶1∶1的同分异构体的结构简式为
您最近一年使用:0次
试卷分析
整体难度:适中
考查范围:有机化学基础、化学与STSE、认识化学科学、化学反应原理、常见无机物及其应用、化学实验基础、物质结构与性质
试卷题型(共 12题)
题型
数量
单选题
7
解答题
5
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 淀粉和纤维素 蛋白质 化学科学对人类文明发展的意义 药物的合理使用 | |
| 2 | 0.65 | 物质结构基础与NA相关推算 溶液pH的计算 | |
| 3 | 0.85 | 缩聚反应机理及判断 | |
| 4 | 0.65 | 氯气的实验室制法 二氧化硫的化学性质 Fe2+的鉴别及其应用 化学实验方案的设计与评价 | |
| 5 | 0.65 | 电解原理的应用 电解原理的理解及判断 电解池电极反应式及化学方程式的书写与判断 电解池有关计算 | |
| 6 | 0.65 | 金属与非金属在周期表中位置及其性质递变的规律 元素周期律的应用 微粒半径大小的比较方法 根据物质性质进行元素种类推断 | |
| 7 | 0.65 | 难溶电解质的溶解平衡 溶度积常数相关计算 | |
| 二、解答题 | |||
| 8 | 0.4 | 二氧化硫的制备 二氧化硫与其他强氧化剂的反应 配合物的结构与性质 化学实验方案的设计与评价 | 实验探究题 |
| 9 | 0.4 | 根据△H=反应物的键能之和-生成物的键能之和进行计算 化学反应速率计算 影响化学反应速率的内因 化学平衡的移动及其影响因素 | 原理综合题 |
| 10 | 0.65 | 偏铝酸钠与二氧化碳的反应 影响化学反应速率的其他因素 化学反应条件的控制及优化 | 工业流程题 |
| 11 | 0.65 | 电子排布式 利用杂化轨道理论判断化学键杂化类型 简单配合物的成键 晶胞的有关计算 | 结构与性质 |
| 12 | 0.65 | 根据要求书写同分异构体 多官能团有机物的结构与性质 有机推断综合考查 | 有机推断题 |