2024届河北省邯郸市高三下学期第四次调研检测化学试卷
河北
高三
模拟预测
2024-05-13
219次
整体难度:
适中
考查范围:
常见无机物及其应用、化学反应原理、认识化学科学、物质结构与性质、有机化学基础、化学实验基础
2024届河北省邯郸市高三下学期第四次调研检测化学试卷
河北
高三
模拟预测
2024-05-13
219次
整体难度:
适中
考查范围:
常见无机物及其应用、化学反应原理、认识化学科学、物质结构与性质、有机化学基础、化学实验基础
一、单选题 添加题型下试题
1. “挖掘文物价值,讲好中国故事。”下列文物在潮湿空气中易发生电化学腐蚀的是
| 选项 | A | B |
| 文物 |
|
|
| 名称 | 先锋煲(陶) | 翔鹭纹铜鼓 |
| 选项 | C | D |
| 文物 |
|
|
| 名称 | 弦纹玻璃杯 | 六棱柱形水晶穿珠 |
| A.A | B.B | C.C | D.D |
【知识点】 硅酸盐 金属的化学腐蚀与电化学腐蚀解读 吸氧腐蚀解读
您最近一年使用:0次
2024-05-14更新
|
97次组卷
|
2卷引用:2024届河北省邯郸市高三下学期第四次调研检测化学试卷
单选题
|
适中(0.65)
2. 亚氨基化硫(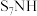 )的制备原理:
)的制备原理: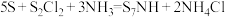 。下列化学用语表述正确的是
。下列化学用语表述正确的是
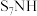 )的制备原理:
)的制备原理: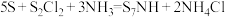 。下列化学用语表述正确的是
。下列化学用语表述正确的是A.基态S原子的价层电子排布式: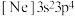 |
B. 的VSEPR模型: 的VSEPR模型: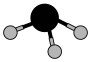 |
C. 的电子式: 的电子式: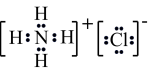 |
D. 的结构式: 的结构式: |
您最近一年使用:0次
2024-05-14更新
|
230次组卷
|
3卷引用:2024届河北省邯郸市高三下学期第四次调研检测化学试卷
单选题
|
较易(0.85)
您最近一年使用:0次
单选题
|
适中(0.65)
名校
4. 下列化学事实不符合“事物的双方既相互对立又相互统一”的哲学观点的是
| A.小苏打溶液中存在电离和水解平衡 |
B.若硫化氢和浓硫酸反应后的含硫产物只有 , , 既是氧化产物,又是还原产物 既是氧化产物,又是还原产物 |
| C.电解饱和食盐水时阴极和阳极反应同时发生 |
D. 、 、 、 、 的氧化性随着卤素原子序数的增大而减弱 的氧化性随着卤素原子序数的增大而减弱 |
您最近一年使用:0次
2024-05-18更新
|
160次组卷
|
3卷引用:2024届河北省邯郸市高三下学期第四次调研检测化学试卷
单选题
|
适中(0.65)
解题方法
5. 下列物质性质和原理分析相匹配的是
| 选项 | 物质性质 | 原理分析 |
| A | 冰醋酸不导电,醋酸溶液能导电 | 冰醋酸中没有能自由移动的离子 醋酸溶液中有能自由移动的离子 |
| B |  的酸性比 的酸性比 的强 的强 |  的摩尔质量小于 的摩尔质量小于 |
| C | 甲酸的沸点高于二甲醚 | 甲酸的范德华力大于二甲醚 |
| D | 油漆易溶于甲苯,不溶于水 | 甲苯是非极性溶剂,水是极性溶剂 油漆是极性大的物质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-05-13更新
|
293次组卷
|
3卷引用:河北省邢台市2024届高三下学期质量检测一模化学试题
单选题
|
适中(0.65)
6. 武汉大学某课题组通过铜/铬催化实现烃与醛合成醇,下列叙述错误的是
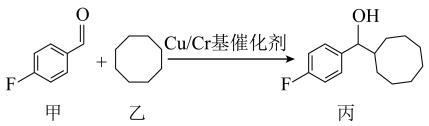
A.基态 、 、 原子中未成对电子数分别为4、1 原子中未成对电子数分别为4、1 |
| B.上述反应是加成反应,丙能发生消去反应 |
| C.丙分子含1个手性碳原子 |
D.甲、丙都能使酸性 溶液褪色 溶液褪色 |
您最近一年使用:0次
2024-05-14更新
|
264次组卷
|
2卷引用:2024届河北省邯郸市高三下学期第四次调研检测化学试卷
7. 短周期元素X、Y、Z、W的原子序数依次增大,X、W位于同主族但不相邻,基态Z原子价层电子排布式为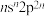 ,
, 是生活中常见的食品发泡剂。下列叙述正确的是
是生活中常见的食品发泡剂。下列叙述正确的是
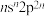 ,
, 是生活中常见的食品发泡剂。下列叙述正确的是
是生活中常见的食品发泡剂。下列叙述正确的是A.电负性: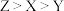 | B.第一电离能: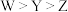 |
C.最简单氢化物的键角: | D.熔点: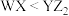 |
您最近一年使用:0次
2024-05-13更新
|
126次组卷
|
2卷引用:2024届河北省邯郸市高三下学期第四次调研检测化学试卷
单选题
|
适中(0.65)
解题方法
8. 水热法制备 的流程如图,下列叙述正确的是
的流程如图,下列叙述正确的是
 的流程如图,下列叙述正确的是
的流程如图,下列叙述正确的是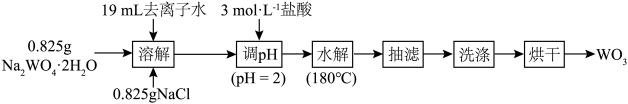
| A.本实验使用托盘天平称量 | B. 作反应的氧化剂 作反应的氧化剂 |
C.调 为2的目的是促进反应完全 为2的目的是促进反应完全 | D.用 溶液检验产品是否洗净 溶液检验产品是否洗净 |
您最近一年使用:0次
单选题
|
较易(0.85)
解题方法
9. 下列实验操作正确或操作规范且能达到实验目的的是
| 选项 | 操作 | 目的 |
| A | 取适量 晶体溶于浓硝酸中,加水稀释到指定刻度 晶体溶于浓硝酸中,加水稀释到指定刻度 | 配制一定物质的量浓度的溶液 |
| B | 用碱式滴定管盛装标准 溶液并滴定草酸溶液 溶液并滴定草酸溶液 | 测定草酸溶液浓度 |
| C | 向 的酒精中加入钠粒 的酒精中加入钠粒 | 证明 的酒精中含水 的酒精中含水 |
| D | 向 溶液中先滴加少量 溶液中先滴加少量  溶液 溶液振荡后再滴加少量  溶液 溶液 | 明: |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-05-14更新
|
354次组卷
|
4卷引用:河北省邢台市2024届高三下学期质量检测一模化学试题
单选题
|
适中(0.65)
10. 硫代硫酸钠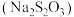 主要用于照相时作定影剂,也可用作氰化物的解毒剂,下列离子方程式书写错误的是
主要用于照相时作定影剂,也可用作氰化物的解毒剂,下列离子方程式书写错误的是
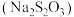 主要用于照相时作定影剂,也可用作氰化物的解毒剂,下列离子方程式书写错误的是
主要用于照相时作定影剂,也可用作氰化物的解毒剂,下列离子方程式书写错误的是A.用过量的 溶液除去底片上的 溶液除去底片上的 时有 时有 生成: 生成: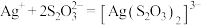 |
B.久置空气中的 溶液变质: 溶液变质: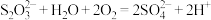 |
C.用 溶液吸收工业尾气中足量的 溶液吸收工业尾气中足量的 : : |
D.向 溶液中滴加稀硫酸: 溶液中滴加稀硫酸: |
【知识点】 离子方程式的正误判断解读
您最近一年使用:0次
2024-04-21更新
|
530次组卷
|
5卷引用:河北省邢台市2024届高三下学期质量检测一模化学试题
单选题
|
适中(0.65)
解题方法
11.  的回收和利用是实现“碳中和”的有效途径。在一恒容密闭反应器中充入体积之比为
的回收和利用是实现“碳中和”的有效途径。在一恒容密闭反应器中充入体积之比为 的
的 和
和 ,发生反应:①
,发生反应:①
 ,②
,②
 。在相同时间内,
。在相同时间内, 的转化率、
的转化率、 的选择性[
的选择性[ 的选择性
的选择性 ]与温度的关系如图所示。下列叙述错误的是
]与温度的关系如图所示。下列叙述错误的是
 的回收和利用是实现“碳中和”的有效途径。在一恒容密闭反应器中充入体积之比为
的回收和利用是实现“碳中和”的有效途径。在一恒容密闭反应器中充入体积之比为 的
的 和
和 ,发生反应:①
,发生反应:①
 ,②
,②
 。在相同时间内,
。在相同时间内, 的转化率、
的转化率、 的选择性[
的选择性[ 的选择性
的选择性 ]与温度的关系如图所示。下列叙述错误的是
]与温度的关系如图所示。下列叙述错误的是
A.温度高于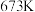 时,主要发生反应② 时,主要发生反应② |
B.温度低于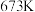 时, 时, 的选择性随温度升高而增大 的选择性随温度升高而增大 |
C.平衡时,再充入 和 和 ,再次达到平衡时, ,再次达到平衡时, 的物质的量增大 的物质的量增大 |
D.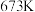 下反应达到平衡时, 下反应达到平衡时, 、 、 、 、 的浓度之比为 的浓度之比为 |
您最近一年使用:0次
2024-05-14更新
|
436次组卷
|
5卷引用:河北省邢台市2024届高三下学期质量检测一模化学试题
单选题
|
适中(0.65)
解题方法
12. 香港城市大学、中国科学院深圳先进技术研究院和深圳大学合作,证明了 纳米片在酸性条件下具有本征差的析氢活性,展现出快速选择性地将硝酸根离子还原为氨的催化性能。下列有关装置放电过程(如图所示)的叙述错误的是
纳米片在酸性条件下具有本征差的析氢活性,展现出快速选择性地将硝酸根离子还原为氨的催化性能。下列有关装置放电过程(如图所示)的叙述错误的是
 纳米片在酸性条件下具有本征差的析氢活性,展现出快速选择性地将硝酸根离子还原为氨的催化性能。下列有关装置放电过程(如图所示)的叙述错误的是
纳米片在酸性条件下具有本征差的析氢活性,展现出快速选择性地将硝酸根离子还原为氨的催化性能。下列有关装置放电过程(如图所示)的叙述错误的是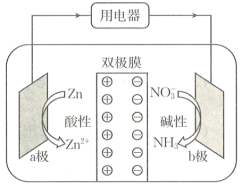
| A.电子由a极经用电器流向b极 |
| B.a极为负极,b极发生还原反应 |
C.b极上的电极反应式为 |
D.a极质量减少2.60g时,b极区有0.09  向双极膜迁移 向双极膜迁移 |
您最近一年使用:0次
单选题
|
适中(0.65)
13.  常用于制备磁芯、磁盘和传感器等,它的晶胞(结构如图)为等轴晶系。下列叙述错误的是
常用于制备磁芯、磁盘和传感器等,它的晶胞(结构如图)为等轴晶系。下列叙述错误的是
已知:晶胞参数为a ,
, 为阿伏加德罗常数的值。
为阿伏加德罗常数的值。
 常用于制备磁芯、磁盘和传感器等,它的晶胞(结构如图)为等轴晶系。下列叙述错误的是
常用于制备磁芯、磁盘和传感器等,它的晶胞(结构如图)为等轴晶系。下列叙述错误的是已知:晶胞参数为a
 ,
, 为阿伏加德罗常数的值。
为阿伏加德罗常数的值。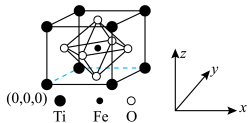
A. 的分数坐标为 的分数坐标为 | B.氧离子构成正八面体形 |
C. 和 和 之间的距离为 之间的距离为 | D. 晶体密度为 晶体密度为 |
您最近一年使用:0次
2024-05-14更新
|
134次组卷
|
2卷引用:2024届河北省邯郸市高三下学期第四次调研检测化学试卷
单选题
|
适中(0.65)
14. 常温下,向浓度相等的甲酸( )和醋酸(
)和醋酸( )的混合溶液中滴加氨水,溶液中
)的混合溶液中滴加氨水,溶液中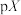 [
[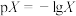 ,
, 、
、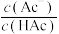 、
、 ]与
]与 的关系如图所示。下列叙述错误的是
的关系如图所示。下列叙述错误的是
 )和醋酸(
)和醋酸( )的混合溶液中滴加氨水,溶液中
)的混合溶液中滴加氨水,溶液中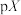 [
[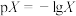 ,
, 、
、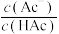 、
、 ]与
]与 的关系如图所示。下列叙述错误的是
的关系如图所示。下列叙述错误的是
A. 代表 代表 与 与 的变化关系 的变化关系 |
B.常温下, |
C.向 溶液中滴加氨水至Q点: 溶液中滴加氨水至Q点: |
D.上述反应中,最先生成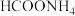 和 和 |
您最近一年使用:0次
2024-05-14更新
|
124次组卷
|
2卷引用:2024届河北省邯郸市高三下学期第四次调研检测化学试卷
二、解答题 添加题型下试题
解答题-工业流程题
|
适中(0.65)
15. 铬酸铅( )又称铬黄,是一种重要的黄色颜料,常用作橡胶、水彩、色纸的着色剂。以含铅废渣(主要成分是
)又称铬黄,是一种重要的黄色颜料,常用作橡胶、水彩、色纸的着色剂。以含铅废渣(主要成分是 和
和 ,还含
,还含 ,
, 等)为原料制备铬酸铅的流程如下:
等)为原料制备铬酸铅的流程如下: 不溶于硝酸。
不溶于硝酸。
②常温下,几种难溶电解质的溶度积如下:
回答下列问题:
(1)铅位于周期表第_________ 周期_________ 族,基态铅原子最高能级上电子云轮廓图为_________ 形。
(2)“碱浸”中 转化反应的离子方程式为
转化反应的离子方程式为_________ 。
(3)已知:“酸浸”中6.3g 作氧化剂时转移0.3
作氧化剂时转移0.3 电子。气体R在空气中的颜色变化为
电子。气体R在空气中的颜色变化为_________ 。
(4)“酸浸”中铅元素浸出率与温度、硝酸浓度的关系如图所示。“酸浸”最佳条件为______________ 。 ,“除铁”中控制
,“除铁”中控制 范围为
范围为____________ ,
 ,则表明
,则表明 已完全沉淀。
已完全沉淀。
(6)“沉铬”中生成 反应的离子方程式为
反应的离子方程式为____________ 。
 )又称铬黄,是一种重要的黄色颜料,常用作橡胶、水彩、色纸的着色剂。以含铅废渣(主要成分是
)又称铬黄,是一种重要的黄色颜料,常用作橡胶、水彩、色纸的着色剂。以含铅废渣(主要成分是 和
和 ,还含
,还含 ,
, 等)为原料制备铬酸铅的流程如下:
等)为原料制备铬酸铅的流程如下:
 不溶于硝酸。
不溶于硝酸。②常温下,几种难溶电解质的溶度积如下:
电解质 |
|
|
|
|
|
|
|
|
|
|
|
(1)铅位于周期表第
(2)“碱浸”中
 转化反应的离子方程式为
转化反应的离子方程式为(3)已知:“酸浸”中6.3g
 作氧化剂时转移0.3
作氧化剂时转移0.3 电子。气体R在空气中的颜色变化为
电子。气体R在空气中的颜色变化为(4)“酸浸”中铅元素浸出率与温度、硝酸浓度的关系如图所示。“酸浸”最佳条件为

 ,“除铁”中控制
,“除铁”中控制 范围为
范围为
 ,则表明
,则表明 已完全沉淀。
已完全沉淀。(6)“沉铬”中生成
 反应的离子方程式为
反应的离子方程式为
您最近一年使用:0次
2024-05-14更新
|
163次组卷
|
2卷引用:2024届河北省邯郸市高三下学期第四次调研检测化学试卷
解答题-实验探究题
|
较难(0.4)
16. 硫酸四氨合锌[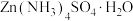 ]是一种重要的试剂,在工业上有重要的应用。某小组在实验室制备硫酸四氨合锌的步骤如下:
]是一种重要的试剂,在工业上有重要的应用。某小组在实验室制备硫酸四氨合锌的步骤如下:
在仪器X内加入1.5g 、2.5g尿素(
、2.5g尿素(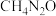 ,过量)和5.0
,过量)和5.0 乙二醇(
乙二醇( )及适量蒸馏水,油浴加热,控制温度在120℃以下回流。加热时溶液澄清,继续反应半小时有固温度计体析出,再反应半小时,冷却,抽滤,用无水乙醇洗涤沉淀数次,在95℃下烘干产品。回答下列问题:
)及适量蒸馏水,油浴加热,控制温度在120℃以下回流。加热时溶液澄清,继续反应半小时有固温度计体析出,再反应半小时,冷却,抽滤,用无水乙醇洗涤沉淀数次,在95℃下烘干产品。回答下列问题:_________ ;尿素易溶于水的原因是_______________ 。
(2)仪器X的名称是_________ ;冷凝管中进水口是_________ (填“a”或“b”)。
(3)尿素与水反应的化学方程式为_________ ;乙二醇的作用是_________ 。
(4)加热“回流”时温度不宜高于120℃,其原因是_________ 。
(5)烘干产品时宜选择的加热方式为_________ (填标号)。
a.酒精灯直接加热 b.沙浴 c.水浴加热
(6)用乙醇洗涤产品,而不用水洗涤,利用了乙醇的性质是_________ 。
(7)若最终得到1.976g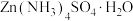 ,则产率为
,则产率为_________ (保留3位有效数字)。
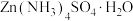 ]是一种重要的试剂,在工业上有重要的应用。某小组在实验室制备硫酸四氨合锌的步骤如下:
]是一种重要的试剂,在工业上有重要的应用。某小组在实验室制备硫酸四氨合锌的步骤如下:在仪器X内加入1.5g
 、2.5g尿素(
、2.5g尿素(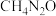 ,过量)和5.0
,过量)和5.0 乙二醇(
乙二醇( )及适量蒸馏水,油浴加热,控制温度在120℃以下回流。加热时溶液澄清,继续反应半小时有固温度计体析出,再反应半小时,冷却,抽滤,用无水乙醇洗涤沉淀数次,在95℃下烘干产品。回答下列问题:
)及适量蒸馏水,油浴加热,控制温度在120℃以下回流。加热时溶液澄清,继续反应半小时有固温度计体析出,再反应半小时,冷却,抽滤,用无水乙醇洗涤沉淀数次,在95℃下烘干产品。回答下列问题: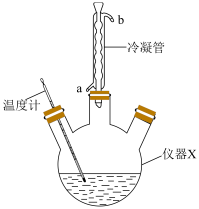
(2)仪器X的名称是
(3)尿素与水反应的化学方程式为
(4)加热“回流”时温度不宜高于120℃,其原因是
(5)烘干产品时宜选择的加热方式为
a.酒精灯直接加热 b.沙浴 c.水浴加热
(6)用乙醇洗涤产品,而不用水洗涤,利用了乙醇的性质是
(7)若最终得到1.976g
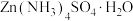 ,则产率为
,则产率为
您最近一年使用:0次
解答题-原理综合题
|
适中(0.65)
解题方法
17. 我国科学家开发出了高效催化剂ZnZrOx,实现CO2催化还原合成乙烯和丙烯,反应原理如下:
Ⅰ.
 ;
;
Ⅱ.
 。
。
回答下列问题:
(1)在周期表中, 和
和 相邻,二者中第二电离能与第一电离能之差较大的是
相邻,二者中第二电离能与第一电离能之差较大的是_________ (填“ ”或“
”或“ ”)。
”)。
(2)已知几种可燃物的燃烧热如下:

 。则
。则
_________  。
。
(3)在密闭容器中充入适量CO2和H2,发生上述反应。CO2的平衡转化率与温度、投料比 的关系如图所示。代表CO2平衡转化率与投料比关系的曲线是
的关系如图所示。代表CO2平衡转化率与投料比关系的曲线是______ (填“①”或“②”),判断的依据是_________ 。 CO2和5
CO2和5 H2,同时发生反应Ⅰ和反应Ⅱ,测得单位时间内CO2的转化率与催化剂Cat1,Cat2及温度的关系如图所示。
H2,同时发生反应Ⅰ和反应Ⅱ,测得单位时间内CO2的转化率与催化剂Cat1,Cat2及温度的关系如图所示。_________ (填“Cat1”或“Cat2”);b点_________ (填“达到”或“未达到”)平衡状态,判断依据是_________ 。
②Cat1作用下,温度高于400℃时,b→c过程中CO2转化率降低,可能的原因是_________ 。
③400℃时,CO2转化率为75%,此时容器中H2O的物质的量为_________  。
。
(5)T℃时,在1L恒容密闭容器中充入1.0 CO2和2.5
CO2和2.5 H2,同时发生反应Ⅰ和反应Ⅱ,达到平衡时CO2转化率为50%,乙烯的选择性为50%,在该条件下反应Ⅰ的平衡常数
H2,同时发生反应Ⅰ和反应Ⅱ,达到平衡时CO2转化率为50%,乙烯的选择性为50%,在该条件下反应Ⅰ的平衡常数
_________  。提示:乙烯的选择性
。提示:乙烯的选择性 。
。
Ⅰ.

 ;
;Ⅱ.

 。
。回答下列问题:
(1)在周期表中,
 和
和 相邻,二者中第二电离能与第一电离能之差较大的是
相邻,二者中第二电离能与第一电离能之差较大的是 ”或“
”或“ ”)。
”)。(2)已知几种可燃物的燃烧热如下:
物质 |
|
|
|
燃烧热 | -285.8 | -1411.0 | -2058.0 |

 。则
。则
 。
。(3)在密闭容器中充入适量CO2和H2,发生上述反应。CO2的平衡转化率与温度、投料比
 的关系如图所示。代表CO2平衡转化率与投料比关系的曲线是
的关系如图所示。代表CO2平衡转化率与投料比关系的曲线是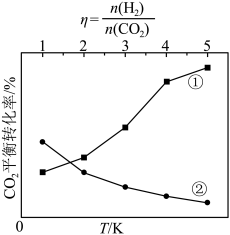
 CO2和5
CO2和5 H2,同时发生反应Ⅰ和反应Ⅱ,测得单位时间内CO2的转化率与催化剂Cat1,Cat2及温度的关系如图所示。
H2,同时发生反应Ⅰ和反应Ⅱ,测得单位时间内CO2的转化率与催化剂Cat1,Cat2及温度的关系如图所示。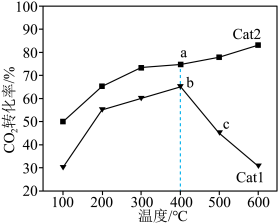
②Cat1作用下,温度高于400℃时,b→c过程中CO2转化率降低,可能的原因是
③400℃时,CO2转化率为75%,此时容器中H2O的物质的量为
 。
。(5)T℃时,在1L恒容密闭容器中充入1.0
 CO2和2.5
CO2和2.5 H2,同时发生反应Ⅰ和反应Ⅱ,达到平衡时CO2转化率为50%,乙烯的选择性为50%,在该条件下反应Ⅰ的平衡常数
H2,同时发生反应Ⅰ和反应Ⅱ,达到平衡时CO2转化率为50%,乙烯的选择性为50%,在该条件下反应Ⅰ的平衡常数
 。提示:乙烯的选择性
。提示:乙烯的选择性 。
。
您最近一年使用:0次
解答题-有机推断题
|
较难(0.4)
18.  是合成某药物的中间体,一种合成
是合成某药物的中间体,一种合成 的流程如下(
的流程如下(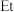 为乙基,
为乙基, 为苯基),回答下列问题:
为苯基),回答下列问题:_____ 。
(2)有机物中N原子电子云密度越大,碱性越强。下列有机物碱性由弱到强排序为_____ (填标号)。_____ ,H中含氧官能团是_____ (填名称)。
(4)A→B的反应类型是_____ ,有机物y的作用是_____ 。
(5)写出E→F的化学方程式:_____ 。
(6)在C的同分异构体中,同时满足下列条件的结构简式为_____ (写一种)。
①能发生银镜反应;②1mol有机物最多能消耗2molNaOH;③在核磁共振氢谱上峰的面积比为1∶2∶6.
(7)一种重要的有机物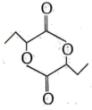 的合成路线如下图(反应条件已略去),其中
的合成路线如下图(反应条件已略去),其中 和
和 的结构简式分别为
的结构简式分别为_____ 和_____ 。
 是合成某药物的中间体,一种合成
是合成某药物的中间体,一种合成 的流程如下(
的流程如下(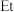 为乙基,
为乙基, 为苯基),回答下列问题:
为苯基),回答下列问题: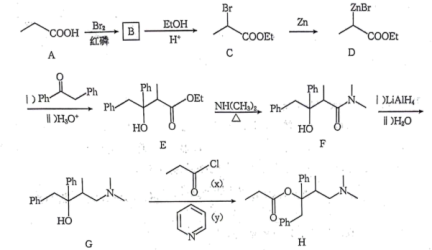
(2)有机物中N原子电子云密度越大,碱性越强。下列有机物碱性由弱到强排序为
a.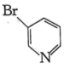 b.
b. c.
c. d.
d.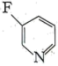
(4)A→B的反应类型是
(5)写出E→F的化学方程式:
(6)在C的同分异构体中,同时满足下列条件的结构简式为
①能发生银镜反应;②1mol有机物最多能消耗2molNaOH;③在核磁共振氢谱上峰的面积比为1∶2∶6.
(7)一种重要的有机物
 的合成路线如下图(反应条件已略去),其中
的合成路线如下图(反应条件已略去),其中 和
和 的结构简式分别为
的结构简式分别为
您最近一年使用:0次
2024-05-12更新
|
181次组卷
|
2卷引用:河北省邢台市2024届高三下学期质量检测一模化学试题
试卷分析
整体难度:适中
考查范围:常见无机物及其应用、化学反应原理、认识化学科学、物质结构与性质、有机化学基础、化学实验基础
试卷题型(共 18题)
题型
数量
单选题
14
解答题
4
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 硅酸盐 金属的化学腐蚀与电化学腐蚀 吸氧腐蚀 | |
| 2 | 0.65 | 共价化合物的结构及形成过程 电子式的书写与判断 电子排布式 利用杂化轨道理论判断分子的空间构型 | |
| 3 | 0.85 | 有机物重结晶 | |
| 4 | 0.65 | 氧化还原反应的几组概念 盐类水解在解题方面的应用 电解原理的理解及判断 | |
| 5 | 0.65 | 非电解质、电解质物质类别判断 极性分子和非极性分子 氢键对物质性质的影响 | |
| 6 | 0.65 | 分子的手性 醇的消去反应 醛类与强氧化剂反应 电子排布式 | |
| 7 | 0.65 | 根据原子结构进行元素种类推断 电离能 元素性质与电负性的关系 分子的性质 | |
| 8 | 0.65 | 氧化还原反应定义、本质及特征 浓度对化学平衡移动的影响 常用仪器及使用 常见阴离子的检验 | |
| 9 | 0.85 | 硝酸的强氧化性 酸碱中和滴定实验相关仪器 沉淀转化 乙醇与钠反应 | |
| 10 | 0.65 | 离子方程式的正误判断 | |
| 11 | 0.65 | 化学平衡的移动及其影响因素 化学平衡图像分析 温度对化学平衡移动的影响 转化率的相关计算及判断 | |
| 12 | 0.65 | 原电池电子流向判断及应用 原电池正负极判断 原电池电极反应式书写 原电池有关计算 | |
| 13 | 0.65 | 晶胞概念及判断 根据晶胞结构确定晶体化学式 晶胞的有关计算 | |
| 14 | 0.65 | 电离平衡常数及影响因素 盐溶液中离子浓度大小的比较 弱电解质的电离平衡常数 | |
| 二、解答题 | |||
| 15 | 0.65 | 硝酸的强氧化性 溶度积常数相关计算 配合物的应用 其他金属及其化合物 | 工业流程题 |
| 16 | 0.4 | 轨道表示式 物质分离、提纯综合应用 物质制备的探究 综合实验设计与评价 | 实验探究题 |
| 17 | 0.65 | 盖斯定律与热化学方程式 化学平衡的移动及其影响因素 化学平衡状态的判断方法 化学平衡常数的有关计算 | 原理综合题 |
| 18 | 0.4 | 根据要求书写同分异构体 合成过程中羟基引入方法 多官能团有机物的结构与性质 有机推断综合考查 | 有机推断题 |