河南省许昌市第三中学2020-2021学年高一上学期质量检测化学试题
河南
高一
阶段练习
2020-11-03
208次
整体难度:
适中
考查范围:
认识化学科学、常见无机物及其应用、化学实验基础、化学反应原理、物质结构与性质、有机化学基础
一、单选题 添加题型下试题
A.使酚酞溶液变红的溶液:H+、Cl-、 、Ba2+ 、Ba2+ |
B.澄清透明的溶液: 、Al3+、 、Al3+、 、K+ 、K+ |
C.强碱性溶液:K+、Mg2+、 、 、 |
D.无色的溶液: 、 、 、Cu2+、 、Cu2+、 |
【知识点】 离子共存 限定条件下的离子共存解读
| A.分散质粒子半径介于1nm~100nm之间的分散系称为胶体 |
| B.胶体粒子很小,可以稳定存在的原因是胶粒的布朗运动 |
| C.容量瓶用蒸馏水洗涤后残留有少量的水,将导致配制结果不变 |
D.检验某溶液是否含有 时,应取少量该溶液,依次加入BaCl2溶液和稀盐酸 时,应取少量该溶液,依次加入BaCl2溶液和稀盐酸 |
A.铜片上有气泡产生,锌片逐渐溶解 | B.电子在溶液中从Cu电极流向Zn电极 |
| C.把铜片换成石墨,实验现象相同 | D.把稀硫酸换成硫酸铜溶液,电流计指针依然偏转 |
【知识点】 原电池 原电池电子流向判断及应用解读
| A.①②③④ | B.②③④ | C.③④ | D.②③ |
【知识点】 元素周期表的应用
| A.10Q | B.10Q~5Q | C.大于10Q | D.5Q |
【知识点】 化学反应热的计算
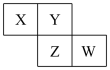
| A.原子半径:W>Z>Y>X |
| B.最高价氧化物对应水化物的酸性W比Z弱 |
| C.Y的气态氢化物的稳定性较Z的弱 |
| D.四种元素的单质中,Z的熔、沸点最高 |
| A.向 FeCl3溶液中滴加氨水:Fe3++3OH-=Fe(OH)3↓ |
| B.磁性氧化铁溶于足量稀硝酸:Fe3O4+8H+=Fe2++2Fe3++4H2O |
| C.用过量氨水吸收工业尾气中的 SO2:2NH3·H2O + SO2 =2NH4++ SO32-+ H2O |
| D.将铝片加入烧碱溶液中:2Al + 2OH- = 2AlO2-+ H2↑ |
| A.因是同一反应,所以用不同物质表示化学反应速率时,所得数值是相同的 |
| B.根据化学反应速率的大小可以知道化学反应进行的快慢 |
| C.化学反应速率为“1mol/(L•min)”表示的意思是:时间为1min时,某物质的浓度为1mol/L |
| D.化学反应速率是指一定时间内任何一种反应物浓度的减少或者任何一种生成物浓度的增加 |
| A.Na→NaOH→Na2CO3 | B.Fe→Fe(NO3)3→Fe(OH)3 |
| C.A1→A12O3→A1(OH)3 | D.Mg→MgCl2→Mg(OH)2 |
| 物质 | 杂质 | 除杂质所用试剂和方法 | |
| A | KCl溶液 | I2 | CCl4,萃取分液 |
| B | CO2 | HCl | 饱和NaHCO3溶液,洗气 |
| C | Mg粉 | Al粉 | NaOH溶液,过滤 |
| D | CaCO3 | CaO | 盐酸,过滤 |
| A.A | B.B | C.C | D.D |
【知识点】 物质分离、提纯的常见化学方法解读
| A.2H2S+SO2=3S+2H2O中,氧化产物和还原产物物质的量之比为2:1 |
| B.4Zn+10HNO3=4Zn(NO3)2+NH4NO3+3H2O中,氧化剂和还原剂物质的量之比为5:2 |
C.3I2+6KOH 5KI+KIO3+3H2O中,被氧化和被还原的碘元素物质的量之比为1:5 5KI+KIO3+3H2O中,被氧化和被还原的碘元素物质的量之比为1:5 |
D.2FeS+6H2SO4(浓) Fe2(SO4)3+3SO2+2S↓+6H2O中,反应中发生氧化反应和发生还原反应的硫元素物质的量之比为2:3 Fe2(SO4)3+3SO2+2S↓+6H2O中,反应中发生氧化反应和发生还原反应的硫元素物质的量之比为2:3 |
【知识点】 氧化还原反应的几组概念解读 与氧化剂、还原剂有关的计算解读
A.Na+、K+、Cu2+、SO | B.NH 、Na+、NO 、Na+、NO 、Cl- 、Cl- |
C.K+、Ca2+、HCO 、Cl- 、Cl- | D.Mg2+、Fe3+、Cl-、OH- |
【知识点】 离子反应的发生条件解读 离子共存 限定条件下的离子共存解读
a | ||
b | ||
c |
| A.a是一种活泼的非金属元素 |
| B.b的氢化物很稳定 |
| C.c的最高价氧化物的水化物是一种弱酸 |
| D.b元素的最高化合物为+7价。 |
| A.CaCl2 | B.KOH | C.H2O | D.N2 |
【知识点】 化学键与物质类别关系的判断解读
| A.CO2 H2S | B.C2H4 CH4 |
| C.C60 C2H4 | D.NH3 HCl |
【知识点】 共价键概念及判断解读 极性分子和非极性分子解读
| A.I2、Br2、Cl2、F2 | B.F2、Cl2、Br2、I2 | C.F-、Cl-、Br-、I- | D.Li、Na、K、Rb |
【知识点】 同主族元素性质递变规律
| A.人体最主要的供能物质是维生素 |
| B.淀粉和纤维素是天然高分子化合物 |
| C.蛋白质溶液中加入饱和(NH4)2SO4溶液,蛋白质析出,再加水会溶解 |
| D.葡萄糖作为营养剂供给人体能量,在体内发生主要的反应是氧化反应 |

| A.CuS | B.FeS | C.NO2 | D.FeCl2 |
【知识点】 无机综合推断 碳酸钠与碳酸氢钠的相互转化解读 铁的其他化合物
| A.NO2 | B.NO | C.CO2 | D.Cl2 |
【知识点】 二氧化氮 一氧化氮的化学性质解读 常见气体的制备与收集解读
 的过程中,下列操作正确的是(提示:稀硝酸具有强氧化性,可将
的过程中,下列操作正确的是(提示:稀硝酸具有强氧化性,可将 氧化为
氧化为 )
)A.先加入稀硝酸,没有产生沉淀,然后再加硝酸钡,产生白色沉淀,证明有 存在 存在 |
B.先加入硝酸钡,产生白色沉淀,然后再加稀硝酸,沉淀不溶解,证明有 存在 存在 |
C.先加入稀盐酸,没有产生沉淀,然后再加氯化钡,产生白色沉淀,证明有 存在 存在 |
D.先加入氯化钡,产生白色沉淀,然后再加稀盐酸,沉淀不溶解,证明有 存在 存在 |
二、计算题 添加题型下试题

①步骤Ⅰ为白磷的工业生产方法之一,反应在1300℃的高温炉中进行,其中SiO2的作用是用于造渣(CaSiO3),焦炭的作用是
②不慎将白磷沾到皮肤上,可用0.2mol/LCuSO4溶液冲洗,根据步骤Ⅱ可判断,1mol/LCuSO4溶液所能氧化的白磷的物质的量为
①所含分子数目之比为
②所含O原子数目之比为
③相同条件下的体积之比为
④相同条件下的密度之比为
【知识点】 阿伏加德罗定律的应用解读 物质的量有关计算
(1)Na2R的摩尔质量为
(2)R的相对原子质量为
(3)若Na2R中含R的质量为1.6 g,则Na2R的物质的量为
【知识点】 碳酸钠、碳酸氢钠混合物的有关求算解读
三、填空题 添加题型下试题
四、计算题 添加题型下试题
【知识点】 化学方程式计算中物质的量的运用解读
五、解答题 添加题型下试题
(1)配制时,除量筒、烧杯、玻璃棒外还需玻璃仪器有
(2)减小误差量取时需选用合适的量筒量取
(3)在容量瓶的使用方法中,下列操作不正确的是
A.使用容量瓶前检查它是否漏水
B.容量瓶用蒸馏水洗净后,再用待配溶液润洗
C.配制溶液时,如果试样是固体,把称好的试样用纸条小心倒入容量瓶中,缓慢加入蒸馏水到接近标线1~2cm处,改用胶头滴管加蒸馏水到标线
D.往容量瓶中转移溶液时应用玻璃棒引流
(4)在配制过程中,其他操作都是正确的,下列操作会引起误差偏高的是
①转移溶液时不慎有少量洒到容量瓶外面 ②没有洗涤烧杯和玻璃棒③定容时俯视刻度线④容量瓶不干燥,含有少量蒸馏水⑤定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线。⑥未冷却到室温就将溶液转移到容量瓶并定容
六、填空题 添加题型下试题
(1)其中属于电解质的是
(2)写出NaOH(aq)与Al反应的离子方程式:
(3)胶体是一种常见的分散系,回答下列问题。
①向Fe(OH)3胶体中加入Na2SO4饱和溶液,由于
②区分胶体和溶液常用的方法叫做
七、解答题 添加题型下试题
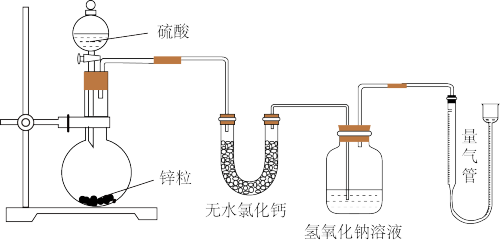
(1)若在烧瓶中放入1.30g锌粒,与cmol/LH2SO4反应,为保证实验结论的可靠,量气管的适宜规格是
A.200mL B.400mL C.500mL
(2)若1.30g锌粒完全溶解,测得盛氢氧化钠溶液的洗气瓶增重1.28g,则圆底烧瓶中发生反应的化学方程式为
(3)若烧瓶中投入ag锌且完全反应,氢氧化钠洗气瓶增重bg量气管中收集到VmL气体,其依据得失电子守恒的原理,可得出a、b、V之间的关系为:是
(4)若在烧瓶中投入dg锌,再加入VLcmol/L浓硫酸,充分反应后锌有剩余,测得盛氢氧化钠溶液的洗气瓶增重mg,则整个实验过程产生的混和气体中H2和SO2物质的量之比
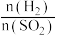 =
=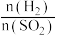 的比值将
的比值将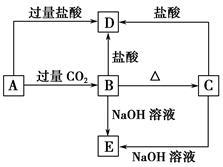
(1)写出化学式:A
(2)写出下列反应的离子方程式:
A→B:
A→D:
回答下列问题:
(1)X元素在元素周期表中的位置
(2)由Y和W形成的化合物的电子式
(3)YX2分子的结构式为
(4)前四种元素的简单氢化物中Z的沸点最高,原因是
(5)写出Q和W两种元素的最高价氧化物的水化物发生反应的离子方程式
试卷分析
试卷题型(共 33题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 离子共存 限定条件下的离子共存 | |
| 2 | 0.85 | 分散系概念 胶体 硫酸根离子的检验 配制一定物质的量浓度的溶液实验的误差分析 | |
| 3 | 0.65 | 原电池 原电池电子流向判断及应用 | |
| 4 | 0.85 | 元素周期表的应用 | |
| 5 | 0.65 | 化学反应热的计算 | |
| 6 | 0.65 | 元素周期表提供的元素信息 元素非金属性强弱的比较方法 微粒半径大小的比较方法 根据原子结构进行元素种类推断 | |
| 7 | 0.65 | 离子反应的发生条件 离子方程式的书写 离子方程式的正误判断 硝酸的强氧化性 | |
| 8 | 0.65 | 化学反应速率含义、单位 化学反应速率的定量表示方法 化学反应速率与化学计量数之间的关系 | |
| 9 | 0.65 | 钠 含镁化合物 氧化铝 铁与强氧化性酸的反应 | |
| 10 | 0.65 | 物质分离、提纯的常见化学方法 | |
| 11 | 0.65 | 氧化还原反应的几组概念 与氧化剂、还原剂有关的计算 | |
| 12 | 0.85 | 离子反应的发生条件 离子共存 限定条件下的离子共存 | |
| 13 | 0.85 | 元素周期律、元素周期表的推断 “定位法”在推断中的应用 “位构性”关系理解及应用 | |
| 14 | 0.85 | 化学键与物质类别关系的判断 | |
| 15 | 0.65 | 共价键概念及判断 极性分子和非极性分子 | |
| 16 | 0.85 | 同主族元素性质递变规律 | |
| 17 | 0.65 | 淀粉和纤维素 蛋白质 | |
| 18 | 0.65 | 无机综合推断 碳酸钠与碳酸氢钠的相互转化 铁的其他化合物 | |
| 19 | 0.65 | 二氧化氮 一氧化氮的化学性质 常见气体的制备与收集 | |
| 20 | 0.85 | 硫酸根离子的检验 | |
| 二、计算题 | |||
| 21 | 0.65 | 依据物质的量浓度公式的基础计算 物质的量浓度计算-与溶质成分有关的计算 电离方程式 | |
| 22 | 0.65 | 氧化还原反应的几组概念 与氧化剂、还原剂有关的计算 基于氧化还原反应守恒规律的计算 | |
| 23 | 0.85 | 阿伏加德罗定律的应用 物质的量有关计算 | |
| 24 | 0.85 | 摩尔质量 物质的量有关计算 | |
| 25 | 0.65 | 根据n=m/M进行相关计算 化学方程式计算中物质的量的运用 氧化钠的化学性质 过氧化钠与水的反应 | |
| 26 | 0.65 | 碳酸钠、碳酸氢钠混合物的有关求算 | |
| 28 | 0.65 | 化学方程式计算中物质的量的运用 | |
| 三、填空题 | |||
| 27 | 0.94 | 氯离子的检验 | |
| 30 | 0.65 | 胶体的性质和应用 电解质与非电解质 铝与强碱溶液反应 | |
| 四、解答题 | |||
| 29 | 0.85 | 配制一定物质的量浓度的溶液的步骤、操作 配制一定物质的量浓度的溶液实验的误差分析 配制一定物质的量浓度的溶液实验的仪器 配制一定物质的量浓度溶液的综合考查 | 实验探究题 |
| 31 | 0.4 | 化学方程式计算中物质的量的运用 酸的通性 浓硫酸的强氧化性 探究物质组成或测量物质的含量 | 实验探究题 |
| 32 | 0.65 | 焰色试验 氢氧化铝与强酸反应 铝三角转化 | 无机推断题 |
| 33 | 0.65 | 氢氧化铝与强酸反应 元素周期律、元素周期表的推断 “位构性”关系理解及应用 化学键与物质类别关系的判断 | 无机推断题 |



