某混合物的水溶液中,只可能含有以下离子中的若干种:K+、Mg2+、Fe3+、NH 、Cl-、CO
、Cl-、CO 和SO
和SO 。现每次取10.00mL进行实验:
。现每次取10.00mL进行实验:
查阅资料:OH-+NH
 NH3↑+H2O
NH3↑+H2O
①第一份加入AgNO3溶液有沉淀产生;
②第二份加入足量NaOH后加热,假设气体完全放出,收集到0.672L的气体(标准状况下)
③第三份加入足量BaCl2溶液后得干燥沉淀6.63g,沉淀经足量盐酸洗涤,干燥后剩余4.66g。
请回答:(1)一定存在的离子有___________ ,c(CO )=
)=_ mol/L。
(2)K+是否存在?___________ ;若存在,浓度范围是___________ (若不存在,则不必回答第2问)。
(3)根据以上实验,不能判断哪些离子是否存在?___________ 若存在这些离子,如何进行检验?___________ 。
(4)写出③中盐酸洗涤沉淀发生反应的离子方程式___________ 。
 、Cl-、CO
、Cl-、CO 和SO
和SO 。现每次取10.00mL进行实验:
。现每次取10.00mL进行实验:查阅资料:OH-+NH

 NH3↑+H2O
NH3↑+H2O①第一份加入AgNO3溶液有沉淀产生;
②第二份加入足量NaOH后加热,假设气体完全放出,收集到0.672L的气体(标准状况下)
③第三份加入足量BaCl2溶液后得干燥沉淀6.63g,沉淀经足量盐酸洗涤,干燥后剩余4.66g。
请回答:(1)一定存在的离子有
 )=
)=(2)K+是否存在?
(3)根据以上实验,不能判断哪些离子是否存在?
(4)写出③中盐酸洗涤沉淀发生反应的离子方程式
更新时间:2020-12-14 13:50:49
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】现有含有少量NaCl、Na2SO4、Na2CO3等杂质的NaNO3溶液,选择适当地试剂除去杂质,得到纯净的NaNO3固体,实验流程如图所示。
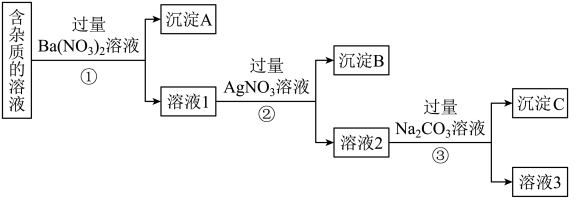
(1)沉淀A的主要成分是_______ 、________ (填化学式)。
(2)②中相关的离子方程式为________ ;③中加入过量的Na2CO3溶液的目的是_______ 。
(3)溶液3经过处理可以得到NaNO3固体,溶液3中肯定含有的杂质是_______ ,为了除去杂质,可向溶液3中加入适量的_______ 溶液。

(1)沉淀A的主要成分是
(2)②中相关的离子方程式为
(3)溶液3经过处理可以得到NaNO3固体,溶液3中肯定含有的杂质是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】Ⅰ.某无色溶液中可能含有Na+、Ba2+、Cu2+、CO 、Cl-、Mg2+中的一种或几种离子。
、Cl-、Mg2+中的一种或几种离子。
①向此溶液中滴加足量稀盐酸无明显现象。
②取少许①的溶液并加入少量的Na2SO4溶液,有白色沉淀产生。
③取②的上层清液并加入足量的NaOH溶液,有白色沉淀产生。
则原溶液中一定含有的离子是_______ ,一定不含有的离子是_______ 。
II.酸式盐是盐的一种,可看作是多元酸中的氢离子未被完全中和所得到的盐,常见的有NaHCO3、NaHSO4、KH2PO4、K2HPO4等。已知H3PO2(次磷酸)与足量的NaOH反应只生成一种盐NaH2PO2,H3PO2水溶液中存在H3PO2分子。
(1)H3PO2属于_______ 酸;NaH2PO2为_______ 盐(填序号)
①一元酸,②二元酸,③三元酸,④强酸,⑤弱酸,⑥正盐,⑦酸式盐
(2)写出H3PO2溶液与足量NaOH溶液反应的离子方程式_______ 。
 、Cl-、Mg2+中的一种或几种离子。
、Cl-、Mg2+中的一种或几种离子。①向此溶液中滴加足量稀盐酸无明显现象。
②取少许①的溶液并加入少量的Na2SO4溶液,有白色沉淀产生。
③取②的上层清液并加入足量的NaOH溶液,有白色沉淀产生。
则原溶液中一定含有的离子是
II.酸式盐是盐的一种,可看作是多元酸中的氢离子未被完全中和所得到的盐,常见的有NaHCO3、NaHSO4、KH2PO4、K2HPO4等。已知H3PO2(次磷酸)与足量的NaOH反应只生成一种盐NaH2PO2,H3PO2水溶液中存在H3PO2分子。
(1)H3PO2属于
①一元酸,②二元酸,③三元酸,④强酸,⑤弱酸,⑥正盐,⑦酸式盐
(2)写出H3PO2溶液与足量NaOH溶液反应的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】用如图所示Ⅰ和Ⅱ装置组合与Ⅰ和Ⅲ装置组合进行相关实验(夹持仪器略),回答下列问题:
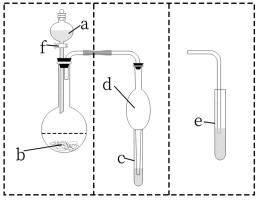
(1)若用Ⅰ和Ⅱ装置或Ⅰ和Ⅲ装置组合,实验前检查装置气密性的方法是___ 。
(2)在Ⅰ和Ⅱ装置组合中,若a为浓硫酸,b为铜粉,c容器中盛放品红溶液,旋开f后,给烧瓶加热,一段时间后c中的现象是___ ,写出烧瓶中发生反应的化学方程式___ 。
(3)在Ⅰ装置中,若a为浓氨水,b为生石灰,欲制取氨气并证明氨水有碱性,最好应选用___ (填“Ⅱ”或“Ⅲ”)装置与其组合,原因是___ 。
(4)在Ⅰ装置中,若a为可能含有Mg2+、Cu2+、Al3+、Fe3+四种阳离子的水溶液,b为过氧化钠固体,旋开f后,有白色沉淀产生并放出氧气,过氧化钠固体的物质的量与产生沉淀的质量关系如图,则a溶液中含有的阳离子有___ ,其阳离子的物质的量浓度之比为___ 。
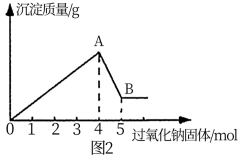
(5)在图中A→B段反应过程中溶液所增加的阴离子是___ 。

(1)若用Ⅰ和Ⅱ装置或Ⅰ和Ⅲ装置组合,实验前检查装置气密性的方法是
(2)在Ⅰ和Ⅱ装置组合中,若a为浓硫酸,b为铜粉,c容器中盛放品红溶液,旋开f后,给烧瓶加热,一段时间后c中的现象是
(3)在Ⅰ装置中,若a为浓氨水,b为生石灰,欲制取氨气并证明氨水有碱性,最好应选用
(4)在Ⅰ装置中,若a为可能含有Mg2+、Cu2+、Al3+、Fe3+四种阳离子的水溶液,b为过氧化钠固体,旋开f后,有白色沉淀产生并放出氧气,过氧化钠固体的物质的量与产生沉淀的质量关系如图,则a溶液中含有的阳离子有

(5)在图中A→B段反应过程中溶液所增加的阴离子是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】(I)新冠肺炎疫情期间,“84消毒液”被广泛应用于物体表面杀菌消毒。襄阳四中高一年级某学习小组的同学参阅“84消毒液”的配方,欲用NaClO固体配制480mL0.2mol/L的NaClO消毒液。回答下列问题:
(1)配制上述溶液需要的玻璃仪器有量简、烧杯、玻璃棒、____ 、____ 。
(2)需要用托盘天平称量NaClO固体的质量为_____ 。
(3)该小组的同学查阅资料得知:“84消毒液”与稀硫酸混合使用可增强消毒能力,于是他们准备用98%(密度为1.84g•cm-3)的浓硫酸配制250mL1.84mol•L-1的稀硫酸用于增强“84消毒液”的消毒能力。
①需用量简量取浓硫酸的体积为_____ mL。
②若所配制的稀硫酸浓度偏小,则下列可能的原因分析中正确的是_____ 。
A.配制前,容量瓶中有少量蒸馏水 B.量取浓硫酸时,仰视液体的凹液面
C.未冷却,立即转移至容量瓶定容 D.定容时,仰视溶液的凹液面
(II)有一份无色溶液,只可能有Na+、Cl-、H+、SO 、CO
、CO 、Cu2+、NO
、Cu2+、NO 中的几种(忽略水电离产生的少量的OH-)。取该溶液检测,发现溶液显强酸性。
中的几种(忽略水电离产生的少量的OH-)。取该溶液检测,发现溶液显强酸性。
(4)不需要进一步实验,可以判断,溶液中一定存在____ ,一定不存在____ 。
(5)进一步测定,取100mL该溶液,发现该溶液中n(H+)=0.01mol,加入足量BaCl2,生成2.33g沉淀,过滤,滤液中加入足量AgNO3溶液,产生5.74g沉淀。则该100mL溶液中Na+的物质的量浓度_____ (填“至少”或“至多”)为_____ 。
(1)配制上述溶液需要的玻璃仪器有量简、烧杯、玻璃棒、
(2)需要用托盘天平称量NaClO固体的质量为
(3)该小组的同学查阅资料得知:“84消毒液”与稀硫酸混合使用可增强消毒能力,于是他们准备用98%(密度为1.84g•cm-3)的浓硫酸配制250mL1.84mol•L-1的稀硫酸用于增强“84消毒液”的消毒能力。
①需用量简量取浓硫酸的体积为
②若所配制的稀硫酸浓度偏小,则下列可能的原因分析中正确的是
A.配制前,容量瓶中有少量蒸馏水 B.量取浓硫酸时,仰视液体的凹液面
C.未冷却,立即转移至容量瓶定容 D.定容时,仰视溶液的凹液面
(II)有一份无色溶液,只可能有Na+、Cl-、H+、SO
 、CO
、CO 、Cu2+、NO
、Cu2+、NO 中的几种(忽略水电离产生的少量的OH-)。取该溶液检测,发现溶液显强酸性。
中的几种(忽略水电离产生的少量的OH-)。取该溶液检测,发现溶液显强酸性。(4)不需要进一步实验,可以判断,溶液中一定存在
(5)进一步测定,取100mL该溶液,发现该溶液中n(H+)=0.01mol,加入足量BaCl2,生成2.33g沉淀,过滤,滤液中加入足量AgNO3溶液,产生5.74g沉淀。则该100mL溶液中Na+的物质的量浓度
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】某溶液中含有 、
、 、Cl三种阴离子,如果只取用一次该溶液(可以使用过滤操作),就能把三种离子依次检验出来:
、Cl三种阴离子,如果只取用一次该溶液(可以使用过滤操作),就能把三种离子依次检验出来:
(1)应该先检验_____ 离子,加入的试剂是稀硝酸,反应的离子方程式为:_____________ ;
(2)再检验_____ 离子,加入的试剂是_________ ,反应的离子方程式为:__________________ ;
(3)最后检验_____ 离子,加入的试剂是_________ ,反应的离子方程式为:________________ 。
 、
、 、Cl三种阴离子,如果只取用一次该溶液(可以使用过滤操作),就能把三种离子依次检验出来:
、Cl三种阴离子,如果只取用一次该溶液(可以使用过滤操作),就能把三种离子依次检验出来: (1)应该先检验
(2)再检验
(3)最后检验
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】某溶液只含Cl 、CO
、CO 、SO
、SO 、Na
、Na 、K
、K 、Mg
、Mg 六种离子中的某几种。经实验:
六种离子中的某几种。经实验:
①原溶液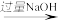 白色沉淀;
白色沉淀;
②原溶液中加BaCl2溶液不产生沉淀;
③原溶液中加AgNO3溶液产生白色沉淀,再加稀硝酸白色沉淀不溶解。回答下列问题:
(1)试分析原溶液中一定含有的离子是______________ ,一定不含有的离子是_______ ,可能含有的离子是______________ 。
(2)有的同学认为实验③可以省略,你认为是否正确(填“是”或“否”)_________ ,说明理由_________________________________________________________ 。
 、CO
、CO 、SO
、SO 、Na
、Na 、K
、K 、Mg
、Mg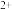 六种离子中的某几种。经实验:
六种离子中的某几种。经实验:①原溶液
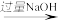 白色沉淀;
白色沉淀;②原溶液中加BaCl2溶液不产生沉淀;
③原溶液中加AgNO3溶液产生白色沉淀,再加稀硝酸白色沉淀不溶解。回答下列问题:
(1)试分析原溶液中一定含有的离子是
(2)有的同学认为实验③可以省略,你认为是否正确(填“是”或“否”)
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】某溶液只含Cl 、CO
、CO 、SO
、SO 、Na
、Na 、K
、K 、Mg
、Mg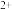 六种离子中的某几种。经实验:
六种离子中的某几种。经实验:
①原溶液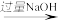 白色沉淀;
白色沉淀;
②原溶液中加BaCl2溶液不产生沉淀;
③原溶液中加AgNO3溶液产生白色沉淀,再加稀硝酸白色沉淀不溶解。回答下列问题:
(1)试分析原溶液中一定含有的离子是______________ ,一定不含有的离子是_______ ,可能含有的离子是______________ 。
(2)有的同学认为实验③可以省略,你认为是否正确(填“是”或“否”)_________ ,说明理由_________________________________________________________ 。
 、CO
、CO 、SO
、SO 、Na
、Na 、K
、K 、Mg
、Mg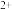 六种离子中的某几种。经实验:
六种离子中的某几种。经实验:①原溶液
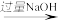 白色沉淀;
白色沉淀;②原溶液中加BaCl2溶液不产生沉淀;
③原溶液中加AgNO3溶液产生白色沉淀,再加稀硝酸白色沉淀不溶解。回答下列问题:
(1)试分析原溶液中一定含有的离子是
(2)有的同学认为实验③可以省略,你认为是否正确(填“是”或“否”)
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】某强酸性稀溶液中可能存在Al3+、Fe2+、 、Ba2+、Cl﹣、
、Ba2+、Cl﹣、 、
、 、SiO
、SiO 、
、 中的若干种,现取适量该溶液进行如下实验。
中的若干种,现取适量该溶液进行如下实验。
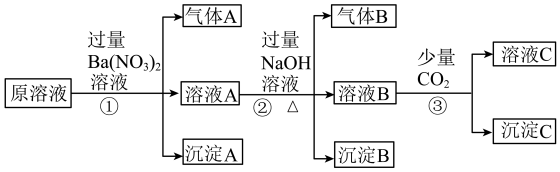
(1)由强酸性条件即可判断原溶液中一定不存在的离子有_____ 。
(2)写出生成气体A的离子方程式:_____ 。
(3)写出气体A和气体B在催化剂、加热条件下反应生成无毒物质的化学方程式:_____ 。
(4)沉淀C中一定有_____ (填化学式,下同),可能有_____ 。
(5)通过以上分析知,原溶液中一定含有的离子有_____ 。
 、Ba2+、Cl﹣、
、Ba2+、Cl﹣、 、
、 、SiO
、SiO 、
、 中的若干种,现取适量该溶液进行如下实验。
中的若干种,现取适量该溶液进行如下实验。
(1)由强酸性条件即可判断原溶液中一定不存在的离子有
(2)写出生成气体A的离子方程式:
(3)写出气体A和气体B在催化剂、加热条件下反应生成无毒物质的化学方程式:
(4)沉淀C中一定有
(5)通过以上分析知,原溶液中一定含有的离子有
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】有一包白色粉末可能含硫酸钡、碳酸钠、和氢氧化钡中的一种或几种,取一定量的该粉末加入到盛有足量水的烧杯中,搅拌、静置,观察到有白色不溶物。
小张同学认为,白色粉末中一定含有硫酸钡;
小李同学认为,小张同学的结论不准确,其理由可用化学方程式表示为______________ 。
针对上述两名同学的观点,小刘同学进一步设计如下实验方案进行探究:

(1)步骤③中,滴入酚酞溶液后,若滤液E为红色,则滤液E中除酚酞外还一定含有的溶质是_______ (填化学式,下同),由此得出原白色粉末成分组成的结论是______________ 。
(2)小王同学认为,只需要取少量滤渣B,加入过量的稀盐酸,若看到的现象是白色不溶物部分溶解,且有气泡产生,就足以说明原白色粉末的成分是__________________ 。
小张同学认为,白色粉末中一定含有硫酸钡;
小李同学认为,小张同学的结论不准确,其理由可用化学方程式表示为
针对上述两名同学的观点,小刘同学进一步设计如下实验方案进行探究:

(1)步骤③中,滴入酚酞溶液后,若滤液E为红色,则滤液E中除酚酞外还一定含有的溶质是
(2)小王同学认为,只需要取少量滤渣B,加入过量的稀盐酸,若看到的现象是白色不溶物部分溶解,且有气泡产生,就足以说明原白色粉末的成分是
您最近一年使用:0次



