回答下列问题:
(1)在标准状况下,有物质①44. 8 LH2,②24 gCH4,③l molH2O,④3. 01×1023个O2,含分子数最多的是___________ (填序号,下同),含电子数最多的是___________ ,质量最大的是___________ ,体积最小的是___________ ;
(2)选择下列实验方法分离物质,将分离方法的序号填在横线上。
a、萃取分液法;b、 加热分解; c、结晶法;d、 分液法;e、蒸馏法;f、 过滤法
①___________ 从硝酸钾 和氯化钠的混合溶液中获得硝酸钾
②___________ 分离水和苯的混合物
③___________ 分离碘和四氯化碳
④___________ 分离食盐水和沙子的混合物
(1)在标准状况下,有物质①44. 8 LH2,②24 gCH4,③l molH2O,④3. 01×1023个O2,含分子数最多的是
(2)选择下列实验方法分离物质,将分离方法的序号填在横线上。
a、萃取分液法;b、 加热分解; c、结晶法;d、 分液法;e、蒸馏法;f、 过滤法
①
②
③
④
更新时间:2022-09-17 07:17:42
|
相似题推荐
【推荐1】(1)常温常压下,用等质量的 、
、 、
、 、
、 四种气体分别吹出四个气球,其中气体为
四种气体分别吹出四个气球,其中气体为 的是
的是___________ (填序号)。
A . B .
B . C .
C . D.
D.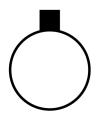
(2)在标准状况下,2.24L由 、
、 组成的混合气体中含有的氮元素的质量约为
组成的混合气体中含有的氮元素的质量约为___________ 。
(3)在0.1L由KCl、 、
、 形成的植物营养液中,
形成的植物营养液中,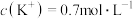 ,
,
 ,
,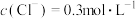 ,向混合溶液中滴加足量的
,向混合溶液中滴加足量的 溶液后产生沉淀的物质的量为
溶液后产生沉淀的物质的量为________ 。
(4)在干燥烧瓶中用向下排空气法收集氨气(已知:空气不可能排净,空气的平均相对分子质量为29,瓶内气体对氢气的相对密度为9.5,氨气极易溶于水),将此瓶气体倒置于水槽中,烧瓶内液面上升的体积占烧瓶总体积的___________ 。
(5) 溶液(密度为
溶液(密度为 )和
)和 溶液(密度为
溶液(密度为 )的混合,所得密度为
)的混合,所得密度为 的混合溶液中
的混合溶液中 的浓度为
的浓度为____________ (用含 、
、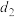 、
、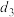 的式子表示)。
的式子表示)。
 、
、 、
、 、
、 四种气体分别吹出四个气球,其中气体为
四种气体分别吹出四个气球,其中气体为 的是
的是A .
 B .
B . C .
C . D.
D.
(2)在标准状况下,2.24L由
 、
、 组成的混合气体中含有的氮元素的质量约为
组成的混合气体中含有的氮元素的质量约为(3)在0.1L由KCl、
 、
、 形成的植物营养液中,
形成的植物营养液中,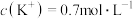 ,
,
 ,
,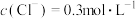 ,向混合溶液中滴加足量的
,向混合溶液中滴加足量的 溶液后产生沉淀的物质的量为
溶液后产生沉淀的物质的量为(4)在干燥烧瓶中用向下排空气法收集氨气(已知:空气不可能排净,空气的平均相对分子质量为29,瓶内气体对氢气的相对密度为9.5,氨气极易溶于水),将此瓶气体倒置于水槽中,烧瓶内液面上升的体积占烧瓶总体积的
(5)
 溶液(密度为
溶液(密度为 )和
)和 溶液(密度为
溶液(密度为 )的混合,所得密度为
)的混合,所得密度为 的混合溶液中
的混合溶液中 的浓度为
的浓度为 、
、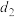 、
、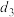 的式子表示)。
的式子表示)。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】在273K和101kPa的条件下,将2.00g氦气,1.40g氮气和1.60g氧气混合,求:
(1)该混合气体的总物质的量为______________
(2)该混合气体的体积是_______________
(3)该混合气体的平均摩尔质量为_________
(1)该混合气体的总物质的量为
(2)该混合气体的体积是
(3)该混合气体的平均摩尔质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】光卤石(xKCl·yMgCl2·zH2O)的组成可通过下列实验测定:
(1)准确称取5.550g样品溶于水,配成100.00mL溶液,将溶液分成二等份。配制100.00mL溶液时,所需的玻璃仪器有:烧杯、玻璃棒、胶头滴管,还有_______ 。
(2)在一份中加入足量的NaOH溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体[Mg(OH)2]0.580g,其中一份中n(Mg2+)=_________ mol
(3)在另一份溶液中加入足量的HNO3酸化的AgNO3溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体4.305g,其中一份中n(Cl-)=________ mol
(4)其中一份中n(K+)=___________ mol,n(H2O)=____________ mol
(5)光卤石的化学式为______________________
(1)准确称取5.550g样品溶于水,配成100.00mL溶液,将溶液分成二等份。配制100.00mL溶液时,所需的玻璃仪器有:烧杯、玻璃棒、胶头滴管,还有
(2)在一份中加入足量的NaOH溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体[Mg(OH)2]0.580g,其中一份中n(Mg2+)=
(3)在另一份溶液中加入足量的HNO3酸化的AgNO3溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体4.305g,其中一份中n(Cl-)=
(4)其中一份中n(K+)=
(5)光卤石的化学式为
您最近一年使用:0次
【推荐1】我国政府为了消除碘缺乏病,规定在食盐中必须加入适量的碘酸。检验实验中是否加碘,可利用如下反应:
(1)该反应中氧化剂和还原剂的物质的量之比为___________ ;
(2)如果反应中转移0.5mol电子,则生成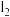 的物质的量为
的物质的量为_____________ ;
(3)若要提取生成的碘,所用的萃取剂可以是_________ (填序号)
①水 ②酒精 ③淀粉溶液 ④四氯化碳

(1)该反应中氧化剂和还原剂的物质的量之比为
(2)如果反应中转移0.5mol电子,则生成
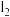 的物质的量为
的物质的量为(3)若要提取生成的碘,所用的萃取剂可以是
①水 ②酒精 ③淀粉溶液 ④四氯化碳
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】在一定温度下,溶质溶解在两种互相接触但互不相溶的溶剂中的浓度之比是一个常数K。若CA(克/升)、CB(克/升)分别表示溶质在A、B两种溶液中的浓度,则CA/CB=K。对溶质碘来说,有CCCl4/CH2O=85。现有2升碘水,其中含碘为0.02克。若用CCl4为萃取剂,以两种不同方法进行萃取:
(1)第一种方法是用50毫升萃取剂萃取一次,则水中残余碘的质量为_________ g。
(2)第二种方法是分两次萃取,每次用25毫升萃取剂,求水中残余碘的质量。____________
(1)第一种方法是用50毫升萃取剂萃取一次,则水中残余碘的质量为
(2)第二种方法是分两次萃取,每次用25毫升萃取剂,求水中残余碘的质量。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】(1)区别溶液和胶体的一种常用的物理方法是______ 。
(2)分离两种相互溶解但沸点相差较大的液体常用的实验方法是______ 。
(3)0.1 mol/L Al2(SO4)3中Al3+的物质的量浓度是______ ;同温同压下,等体积的CO和CO2所含分子数之比为________ 。
(4)已知:KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O反应中的氧化剂是______ (写化学式),被氧化的元素是____ (写元素符号)。
(5)若该反应中生成标准状况下的Cl2为67.2 L,则转移的电子个数是_________ 。
(2)分离两种相互溶解但沸点相差较大的液体常用的实验方法是
(3)0.1 mol/L Al2(SO4)3中Al3+的物质的量浓度是
(4)已知:KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O反应中的氧化剂是
(5)若该反应中生成标准状况下的Cl2为67.2 L,则转移的电子个数是
您最近一年使用:0次



