1 . 碘酸铜[Cu(IO3)2]是一种化工产品,难溶于水。某研究小组利用含碘废液制备碘酸铜并测定其纯度。
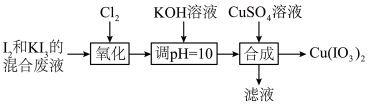
(1)“氧化”中制得HIO3.装置如图甲所示:
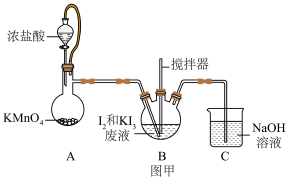
①写出A中发生反应的离子方程式:___________ 。。
②“氧化”在___________ (填仪器名称)中进行, KI3发生反应的化学方程式为___________ 。
③证明B中不含I2的实验方法是___________ 。
(2)分离产品。相对普通过滤,用如图乙所示装置分离产品的主要优点有___________ 。其中安全瓶的作用是___________ 。
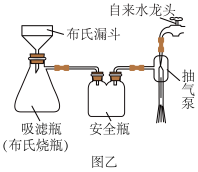
(3)测定产品纯度。
取Wg产品溶于水,加入足量的经酸化的KI溶液,充分反应后,滴加几滴指示剂,用c mol/LNa2S2O3溶液滴定至终点,消耗滴定液体积V mL,有关反应:2Cu2+ +4 +24I-+24H+=2CuI↓+13I2+12H2O,I2+2
+24I-+24H+=2CuI↓+13I2+12H2O,I2+2 =2I- +
=2I- + 。
。
①滴定终点的现象是___________ 。
②该产品纯度为___________ 。
③如果滴定过程中振荡锥形瓶时间太长,导致空气进入,则测定结果___________ (填“偏高”、“偏低”或“无影响”)。

(1)“氧化”中制得HIO3.装置如图甲所示:

①写出A中发生反应的离子方程式:
②“氧化”在
③证明B中不含I2的实验方法是
(2)分离产品。相对普通过滤,用如图乙所示装置分离产品的主要优点有

(3)测定产品纯度。
取Wg产品溶于水,加入足量的经酸化的KI溶液,充分反应后,滴加几滴指示剂,用c mol/LNa2S2O3溶液滴定至终点,消耗滴定液体积V mL,有关反应:2Cu2+ +4
 +24I-+24H+=2CuI↓+13I2+12H2O,I2+2
+24I-+24H+=2CuI↓+13I2+12H2O,I2+2 =2I- +
=2I- + 。
。①滴定终点的现象是
②该产品纯度为
③如果滴定过程中振荡锥形瓶时间太长,导致空气进入,则测定结果
您最近半年使用:0次
名校
解题方法
2 . 下列实验操作正确或规范的是
| A.水银温度计破碎后,立即用水冲洗地面上的水银 |
| B.为节约资源,蒸馏实验防暴沸时将使用过的沸石重复利用 |
| C.润洗滴定管时,将第一次润洗液从上口放出,后两次润洗液从下口放出 |
| D.减压过滤时应选择大于布氏漏斗内径的滤纸,边缘翘起,盖住漏斗内所有小孔 |
您最近半年使用:0次
2023高三·全国·专题练习
解题方法
3 . 硼镁泥主要成分是MgO(占40%),还含有Na2B4O7、CaO、Al2O3、Fe2O3、FeO、MnO、SiO2等杂质。以硼镁泥为原料制取MgSO4·7H2O的工艺流程如下
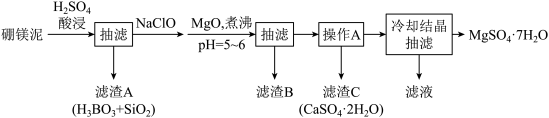
本实验中多次用到抽滤操作,其装置如图,相比普通过滤,抽滤的优点是___________ 。
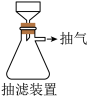

本实验中多次用到抽滤操作,其装置如图,相比普通过滤,抽滤的优点是

您最近半年使用:0次
2023·全国·模拟预测
解题方法
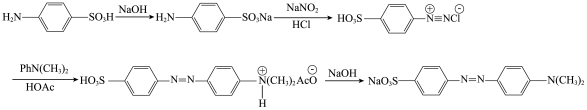
4 . 甲基橙[ ]是一种常见的酸碱指示剂。实验室通过将对氨基苯磺酸与NaOH作用生成易溶于水的盐,再与
]是一种常见的酸碱指示剂。实验室通过将对氨基苯磺酸与NaOH作用生成易溶于水的盐,再与 重氨化,然后与N,N-二甲基苯胺偶联得到粗产品甲基橙。反应原理如下:
重氨化,然后与N,N-二甲基苯胺偶联得到粗产品甲基橙。反应原理如下:
实验过程为

(1)实验过程中为缩短制备时间、加快制备速率,采取的措施有_______ (任写两项)。
(2)淀粉-KI试纸用于检验生成重氮盐时 是否过量。若
是否过量。若 过量,可观察到的现象有
过量,可观察到的现象有_______ ,反应的化学方程式为_______ 。
(3)①选择合适仪器并组装抽滤装置,安装顺序为_______ (填序号)。

②抽滤也称减压过滤,下列说法不正确的是_______ (填序号)。
A.抽滤的原理是利用抽气泵使抽滤瓶中的压强降低,以达到固液分离的目的
B.抽滤的优点是过滤速度快,可得到较干燥的沉淀
C.过滤完之后,先关抽气泵,后去除抽滤瓶接管
③抽滤后,收集晶体,依次用少量水、乙醇、乙醚洗涤,最后压干。用乙醇、乙醚洗涤的目的是_______ ,防止产品变质。
(4)采用_______ 的方法提纯甲基橙粗产品,获得甲基橙精产品。
(5)滴定实验中一般要选择合适的指示剂,下列滴定中能选择甲基橙作指示剂且滴定终点颜色变化正确的是_______ (填序号)。
 ]是一种常见的酸碱指示剂。实验室通过将对氨基苯磺酸与NaOH作用生成易溶于水的盐,再与
]是一种常见的酸碱指示剂。实验室通过将对氨基苯磺酸与NaOH作用生成易溶于水的盐,再与 重氨化,然后与N,N-二甲基苯胺偶联得到粗产品甲基橙。反应原理如下:
重氨化,然后与N,N-二甲基苯胺偶联得到粗产品甲基橙。反应原理如下:
实验过程为

(1)实验过程中为缩短制备时间、加快制备速率,采取的措施有
(2)淀粉-KI试纸用于检验生成重氮盐时
 是否过量。若
是否过量。若 过量,可观察到的现象有
过量,可观察到的现象有(3)①选择合适仪器并组装抽滤装置,安装顺序为

②抽滤也称减压过滤,下列说法不正确的是
A.抽滤的原理是利用抽气泵使抽滤瓶中的压强降低,以达到固液分离的目的
B.抽滤的优点是过滤速度快,可得到较干燥的沉淀
C.过滤完之后,先关抽气泵,后去除抽滤瓶接管
③抽滤后,收集晶体,依次用少量水、乙醇、乙醚洗涤,最后压干。用乙醇、乙醚洗涤的目的是
(4)采用
(5)滴定实验中一般要选择合适的指示剂,下列滴定中能选择甲基橙作指示剂且滴定终点颜色变化正确的是
| 选项 | 滴定管中的溶液 | 锥形瓶中的溶液 | 滴定终点颜色变化 |
| A | NaOH溶液 |  溶液 溶液 | 红色→橙色 |
| B | 盐酸 | 氨水 | 黄色→橙色 |
| C | NaOH溶液 | 盐酸 | 黄色→橙色 |
| D | 酸性 溶液 溶液 |  溶液 溶液 | 红色→橙色 |
您最近半年使用:0次
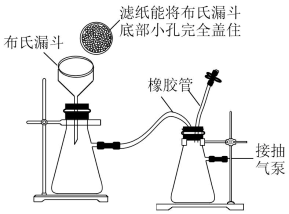
5 . “抽滤”在如图装置中进行,利用抽气泵将装置内的空气不断抽出,可使装置内的压强小于外界大气压,试分析抽滤较普通过滤的优点有_______ (任写一点)。

您最近半年使用:0次
6 . 甲~丁图为中学化学常用的仪器的全部或局部,下列说法不正确的是
 |  | 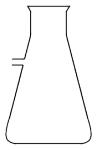 |  |
| 甲 | 乙 | 丙 | 丁 |
| A.甲图所示仪器不能用于蒸馏,因为冷凝下来的液体会存留于球泡处 |
| B.乙图所示仪器使用前需检查是否漏水 |
| C.丙图所示仪器可用于酸碱中和滴定和减压过滤 |
| D.丁图所示仪器检查气密性后装入药品,才能制备气体 |
您最近半年使用:0次
真题
解题方法
7 . 名称为“吸滤瓶”的仪器是
A.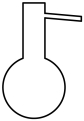 | B. | C.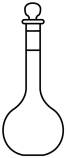 | D.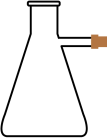 |
您最近半年使用:0次
2022-06-14更新
|
5365次组卷
|
14卷引用:2022年6月浙江省普通高校招生选考化学试题
2022年6月浙江省普通高校招生选考化学试题(已下线)2022年浙江省6月高考真题变式题1-10(已下线)考点49 化学实验基础-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第27讲 化学实验基础知识和技能(练)-2023年高考化学一轮复习讲练测(全国通用)(已下线)第25讲 常见仪器使用和实验基本操作 (讲)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)易错点31 化学实验常用仪器-备战2023年高考化学考试易错题浙江省东阳市横店高级中学2022-2023学年高三上学期10月份检测化学试题(已下线)专题13 化学实验基础(已下线)专题13 化学实验基础(已下线)第08练 实验仪器的选用与基本操作 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)(已下线)专题05 化学实验基础-2023年高考化学真题题源解密(全国通用)(已下线)考点44 化学实验基础(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)考点1 常见仪器使用和实验基本操作(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)第1讲 常用的仪器及基本操作
8 . 化工原料K2([Cu(C2O4)2]·2H2O(二草酸合铜酸钾晶体)为蓝色针状或絮状沉淀,某校同学设计实验制备K2([Cu(C2O4)2]·2H2O,并进行性质探究。
已知: Cu(OH)2分解温度为80°C; Cu2O 为红色。
回答下列相关问题:
[实验一] 制备K2([Cu(C2O4)2]·2H2O晶体
(1)向CuSO4溶液中加入足量NaOH,搅拌加热至80~90°C,观察到的现象是___________ ; 采用如图装置抽滤,打开水龙头,可在布氏漏斗中快速过滤出沉淀,快速过滤的原理是___________ 。
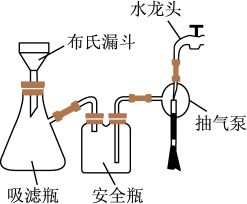
(2)将H2C2O4·2H2O和K2CO3溶液混合制备KHC2O4溶液,则酸性H2C2O4___________ H2CO3(填“大于”“小于”或“等于”)。
(3)将(1)步抽滤出的沉淀加入(2) 步KHC2O4溶液中,50°C的水浴加热充分反应,过滤得K2([Cu(C2O4)2]·2H2O。发生反应的化学方程式为___________ 。
[实验二]探究K2([Cu(C2O4)2]·2H2O晶体热分解产物
按如图所示,装置B、C、F中均盛有足量的澄清石灰水。
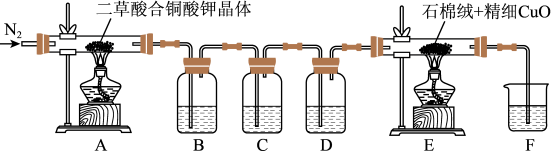
(4)实验操作步骤为:连接装置→___________ (用 数字编号回答)
a.检查装置气密性;b. 加热两处酒精灯;c. 熄灭两处酒精灯: d.通氮气;e.停止通氮气;f.装入药品
①f→a→b→d→e→c ②a→f→d→b→c→e
③a→f→b→d→e→c ④f→a→d→b→c→e
(5)D中盛放的试剂是___________ ,将K2([Cu(C2O4)2]·2H2O晶体持续加热至600°C左右,观察到装置B中澄清石灰水变浑浊,E中黑色固体变为红色,由此可判断分解产生的气体产物为___________ 。 充分分解后冷却,观察到A中固体未见黑色物质,取少量固体于试管中,滴加足量稀硫酸振荡,有气体产生,溶液变蓝,静置仍有红色固体,由此判断试管A中固体成分为___________ (将可能情况全部列出)。
已知: Cu(OH)2分解温度为80°C; Cu2O 为红色。
回答下列相关问题:
[实验一] 制备K2([Cu(C2O4)2]·2H2O晶体
(1)向CuSO4溶液中加入足量NaOH,搅拌加热至80~90°C,观察到的现象是

(2)将H2C2O4·2H2O和K2CO3溶液混合制备KHC2O4溶液,则酸性H2C2O4
(3)将(1)步抽滤出的沉淀加入(2) 步KHC2O4溶液中,50°C的水浴加热充分反应,过滤得K2([Cu(C2O4)2]·2H2O。发生反应的化学方程式为
[实验二]探究K2([Cu(C2O4)2]·2H2O晶体热分解产物
按如图所示,装置B、C、F中均盛有足量的澄清石灰水。

(4)实验操作步骤为:连接装置→
a.检查装置气密性;b. 加热两处酒精灯;c. 熄灭两处酒精灯: d.通氮气;e.停止通氮气;f.装入药品
①f→a→b→d→e→c ②a→f→d→b→c→e
③a→f→b→d→e→c ④f→a→d→b→c→e
(5)D中盛放的试剂是
您最近半年使用:0次
解题方法
9 . 下列说法不正确 的是
| A.减压过滤不适用于过滤胶状氢氧化物类沉淀 |
| B.实验室电器设备着火,可用高压二氧化碳灭火器灭火 |
C.制备硫酸亚铁铵晶体时,可将含 和 和 的溶液浓缩至干 的溶液浓缩至干 |
D.将热的 饱和溶液置于冰水中快速冷却可制得细颗粒的晶体 饱和溶液置于冰水中快速冷却可制得细颗粒的晶体 |
您最近半年使用:0次
10 . 电镀废液中含有Cu2+、Mg2+、Ca2+、Ni2+和Fe3+,某专利申请用下列方法从该类废液中制备高纯度的铜粉。

已知导体和其接触的溶液的界面上会形成一定的电位差,被称作电极电位。如反应Cu2+(氧化态)+2e-=Cu(还原态)的标准电极电位表示为Cu2+/Cu=0.34,该值越大氧化态的氧化性越强,越小还原态的还原性越强。两个电对间的电极电位差别越大,二者之间的氧化还原反应越易发生。某些电对的电极电位如下表所示:
回答下列问题:
(1)蒸发浓缩后的溶液中,Cu2+的物质的量浓度≥_______ (结果保留两位小数)。分离固液混合物时,需要用真空抽滤的方法提高过滤的速度和效果,其原因是_______ 。
(2)溶液的氧化还原电位越高,其氧化能力同样越强。溶液的氧化还原电位,与溶液中离子等微粒的种类及其浓度相关,实验测得Cu2+与SO2反应体系的氧化还原电位与铜粉的回收率和纯度的关系如下表所示:
①由此可知,制备过程中进行电位检测时,要把溶液的氧化还原电位控制在_______ mV左右。
②专利申请书指出,反应液的反应历程为Cu2+首先被还原为Cu+,Cu+再歧化为Cu和Cu2+。反应历程不是Cu2+直接被还原为Cu的原因是_______ 。反应生成Cu+的离子方程式是_______ 。
(3)废液2中含有的金属离子除Mg2+、Ca2+外还有_______ 。为了使这些离子均除去,使水得到进一步的净化,应该在调节溶液pH使其他杂质离子沉淀后,再使Ca2+转化为_______ (填化学式)而除去。

已知导体和其接触的溶液的界面上会形成一定的电位差,被称作电极电位。如反应Cu2+(氧化态)+2e-=Cu(还原态)的标准电极电位表示为Cu2+/Cu=0.34,该值越大氧化态的氧化性越强,越小还原态的还原性越强。两个电对间的电极电位差别越大,二者之间的氧化还原反应越易发生。某些电对的电极电位如下表所示:
| Fe3+/Fe2+ | Cu2+/Cu+ | Cu2+/Cu |  /SO2 /SO2 | Fe2+/Fe | Ni2+/Ni | Mg2+/Mg | Ca2+/Ca |
| 0.77 | 0.52 | 0.34 | 0.17 | -0.44 | -0.23 | -2.38 | -2.76 |
(1)蒸发浓缩后的溶液中,Cu2+的物质的量浓度≥
(2)溶液的氧化还原电位越高,其氧化能力同样越强。溶液的氧化还原电位,与溶液中离子等微粒的种类及其浓度相关,实验测得Cu2+与SO2反应体系的氧化还原电位与铜粉的回收率和纯度的关系如下表所示:
| 反应液的电位(mV) | 360 | 340 | 320 | 300 | 280 | 260 |
| 铜粉的回收率(%) | 86.5 | 90.2 | 95.6 | 97.2 | 97.3 | 97.4 |
| 产品的纯度(%) | 99.9 | 99.9 | 99.9 | 99.9 | 99.9 | 99.9 |
②专利申请书指出,反应液的反应历程为Cu2+首先被还原为Cu+,Cu+再歧化为Cu和Cu2+。反应历程不是Cu2+直接被还原为Cu的原因是
(3)废液2中含有的金属离子除Mg2+、Ca2+外还有
您最近半年使用:0次



