1 . 下列实验结论与实验现象相符合的一组是
选项 | 实验 | 现象 | 结论 |
A | 向NaBr溶液中滴加过量氯水,再加入淀粉KI溶液 | 先变橙色,后变蓝色 | 氧化性: |
B | 向品红溶液中通入某气体 | 品红褪色 | 气体一定是 |
C | 向蔗糖中滴加浓硫酸 | 蔗糖变黑 | 浓硫酸具有吸水性 |
D | 向某盐溶液中加入浓NaOH溶液,加热 | 产生的气体能使湿润的红色石蕊试纸变蓝 | 原溶液中一定含有 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
2 . 体积相同,浓度均为 的两种试剂,改变两种试剂的滴加顺序,边滴加边振荡,反应现象没有明显差别的是
的两种试剂,改变两种试剂的滴加顺序,边滴加边振荡,反应现象没有明显差别的是
 的两种试剂,改变两种试剂的滴加顺序,边滴加边振荡,反应现象没有明显差别的是
的两种试剂,改变两种试剂的滴加顺序,边滴加边振荡,反应现象没有明显差别的是选项 | 试剂Ⅰ | 试剂Ⅱ |
A | 氨水 | 硫酸铜溶液 |
B |  溶液 溶液 |  溶液 溶液 |
C |  溶液 溶液 | NaOH溶液 |
D | KOH溶液 | 酸性 溶液 溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
3 . 劳动开创未来。下列劳动项目对应的化学知识错误的是
选项 | 劳动项目 | 化学知识 |
A | 园艺工人给花草施用草木灰 | 草木灰中含碳酸钾,可作钾肥 |
B | 游泳池水pH偏低时,养护人员用纯碱调节 | 碳酸钠能与 发生反应,使pH增大 发生反应,使pH增大 |
C | 芯片蚀刻工程师用含氢氟酸的混酸蚀刻芯片 | 硅的性质稳定,仅能与酸性很强的氢氟酸反应 |
D | 放射科医生给检查胃部的患者服用“钡餐”造影 | 硫酸钡难溶于水和酸,不能被人体吸收,无毒 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
4 . 下列有关硅从其化合物的叙述错误的是
| A.石英砂可用于生产高纯硅 |
| B.利用高纯硅半导体性能可以制成硅太阳能电池 |
| C.利用高纯硅半导体性能可以制成计算机的芯片 |
D. 硬度大,故可用来生产光导纤维 硬度大,故可用来生产光导纤维 |
您最近一年使用:0次
名校
解题方法
5 . 化合物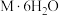 可用作洗涤粉,
可用作洗涤粉, 的结构如下,其中
的结构如下,其中 、
、 、
、 、
、 是原子序数依次增大的短周期主族元素,下列说法错误的是
是原子序数依次增大的短周期主族元素,下列说法错误的是
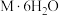 可用作洗涤粉,
可用作洗涤粉, 的结构如下,其中
的结构如下,其中 、
、 、
、 、
、 是原子序数依次增大的短周期主族元素,下列说法错误的是
是原子序数依次增大的短周期主族元素,下列说法错误的是
A. 的基态原子核外电子排布中有1个未成对电子 的基态原子核外电子排布中有1个未成对电子 |
| B.化合物WX为离子化合物,在野外可用作生氢剂 |
C.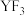 分子的空间构型是三角锥形 分子的空间构型是三角锥形 |
D. 的键角大于 的键角大于 的键角 的键角 |
您最近一年使用:0次
名校
解题方法
6 . 下列做法与调控化学反应速率无关的是
| A.食物存放在冰箱里 | B.橡胶制品中添加抑制剂 |
| C.Zn与稀硫酸反应,滴入少量硫酸铜溶液 | D.在利用Zn与 制取 制取 时,将稀硫酸改为浓硫酸 时,将稀硫酸改为浓硫酸 |
您最近一年使用:0次
7 . 1,6-己二醇是精细化工领域的一种重要原料,广泛应用于UV涂料、聚氨酯、环氧树脂、增塑剂等领域。己二酸二甲酯(DMA)直接加氢制备1,6-己二醇工艺的副产物少、三废少,且产品纯度较高。其制备原理为:
(1)已知
计算上述反应的
___________  。
。
(2)欲提高己二酸二甲酯(DMA)的平衡转化率,可采取下列措施中的___________ (填标号)。
A.适当增压 B.增大DMA的浓度 C.减小产物浓度 D.改进催化剂
反应后气态混合物冷却至室温,可分离出氢气,冷却过程中最先液化的是1,6-己二醇,其沸点最高的原因是___________ 。
(3)在恒温为T℃、恒容为VL的密闭容器中,若投入1mol DMA和4mol ,起始时压强为mkPa,反应th达到平衡,DMA的转化率为90%,则0~th的平均反应速率v(DMA)=
,起始时压强为mkPa,反应th达到平衡,DMA的转化率为90%,则0~th的平均反应速率v(DMA)=___________ 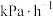 ;T℃下该反应的平衡常数K=
;T℃下该反应的平衡常数K=___________ 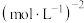 (列出计算式即可)。
(列出计算式即可)。
(4)用 作催化剂,反应压强为3MPa,
作催化剂,反应压强为3MPa,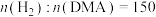 ,反应物以一定的流速通过反应管,测得不同温度下DMA的转化率和1,6-己二醇的收率(收率=转化率×选择性)关系如图所示,图中X点的
,反应物以一定的流速通过反应管,测得不同温度下DMA的转化率和1,6-己二醇的收率(收率=转化率×选择性)关系如图所示,图中X点的
___________  (填“大于”“小于”或“等于”);Y点后,随温度升高1,6-己二醇的收率下降的原因是
(填“大于”“小于”或“等于”);Y点后,随温度升高1,6-己二醇的收率下降的原因是___________ 。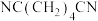 ]合成。
]合成。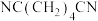 又可用丙烯腈(
又可用丙烯腈( )电有机合成,装置如图所示。
)电有机合成,装置如图所示。___________ 。
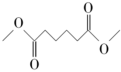 (g)+4H2(g)
(g)+4H2(g)
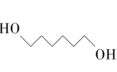 (g)+2CH3OH(g) ∆H
(g)+2CH3OH(g) ∆H
(1)已知
| 化学键 | C=O | C—O | C—H | C—C | O—H | H—H |
键能/ | 745 | a | 413 | b | 467 | 436 |

 。
。(2)欲提高己二酸二甲酯(DMA)的平衡转化率,可采取下列措施中的
A.适当增压 B.增大DMA的浓度 C.减小产物浓度 D.改进催化剂
反应后气态混合物冷却至室温,可分离出氢气,冷却过程中最先液化的是1,6-己二醇,其沸点最高的原因是
(3)在恒温为T℃、恒容为VL的密闭容器中,若投入1mol DMA和4mol
 ,起始时压强为mkPa,反应th达到平衡,DMA的转化率为90%,则0~th的平均反应速率v(DMA)=
,起始时压强为mkPa,反应th达到平衡,DMA的转化率为90%,则0~th的平均反应速率v(DMA)=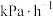 ;T℃下该反应的平衡常数K=
;T℃下该反应的平衡常数K=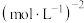 (列出计算式即可)。
(列出计算式即可)。(4)用
 作催化剂,反应压强为3MPa,
作催化剂,反应压强为3MPa,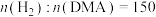 ,反应物以一定的流速通过反应管,测得不同温度下DMA的转化率和1,6-己二醇的收率(收率=转化率×选择性)关系如图所示,图中X点的
,反应物以一定的流速通过反应管,测得不同温度下DMA的转化率和1,6-己二醇的收率(收率=转化率×选择性)关系如图所示,图中X点的
 (填“大于”“小于”或“等于”);Y点后,随温度升高1,6-己二醇的收率下降的原因是
(填“大于”“小于”或“等于”);Y点后,随温度升高1,6-己二醇的收率下降的原因是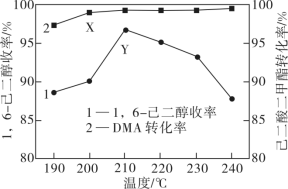
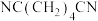 ]合成。
]合成。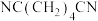 又可用丙烯腈(
又可用丙烯腈( )电有机合成,装置如图所示。
)电有机合成,装置如图所示。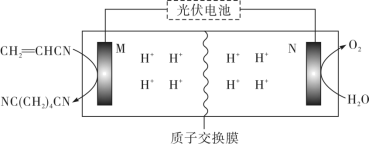
您最近一年使用:0次
名校
解题方法
8 . 某课外小组探究食品添加剂 (焦亚硫酸钠)制备原理,实验操作如下:(已知:焦亚硫酸钠可用饱和亚硫酸氢钠溶液脱水制得)
(焦亚硫酸钠)制备原理,实验操作如下:(已知:焦亚硫酸钠可用饱和亚硫酸氢钠溶液脱水制得)
已知: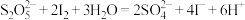 ;
;
 ,实验装置如下:
,实验装置如下:
(1)写出A中反应的化学方程式为______ 。装置 的作用是
的作用是______ 。
(2)第二步控制 中
中 ,若
,若 中溶质只有一种,
中溶质只有一种, 中反应的离子方程式是
中反应的离子方程式是______ 。
(3)第三步加热过程中若温度过高可能会生成 ,检验
,检验 固体是否变质的方法是
固体是否变质的方法是______ ,过滤操作用到的玻璃仪器有______ 。
(4)用于D处合理的装置是______ (填标号)。 :
:
①取 饮料于锥形瓶中,加入
饮料于锥形瓶中,加入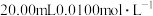 的
的 溶液,塞紧瓶塞充分反应。
溶液,塞紧瓶塞充分反应。
②打开瓶塞,将锥形瓶内液体调至接近中性,滴加 滴淀粉溶液做指示剂。用
滴淀粉溶液做指示剂。用 的
的 溶液滴定,滴定至终点时,消耗
溶液滴定,滴定至终点时,消耗 溶液
溶液 。滴定至终点的现象为:
。滴定至终点的现象为:______ 。饮料中残留的 为
为______  (已知
(已知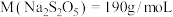 ;计算结果保留两位小数)。
;计算结果保留两位小数)。
 (焦亚硫酸钠)制备原理,实验操作如下:(已知:焦亚硫酸钠可用饱和亚硫酸氢钠溶液脱水制得)
(焦亚硫酸钠)制备原理,实验操作如下:(已知:焦亚硫酸钠可用饱和亚硫酸氢钠溶液脱水制得)实验步骤 | 实验操作 |
第一步 | 连接实验装置并检查装置气密性 |
第二步 |  、 、 、 、 中装入药品,加热 中装入药品,加热 中试管,通过 中试管,通过 数据采集器控制 数据采集器控制 中反应至 中反应至 时,停止加热,将 时,停止加热,将 中铜丝外移脱离浓硫酸 中铜丝外移脱离浓硫酸 |
第三步 | 将 中所得溶液转移至蒸发装置中,加热,结晶脱水、过滤、洗涤、干燥制得焦亚硫酸钠 中所得溶液转移至蒸发装置中,加热,结晶脱水、过滤、洗涤、干燥制得焦亚硫酸钠 |
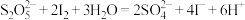 ;
; ,实验装置如下:
,实验装置如下: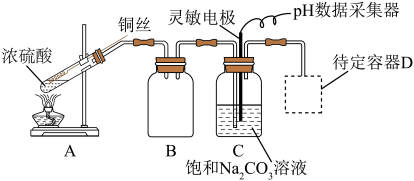
(1)写出A中反应的化学方程式为
 的作用是
的作用是(2)第二步控制
 中
中 ,若
,若 中溶质只有一种,
中溶质只有一种, 中反应的离子方程式是
中反应的离子方程式是(3)第三步加热过程中若温度过高可能会生成
 ,检验
,检验 固体是否变质的方法是
固体是否变质的方法是(4)用于D处合理的装置是
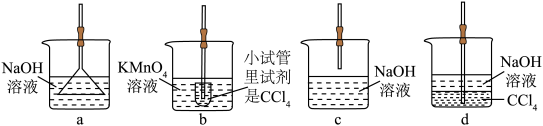
 :
:①取
 饮料于锥形瓶中,加入
饮料于锥形瓶中,加入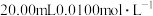 的
的 溶液,塞紧瓶塞充分反应。
溶液,塞紧瓶塞充分反应。②打开瓶塞,将锥形瓶内液体调至接近中性,滴加
 滴淀粉溶液做指示剂。用
滴淀粉溶液做指示剂。用 的
的 溶液滴定,滴定至终点时,消耗
溶液滴定,滴定至终点时,消耗 溶液
溶液 。滴定至终点的现象为:
。滴定至终点的现象为: 为
为 (已知
(已知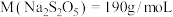 ;计算结果保留两位小数)。
;计算结果保留两位小数)。
您最近一年使用:0次
名校
9 .  为阿伏伽德罗常数,下列说法中正确的是
为阿伏伽德罗常数,下列说法中正确的是
 为阿伏伽德罗常数,下列说法中正确的是
为阿伏伽德罗常数,下列说法中正确的是A. 与 与 充分反应,当固体增重 充分反应,当固体增重 ,转移电子数为 ,转移电子数为 |
B.向 的 的 溶液中加入 溶液中加入 至溶液呈中性,溶液中醋酸根离子数目为 至溶液呈中性,溶液中醋酸根离子数目为 |
C. 钠与 钠与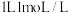 的盐酸反应时,转移电子数为 的盐酸反应时,转移电子数为 |
D.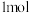 二氧化硅晶体中,所含硅氧键数目为 二氧化硅晶体中,所含硅氧键数目为 |
您最近一年使用:0次
10 . 联合多种工业制备是节能环保,高效生产,减少损耗的重要途径。钛和钛合金性能优良,广泛用于航空、造船和化学工业中。以钛铁矿(主要成分为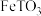 (其中
(其中 为
为 价),含有少量
价),含有少量 、
、 )为主要原料制取
)为主要原料制取 单质和绿矾
单质和绿矾 ,同时联合氯碱工业生产甲醇的工艺流程如图1所示。
,同时联合氯碱工业生产甲醇的工艺流程如图1所示。
回答下列问题:
(1)酸浸后,溶液中钛元素主要以 形式存在,则在酸浸工序中发生的主要反应的化学方程式为
形式存在,则在酸浸工序中发生的主要反应的化学方程式为______ 。
(2)某化学兴趣小组在实验室模拟该工艺流程,保持其他反应条件不变,测得加入铁屑还原体系中 (Ⅲ)含量随反应温度的变化如图2所示。为达到实验目的,最佳反应温度为
(Ⅲ)含量随反应温度的变化如图2所示。为达到实验目的,最佳反应温度为______ 。______ (填标号)。
a.工序①为趁热过滤、洗涤、干燥
b.先用适量稀硫酸洗涤绿矾并将洗涤液与滤液合并,可提高钛的产率
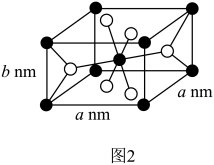
(4)灼烧后的成分为 ,可用作钛白颜料,该物质的一种晶胞结构(四方晶体)如图3所示。该晶体的密度为
,可用作钛白颜料,该物质的一种晶胞结构(四方晶体)如图3所示。该晶体的密度为______  (用含
(用含 、
、 、
、 的代数式表示,
的代数式表示, 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
(5)工序②生成的气体 为可燃性气体,生成气体
为可燃性气体,生成气体 的反应方程式为
的反应方程式为______ 。
(6)还原工序中通入氩气的目的是______ 。
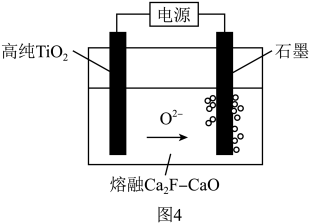
(7)利用图4装置可获得金属钛。在较低的阴极电位下, 中的氧解离进入熔融盐,最后只剩下纯钛,另一极产生
中的氧解离进入熔融盐,最后只剩下纯钛,另一极产生 、
、 和可燃性气体
和可燃性气体 。产生可燃性气体
。产生可燃性气体 的电极反应式为
的电极反应式为______ 。
 (其中
(其中 为
为 价),含有少量
价),含有少量 、
、 )为主要原料制取
)为主要原料制取 单质和绿矾
单质和绿矾 ,同时联合氯碱工业生产甲醇的工艺流程如图1所示。
,同时联合氯碱工业生产甲醇的工艺流程如图1所示。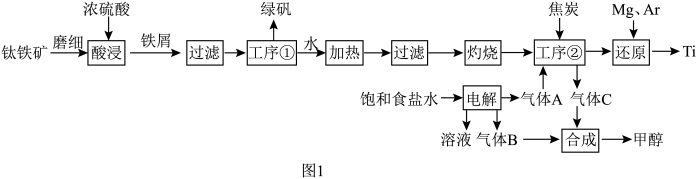

回答下列问题:
(1)酸浸后,溶液中钛元素主要以
 形式存在,则在酸浸工序中发生的主要反应的化学方程式为
形式存在,则在酸浸工序中发生的主要反应的化学方程式为(2)某化学兴趣小组在实验室模拟该工艺流程,保持其他反应条件不变,测得加入铁屑还原体系中
 (Ⅲ)含量随反应温度的变化如图2所示。为达到实验目的,最佳反应温度为
(Ⅲ)含量随反应温度的变化如图2所示。为达到实验目的,最佳反应温度为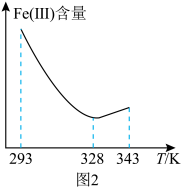
a.工序①为趁热过滤、洗涤、干燥
b.先用适量稀硫酸洗涤绿矾并将洗涤液与滤液合并,可提高钛的产率
(4)灼烧后的成分为
 ,可用作钛白颜料,该物质的一种晶胞结构(四方晶体)如图3所示。该晶体的密度为
,可用作钛白颜料,该物质的一种晶胞结构(四方晶体)如图3所示。该晶体的密度为 (用含
(用含 、
、 、
、 的代数式表示,
的代数式表示, 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
(5)工序②生成的气体
 为可燃性气体,生成气体
为可燃性气体,生成气体 的反应方程式为
的反应方程式为(6)还原工序中通入氩气的目的是
(7)利用图4装置可获得金属钛。在较低的阴极电位下,
 中的氧解离进入熔融盐,最后只剩下纯钛,另一极产生
中的氧解离进入熔融盐,最后只剩下纯钛,另一极产生 、
、 和可燃性气体
和可燃性气体 。产生可燃性气体
。产生可燃性气体 的电极反应式为
的电极反应式为
您最近一年使用:0次



