1 . 通过海水晾晒可以得到粗盐,粗盐除含有NaCl外,还含有 、
、 、
、 以及泥沙等杂质,其除杂过程如下:
以及泥沙等杂质,其除杂过程如下:
 、
、 、
、 以及泥沙等杂质,其除杂过程如下:
以及泥沙等杂质,其除杂过程如下: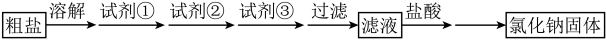
| A.该粗盐除杂过程不涉及到氧化还原反应 |
| B.盐酸作用是调节溶液pH,使溶液呈中性或微酸性,可以用硫酸替代 |
C.检验 是否除净:取少量滤液,加稀盐酸酸化,再加 是否除净:取少量滤液,加稀盐酸酸化,再加 溶液 溶液 |
| D.该除杂过程分别在溶解、过滤、蒸发三操作中3次用到玻璃棒 |
您最近一年使用:0次
解题方法
2 . 粗盐中含有难溶性杂质(泥沙等)和多种可溶性杂质(氯化镁、氯化钙等)。某班同学在粗盐提纯实验中,为把少量可溶性杂质 、
、 一并除去,设计了如下方案:
一并除去,设计了如下方案:
(1)为了加快粗盐的溶解,可采取的措施有_______ (填一种即可)。
(2)写出步骤ⅳ中发生反应的化学方程式:_______ 。
(3)沉淀B的主要成分为_______ (填化学式);往沉淀B中加入足量稀盐酸,观察到的现象为_______ 。
(4)在步骤ⅵ中,___ (填“能”或“不能”)用稀硝酸代替稀盐酸进行该实验,理由为____ 。
(5)步骤ⅶ中操作b指的是_______ 。
(6)该方案实际得到的氯化钠比粗盐中含有的氯化钠要多,理由为_______ 。
 、
、 一并除去,设计了如下方案:
一并除去,设计了如下方案: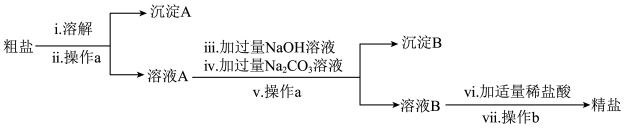
(1)为了加快粗盐的溶解,可采取的措施有
(2)写出步骤ⅳ中发生反应的化学方程式:
(3)沉淀B的主要成分为
(4)在步骤ⅵ中,
(5)步骤ⅶ中操作b指的是
(6)该方案实际得到的氯化钠比粗盐中含有的氯化钠要多,理由为
您最近一年使用:0次
解题方法
3 . 实验活动探究---食盐的精制
实验目的:从粗食盐水中除去
实验用品:
试剂:粗食盐水,稀盐酸,稀硫酸, 溶液,
溶液, 溶液,
溶液, 溶液,
溶液, 溶液
溶液
仪器:烧杯,漏斗,玻璃棒,表面皿, 试纸,滤纸,试管,胶头滴管,铁架台(带铁圈)
试纸,滤纸,试管,胶头滴管,铁架台(带铁圈)
实验操作流程: 离子,需加入过量的
离子,需加入过量的_______ ,写出①中反应的离子方程式_______ 。
(2)操作②加入过量的____ ,写出②中反应的离子方程式___ ;操作③加入过量的 溶液,除了除去
溶液,除了除去 ,还要除去操作①引入的杂质离子
,还要除去操作①引入的杂质离子______ 。
(3)操作④为_______ ,其中玻璃棒的作用是_______ 。
(4)操作⑤向滤液中滴加盐酸,用玻璃棒搅拌,直到_______ ,并用 试纸检验,使滤液呈中性或微酸性。
试纸检验,使滤液呈中性或微酸性。
(5)操作流程④与⑤可以颠倒顺序吗?_______ ,为什么?_______ 。
实验目的:从粗食盐水中除去

实验用品:
试剂:粗食盐水,稀盐酸,稀硫酸,
 溶液,
溶液, 溶液,
溶液, 溶液,
溶液, 溶液
溶液仪器:烧杯,漏斗,玻璃棒,表面皿,
 试纸,滤纸,试管,胶头滴管,铁架台(带铁圈)
试纸,滤纸,试管,胶头滴管,铁架台(带铁圈)实验操作流程:
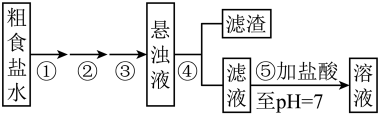
 离子,需加入过量的
离子,需加入过量的(2)操作②加入过量的
 溶液,除了除去
溶液,除了除去 ,还要除去操作①引入的杂质离子
,还要除去操作①引入的杂质离子(3)操作④为
(4)操作⑤向滤液中滴加盐酸,用玻璃棒搅拌,直到
 试纸检验,使滤液呈中性或微酸性。
试纸检验,使滤液呈中性或微酸性。(5)操作流程④与⑤可以颠倒顺序吗?
您最近一年使用:0次
4 . 下列装置正确且能达到相应实验目的的是

A.用装置甲模拟侯氏制碱,从b口通入的气体为 |
B.装置乙用于检验溶液A中是否含有 |
C.装置丙可用于吸收 |
D.装置丁用于除去 中的 中的 气体 气体 |
您最近一年使用:0次
名校
解题方法
5 . 某化学兴趣小组用化学沉淀法去除100gNaCl质量分数为87.75%的粗盐中的 、
、 和
和 ,实验流程如图所示,下列说法正确的是
,实验流程如图所示,下列说法正确的是 的溶解度为3.89g/100g水,
的溶解度为3.89g/100g水, 的溶解度为35.7g/100g水。
的溶解度为35.7g/100g水。
 、
、 和
和 ,实验流程如图所示,下列说法正确的是
,实验流程如图所示,下列说法正确的是
 的溶解度为3.89g/100g水,
的溶解度为3.89g/100g水, 的溶解度为35.7g/100g水。
的溶解度为35.7g/100g水。A.试剂a、试剂b分别为 溶液、NaOH溶液 溶液、NaOH溶液 |
B.滤渣c的主要成分为 、 、 、 、 和 和 |
C.从成本和除杂效果考虑,工业生产中常用 溶液代替 溶液代替 溶液 溶液 |
| D.不考虑实验损耗,最终获得的NaCl的物质的量为1.5mol |
您最近一年使用:0次
2024-04-29更新
|
87次组卷
|
2卷引用:湖南省衡阳市衡阳县三校2023-2024学年高一下学期三月联考化学试题
6 . 为除去粗盐中的 、
、 、
、 、
、 以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如图(用于沉淀的试剂稍过量),有关说法正确的是
以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如图(用于沉淀的试剂稍过量),有关说法正确的是
 、
、 、
、 、
、 以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如图(用于沉淀的试剂稍过量),有关说法正确的是
以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如图(用于沉淀的试剂稍过量),有关说法正确的是
| A.步骤①:根据粗盐的质量和溶解度来确定烧杯和量筒的规格 |
B.步骤②~④: 、 、 和 和 的滴加“顺序”和“量”不可调整 的滴加“顺序”和“量”不可调整 |
C.步骤⑥:用玻璃棒搅拌滤液,直到没有气泡冒出,且 试纸检验滤液呈碱性 试纸检验滤液呈碱性 |
| D.步骤①~⑦:需要的实验用品有分液漏斗、蒸发皿、玻璃棒、陶土网和胶头滴管 |
您最近一年使用:0次
2024-04-29更新
|
401次组卷
|
2卷引用:浙江省丽水湖州衢州三地市2024届高三下学期4月教学质量检测化学试题
名校
解题方法
7 . 活性氧化锌能对太阳光线和其他大气物质形成防护,常用于敏感皮肤的面霜和化妆品。工业上用菱锌矿(主要成分为ZnCO3,还含有Ni、Cd、Fe、Cu等元素及少量不溶于水的杂质)制备ZnO,工艺流程图所示:___________ ,常温下Fe2+比Fe3+更容易被氧化变质,请从结构角度加以解释___________ 。
(2)加入H2O2的目的是___________ ;“调pH”时除ZnO外还可以选用的物质是___________ 。
a.氨水 b.氢氧化铁 c.氢氧化锌
(3)常温下、pH=5时,Fe3+的浓度降到了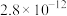 mol/L,此时Fe(OH)3的溶度积常数的数值为
mol/L,此时Fe(OH)3的溶度积常数的数值为___________ 。证明Fe3+已除尽的化学方法是___________ 。
(4)已知沉锌时固体产物是Zn2(OH)2CO3,请写出该过程的离子方程式:___________ 。
(5)粗锌中含有少量Al、Fe、Cu等杂质,可用电解法制备高纯度锌,下列叙述正确的是___________。

(2)加入H2O2的目的是
a.氨水 b.氢氧化铁 c.氢氧化锌
(3)常温下、pH=5时,Fe3+的浓度降到了
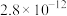 mol/L,此时Fe(OH)3的溶度积常数的数值为
mol/L,此时Fe(OH)3的溶度积常数的数值为(4)已知沉锌时固体产物是Zn2(OH)2CO3,请写出该过程的离子方程式:
(5)粗锌中含有少量Al、Fe、Cu等杂质,可用电解法制备高纯度锌,下列叙述正确的是___________。
| A.粗锌作阳极,纯锌作阴极,电解质溶液是硫酸锌溶液 |
| B.电解过程中,阳极质量的减少与阴极质量的增加相等 |
| C.电解后,溶液中存在的金属阳离子只有Al3+、Fe2+和Zn2+ |
| D.电解后,电解槽底部的阳极泥中只有Cu |
您最近一年使用:0次
解题方法
8 . 下列混合物分离(或除杂)的方法正确的是
| A.除去Mg粉中的Al粉:加入足量NaOH溶液后,过滤、洗涤 |
| B.除去BaCO3固体中混有的BaSO4:加入过量盐酸后,过滤、洗涤 |
| C.除去NaHCO3溶液中的Na2CO3:加入适量稀盐酸 |
| D.除去Al2O3中的少量Fe2O3:加入过量氢氧化钠溶液,过滤、洗涤 |
您最近一年使用:0次
名校
解题方法
9 . 晾晒海水获得的粗盐中含有可溶性杂质 、
、 、
、 等。粗盐提纯的工艺流程如下,下列说法正确的是
等。粗盐提纯的工艺流程如下,下列说法正确的是
 、
、 、
、 等。粗盐提纯的工艺流程如下,下列说法正确的是
等。粗盐提纯的工艺流程如下,下列说法正确的是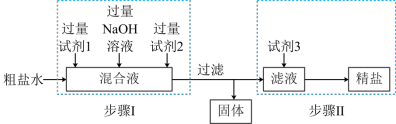
A.“步骤I”中试剂1为 溶液,试剂2为 溶液,试剂2为 溶液 溶液 |
| B.实验室分离“步骤I”生成的沉淀所需的玻璃仪器有烧杯、分液漏斗、玻璃棒 |
| C.“步骤II”中试剂3可以用稀硫酸代替稀盐酸 |
| D.“步骤II”从滤液中获得精盐的方法是蒸发结晶 |
您最近一年使用:0次
名校
解题方法
10 . 通过海水晾晒可得粗盐,粗盐中除NaCl外,还含有MgCl2、CaCl2、Na2SO4以及泥沙等杂质,需要提纯后才能综合利用。某同学利用给定试剂NaOH溶液、BaCl2溶液、Na2CO3溶液和盐酸,设计了如图粗盐精制的实验流程(提示:根据实验目的,请思考试剂的用量):
(1)操作a名称是___________ 。
(2)在实验室粗盐的提纯实验中,玻璃棒的使用不具有的作用是___________。
(3)试剂①是___________ 溶液(填化学式)。
(4)加入NaOH后,得到的主要沉淀B是___________ 。
(5)加入试剂②后,发生反应的离子方程式有___________ 。
(6)如果加入试剂②后直接加盐酸,产生的后果是___________ (用离子方程式表示)。

(1)操作a名称是
(2)在实验室粗盐的提纯实验中,玻璃棒的使用不具有的作用是___________。
| A.在溶解过程中搅拌 | B.在蒸发过程中搅拌 | C.在操作a时引流 | D.使固体析出 |
(3)试剂①是
(4)加入NaOH后,得到的主要沉淀B是
(5)加入试剂②后,发生反应的离子方程式有
(6)如果加入试剂②后直接加盐酸,产生的后果是
您最近一年使用:0次



