名校
1 . 海洋化学资源的研究和合理利用具有广阔前景,从海水中可提取氯、溴、碘等卤族元素。
1.氯离子结构示意图为___________ ,碘在元素周期表中的位置是___________ 。
2.氯气可用来制取漂白粉,漂白粉的有效成分是___________ 。
3.次氯酸钠可用于去除废水中的铵态氮,配平离子方程式并标出电子转移方向和数目。___________
___________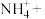 ___________
___________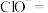 ___________
___________ ___________
___________ ___________
___________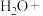 ___________
___________
1.氯离子结构示意图为
2.氯气可用来制取漂白粉,漂白粉的有效成分是
3.次氯酸钠可用于去除废水中的铵态氮,配平离子方程式并标出电子转移方向和数目。
___________
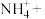 ___________
___________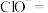 ___________
___________ ___________
___________ ___________
___________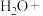 ___________
___________
您最近一年使用:0次
解题方法
2 . 有氧时在硝化细菌作用下, 可转化为
可转化为 和
和 ,将离子方程式补充完整(需配平,并用单线桥法标出电子的转移方向和数目)
,将离子方程式补充完整(需配平,并用单线桥法标出电子的转移方向和数目)______ 。
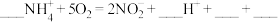 。
。
 可转化为
可转化为 和
和 ,将离子方程式补充完整(需配平,并用单线桥法标出电子的转移方向和数目)
,将离子方程式补充完整(需配平,并用单线桥法标出电子的转移方向和数目)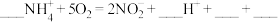 。
。
您最近一年使用:0次
名校
解题方法
3 . 某汽车安全气囊的产气药剂主要含有 、
、 、
、 等物质。当汽车发生碰撞时,产生大量气体使气囊迅速膨胀,从而起到保护作用。完成下列填空:
等物质。当汽车发生碰撞时,产生大量气体使气囊迅速膨胀,从而起到保护作用。完成下列填空:
(1) 是气体发生剂,受热分解产生
是气体发生剂,受热分解产生 与
与 。
。
① 的电子式为
的电子式为_______ 。
②Na与冷水常温下发生反应,请写出该反应的化学方程式_______ 。
(2) 含有的化学键类型为
含有的化学键类型为_______ 。
(3)从结构组成的分类, 属于
属于_______ (选填“离子化合物”或“共价化合物”),请写出鉴别离子化合物和共价化合物的方法:_______ 。
(4)某些安全气囊产气药剂中含 ,
, 为黑火药的主要成分之一、黑火药是中华民族对人类文明的重大贡献。它由
为黑火药的主要成分之一、黑火药是中华民族对人类文明的重大贡献。它由 、硫磺(S)、木炭(C)按一定比例混合而成,爆炸时主要反应如下:
、硫磺(S)、木炭(C)按一定比例混合而成,爆炸时主要反应如下: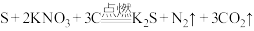
①标出该化学方程式电子转移的方向和数目_______ 。
②其中生成物 的电子式为
的电子式为_______ ; 的结构式为
的结构式为_______ 。
(5)黑火药的元素中,有一种元素单质可制药,其氧化物可做防腐剂、漂白剂,该元素在周期表中的位置是_______ ,该元素单核负离子的结构示意图为_______ 。
 、
、 、
、 等物质。当汽车发生碰撞时,产生大量气体使气囊迅速膨胀,从而起到保护作用。完成下列填空:
等物质。当汽车发生碰撞时,产生大量气体使气囊迅速膨胀,从而起到保护作用。完成下列填空:(1)
 是气体发生剂,受热分解产生
是气体发生剂,受热分解产生 与
与 。
。①
 的电子式为
的电子式为②Na与冷水常温下发生反应,请写出该反应的化学方程式
(2)
 含有的化学键类型为
含有的化学键类型为(3)从结构组成的分类,
 属于
属于(4)某些安全气囊产气药剂中含
 ,
, 为黑火药的主要成分之一、黑火药是中华民族对人类文明的重大贡献。它由
为黑火药的主要成分之一、黑火药是中华民族对人类文明的重大贡献。它由 、硫磺(S)、木炭(C)按一定比例混合而成,爆炸时主要反应如下:
、硫磺(S)、木炭(C)按一定比例混合而成,爆炸时主要反应如下: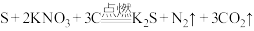
①标出该化学方程式电子转移的方向和数目
②其中生成物
 的电子式为
的电子式为 的结构式为
的结构式为(5)黑火药的元素中,有一种元素单质可制药,其氧化物可做防腐剂、漂白剂,该元素在周期表中的位置是
您最近一年使用:0次
名校
解题方法
4 . 工业制取碳化硅的化学反应方程式如下,请将方程式补充完整,并标出电子转移的方向数目:_______ 。
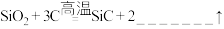
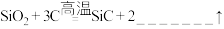
您最近一年使用:0次
名校
解题方法
5 . 以柠檬酸、硫酸亚铁、氨水等为原料制备食品添加剂—柠檬酸铁铵[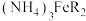 ,M=488g·mol-1]的流程如下所示:
,M=488g·mol-1]的流程如下所示:_______ 。
(2)欲检验FeSO4溶液是否被完全氧化,选用的试剂为_______。
(3)上述流程中,以13.90g绿矾(FeSO4·7H2O)配制FeSO4溶液,经各步骤后,最终制取得19.52g柠檬酸铁铵,则柠檬酸铁铵的产率为_______ 。
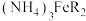 ,M=488g·mol-1]的流程如下所示:
,M=488g·mol-1]的流程如下所示: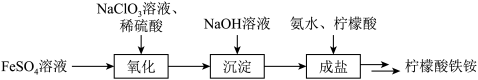
(2)欲检验FeSO4溶液是否被完全氧化,选用的试剂为_______。
| A.NaOH溶液 | B.KSCN溶液 | C.酸性KMnO4溶液 | D.新制氯水 |
(3)上述流程中,以13.90g绿矾(FeSO4·7H2O)配制FeSO4溶液,经各步骤后,最终制取得19.52g柠檬酸铁铵,则柠檬酸铁铵的产率为
您最近一年使用:0次
名校
6 . 配平方程式并标出电子转移方向及数目___________ 。
___________ ___________
___________ ___________
___________ ___________
___________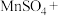 ___________
___________ ___________
___________ ___________
___________
___________
 ___________
___________ ___________
___________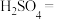 ___________
___________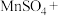 ___________
___________ ___________
___________ ___________
___________
您最近一年使用:0次
7 . 实验室用 与浓盐酸共热制备
与浓盐酸共热制备 ,反应如下:
,反应如下:
(1)该反应中被氧化的元素是___________ ,还原产物是___________ ;
(2)用单线桥标明电子转移的方向与数目___________ 。
(3)该反应中,氧化剂与还原剂的物质的量之比为___________ (前者比后者);盐酸在反应中表现出来的性质是___________ 。
(4)当生成标准状况下 时,转移的电子数目为
时,转移的电子数目为___________ ,被氧化的还原剂的物质的量为___________ 。
(5)也可以用 和浓盐酸反应,在常温下制氯气,请从化合价的角度分析,能够使用
和浓盐酸反应,在常温下制氯气,请从化合价的角度分析,能够使用 的原因:
的原因:___________ 。
(6)举例说明氯气的氧化性比硫单质强,___________ 。
 与浓盐酸共热制备
与浓盐酸共热制备 ,反应如下:
,反应如下:
(1)该反应中被氧化的元素是
(2)用单线桥标明电子转移的方向与数目
(3)该反应中,氧化剂与还原剂的物质的量之比为
(4)当生成标准状况下
 时,转移的电子数目为
时,转移的电子数目为(5)也可以用
 和浓盐酸反应,在常温下制氯气,请从化合价的角度分析,能够使用
和浓盐酸反应,在常温下制氯气,请从化合价的角度分析,能够使用 的原因:
的原因:(6)举例说明氯气的氧化性比硫单质强,
您最近一年使用:0次
8 . 下列反应中,属于氧化还原反应的化合反应是
A.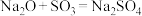 | B. |
C.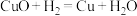 | D. |
您最近一年使用:0次
9 . 氧化还原反应的实质是___________ ,我们可以通过___________ 判断一个反应是否为氧化还原反应。
A. 氧元素的得失 B. 氢元素的得失 C. 电子的转移 D. 元素化合价的升降
A. 氧元素的得失 B. 氢元素的得失 C. 电子的转移 D. 元素化合价的升降
您最近一年使用:0次
解题方法
10 . 工业上、高温煅烧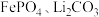 和草酸的混合物制取电池材料磷酸铁锂
和草酸的混合物制取电池材料磷酸铁锂 ,发生的反应为
,发生的反应为
1.配平上述化学方程式并标出电于转移的方向和数目___________ 。
2.一种以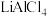 为离子导体的铝—磷酸铁锂电池,该电池放电时的工作原理如图所示。下列说法错误的是 。
为离子导体的铝—磷酸铁锂电池,该电池放电时的工作原理如图所示。下列说法错误的是 。
3.钠电池与锂离子电池工作原理相似,未来在大规模储能中有广阔的应用前景。与锂电池相比,请分析钠电池可能的优劣(各写一条) ___________ 。
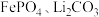 和草酸的混合物制取电池材料磷酸铁锂
和草酸的混合物制取电池材料磷酸铁锂 ,发生的反应为
,发生的反应为
1.配平上述化学方程式并标出电于转移的方向和数目
2.一种以
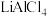 为离子导体的铝—磷酸铁锂电池,该电池放电时的工作原理如图所示。下列说法错误的是 。
为离子导体的铝—磷酸铁锂电池,该电池放电时的工作原理如图所示。下列说法错误的是 。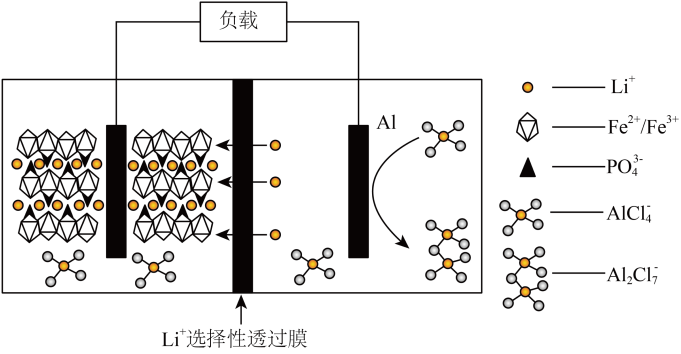
A.放电时,铝电极的电极反应为: | B.放电时, 电极做负极 电极做负极 |
C.充电时, 透过离子交换膜从左向右迁移 透过离子交换膜从左向右迁移 | D.充电时,阳极的电极反应为: |
您最近一年使用:0次



