名校
1 . 2020年突如其来的“新冠肺炎”使人们认识到日常杀菌消毒的重要性。氯气、漂白液、漂白粉都是生活中常用的含氯消毒剂。某校化学兴趣小组为研究Cl2的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的有色布条,b为湿润的有色布条。
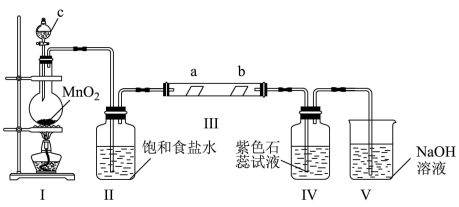
(1)装置Ⅰ中仪器c的名称是___________ ,实验室以二氧化锰和浓盐酸制备氯气的化学方程式为___________
(2)装置Ⅱ的作用是___________
(3)若产生Cl2足量,实验过程中装置Ⅳ中的实验现象___________
(4)实验结束后,该组同学在装置Ⅲ中视察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在图中装置Ⅱ与Ⅲ之间添加图中的___________ 装置(填序号)。

(5)有一种“地康法”制取氯气的反应原理如图所示:
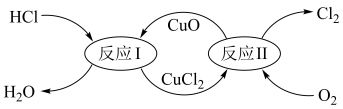
①反应Ⅰ属于___________ 反应。(填四种基本反应类型之一)
②在450℃条件下,反应Ⅱ的化学方程式为 ,请用单线桥表示该反应中电子转移的方向和数目:
,请用单线桥表示该反应中电子转移的方向和数目:___________
③工业生产中常用氨气检查输送氯气的管道是否有Cl2泄漏。若Cl2有泄漏,可以观察到有大量的白烟生成(为NH4Cl固体),同时会生成一种空气中含量最多的物质,试写出该反应的化学方程式___________
④若将Cl2通入热的烧碱溶液中,可以得到NaCl、NaClO和NaClO3的混合液。当混合液中 和ClO
和ClO 的个数比为15:2时,混合液中
的个数比为15:2时,混合液中 和ClO
和ClO 的个数比为
的个数比为___________
⑤世界卫生组织将ClO2定为高效安全灭菌消毒剂,它在食品保鲜、饮用水消毒等方面有广泛应用。消毒效率是用单位质量的消毒剂得电子数来表示的,ClO2作消毒剂时和氯气一样,还原产物均为 ,ClO2的消毒效率是氯气的
,ClO2的消毒效率是氯气的___________ 倍。(保留一位小数)

(1)装置Ⅰ中仪器c的名称是
(2)装置Ⅱ的作用是
(3)若产生Cl2足量,实验过程中装置Ⅳ中的实验现象
(4)实验结束后,该组同学在装置Ⅲ中视察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在图中装置Ⅱ与Ⅲ之间添加图中的

(5)有一种“地康法”制取氯气的反应原理如图所示:

①反应Ⅰ属于
②在450℃条件下,反应Ⅱ的化学方程式为
 ,请用单线桥表示该反应中电子转移的方向和数目:
,请用单线桥表示该反应中电子转移的方向和数目:③工业生产中常用氨气检查输送氯气的管道是否有Cl2泄漏。若Cl2有泄漏,可以观察到有大量的白烟生成(为NH4Cl固体),同时会生成一种空气中含量最多的物质,试写出该反应的化学方程式
④若将Cl2通入热的烧碱溶液中,可以得到NaCl、NaClO和NaClO3的混合液。当混合液中
 和ClO
和ClO 的个数比为15:2时,混合液中
的个数比为15:2时,混合液中 和ClO
和ClO 的个数比为
的个数比为⑤世界卫生组织将ClO2定为高效安全灭菌消毒剂,它在食品保鲜、饮用水消毒等方面有广泛应用。消毒效率是用单位质量的消毒剂得电子数来表示的,ClO2作消毒剂时和氯气一样,还原产物均为
 ,ClO2的消毒效率是氯气的
,ClO2的消毒效率是氯气的
您最近一年使用:0次
2021-11-16更新
|
311次组卷
|
2卷引用:天津市南开中学2021-2022学年高一上学期期中考试化学试题
2 . 氧化还原反应在工农业生产、日常生活中具有广泛的用途。
(1)工业干法制备高铁酸钾的第一步反应为: 。该反应中氧化产物为
。该反应中氧化产物为_______ 。
(2)已知下列三个氧化还原反应:①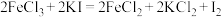 ;②
;② ;③
;③ 。若溶质中
。若溶质中 与
与 共存,为了氧化
共存,为了氧化 而
而 不被氧化,除单质外,还可用反应中的
不被氧化,除单质外,还可用反应中的_______ (从下列三个反应中选择)作氧化剂。
(3)无水情况下, 可以和
可以和 发生如下反应:_______
发生如下反应:_______ _______
_______ _______
_______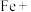 _______
_______ _______
_______ _______
_______ 。配平上述反应方程式,单线桥法标出电子转移的方向和数目
。配平上述反应方程式,单线桥法标出电子转移的方向和数目_______ ;
(4)向含有 、
、 的溶液中通入一定量的氯气,再向反应后的溶液中滴加少量的KSCN溶液,结果溶液变为红色。已知:①还原性
的溶液中通入一定量的氯气,再向反应后的溶液中滴加少量的KSCN溶液,结果溶液变为红色。已知:①还原性 ;②KSCN溶液可用于检验
;②KSCN溶液可用于检验 的存在,溶液呈红色。则下列叙述中正确的是
的存在,溶液呈红色。则下列叙述中正确的是_______ 。
①氧化性: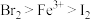
②原溶液中 一定被氧化
一定被氧化
③通入氯气后,原溶液中的 一定被氧化
一定被氧化
④不能确定通入氯气后的溶液中是否还存在
(5)下列转化中,需要加入还原剂才能实现的是_______。
(6)2020年8月初,某海外港口因硝酸铵分解引发剧烈爆炸,已知: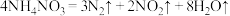 ,则该反应中被还原和被氧化的N原子数之比为
,则该反应中被还原和被氧化的N原子数之比为_______ 。
(7)用如图装置可验证 是否具有漂白性。为达到实验目的,c、d、e三处依次放入的物质为
是否具有漂白性。为达到实验目的,c、d、e三处依次放入的物质为_______ (填序号)。
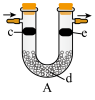
①干燥的有色布条 ②湿润的有色布条 ③浓硫酸 ④碱石灰 ⑤无水
(1)工业干法制备高铁酸钾的第一步反应为:
 。该反应中氧化产物为
。该反应中氧化产物为(2)已知下列三个氧化还原反应:①
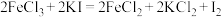 ;②
;② ;③
;③ 。若溶质中
。若溶质中 与
与 共存,为了氧化
共存,为了氧化 而
而 不被氧化,除单质外,还可用反应中的
不被氧化,除单质外,还可用反应中的(3)无水情况下,
 可以和
可以和 发生如下反应:_______
发生如下反应:_______ _______
_______ _______
_______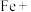 _______
_______ _______
_______ _______
_______ 。配平上述反应方程式,单线桥法标出电子转移的方向和数目
。配平上述反应方程式,单线桥法标出电子转移的方向和数目(4)向含有
 、
、 的溶液中通入一定量的氯气,再向反应后的溶液中滴加少量的KSCN溶液,结果溶液变为红色。已知:①还原性
的溶液中通入一定量的氯气,再向反应后的溶液中滴加少量的KSCN溶液,结果溶液变为红色。已知:①还原性 ;②KSCN溶液可用于检验
;②KSCN溶液可用于检验 的存在,溶液呈红色。则下列叙述中正确的是
的存在,溶液呈红色。则下列叙述中正确的是①氧化性:
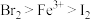
②原溶液中
 一定被氧化
一定被氧化③通入氯气后,原溶液中的
 一定被氧化
一定被氧化④不能确定通入氯气后的溶液中是否还存在

(5)下列转化中,需要加入还原剂才能实现的是_______。
A. | B. |
C. | D. |
(6)2020年8月初,某海外港口因硝酸铵分解引发剧烈爆炸,已知:
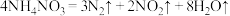 ,则该反应中被还原和被氧化的N原子数之比为
,则该反应中被还原和被氧化的N原子数之比为(7)用如图装置可验证
 是否具有漂白性。为达到实验目的,c、d、e三处依次放入的物质为
是否具有漂白性。为达到实验目的,c、d、e三处依次放入的物质为
①干燥的有色布条 ②湿润的有色布条 ③浓硫酸 ④碱石灰 ⑤无水

您最近一年使用:0次
名校
解题方法
3 . 钠、碳及它们的化合物在生产、生活中有着重要的用途。
(1)某汽车安全气囊的产气药剂主要含有NaN3、Fe2O3、KClO4、NaHCO3等物质。当汽车发生碰撞时,NaN3迅速分解产生N2和Na,同时放出大量的热。N2使气囊迅速膨胀,从而起到保护作用。
① KClO4的名称是___________ ,具有___________ (填“还原性”或“氧化性”)。
② Fe2O3可处理产生的Na,反应为6Na+Fe2O3 =3Na2O+2Fe,反应中Na作___________ (填“还原剂”或“氧化剂”)。
反应过程中氧化产物与还原产物的个数比为:___________ 。
(2)Na2O2可用于呼吸面具或潜水艇中氧气的来源。某实验小组利用下图装置探究Na2O2与CO2的反应。请回答下列问题:

①根据实验目的,虚线框中的装置所用的试剂为___________ 。
②装置C中观察到的现象是___________ ,反应的化学方程式是___________ 。
③装置A的作用是制备CO2,写出A中发生反应的化学方程式是___________ 。
(1)某汽车安全气囊的产气药剂主要含有NaN3、Fe2O3、KClO4、NaHCO3等物质。当汽车发生碰撞时,NaN3迅速分解产生N2和Na,同时放出大量的热。N2使气囊迅速膨胀,从而起到保护作用。
① KClO4的名称是
② Fe2O3可处理产生的Na,反应为6Na+Fe2O3 =3Na2O+2Fe,反应中Na作
反应过程中氧化产物与还原产物的个数比为:
(2)Na2O2可用于呼吸面具或潜水艇中氧气的来源。某实验小组利用下图装置探究Na2O2与CO2的反应。请回答下列问题:

①根据实验目的,虚线框中的装置所用的试剂为
②装置C中观察到的现象是
③装置A的作用是制备CO2,写出A中发生反应的化学方程式是
您最近一年使用:0次
2021-03-21更新
|
585次组卷
|
4卷引用:重庆市南坪中学2020-2021学年高一上学期期中考试化学试题
重庆市南坪中学2020-2021学年高一上学期期中考试化学试题黑龙江省龙西北地区八校2020-2021学年高一下学期3月联考化学试题(已下线)专题卷三 钠及其化合物(B卷)-2021-2022学年高一化学优选好题单元专题双测卷(人教版2019必修第一册)广东省顺德市李兆基中学2021-2022学年高一上学期期中考试化学试题
4 . 综合利用海水可以制备氯化铵、纯碱、金属镁等物质,其流程如下图所示:
(2)写出反应②的离子方程式_______________
(3)X溶液中的主要阳离子是Na+和___________
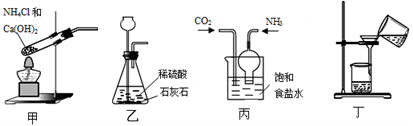
(4)已知氨气极易溶于水,实验室可用NH4Cl和Ca(OH)2固体混合加热制取。根据流程原理制取碳酸氢钠固体,下列实验装置正确且能达到实验目的的是_________
A.用装置甲制取氨气
B.用装置乙制取二氧化碳
C.用装置丙制取碳酸氢钠
D.用装置丁分离碳酸氢钠固体与母液
(5)粗盐中含有Na2SO4、MgCl2、CaCl2等可溶性杂质,为制得纯净的NaCl晶体,操作如下:
①溶解;②依次滴加过量的BaCl2溶液、NaOH溶液、Na2CO3溶液;③______________ ;④滴加适量盐酸;⑤_____________________ (请补全缺少的实验操作)
(6)检验纯碱样品中是否含NaCl,至少应选用的试剂是____________________
(7)电解熔融氯化镁制镁,得到的镁蒸气可在下列哪种气体氛围中冷却(填序号)________________
A.H2 B.CO2 C.O2 D.N2
 (1)反应①~⑤中,属于氧化还原反应的是
(1)反应①~⑤中,属于氧化还原反应的是
(2)写出反应②的离子方程式
(3)X溶液中的主要阳离子是Na+和
(4)已知氨气极易溶于水,实验室可用NH4Cl和Ca(OH)2固体混合加热制取。根据流程原理制取碳酸氢钠固体,下列实验装置正确且能达到实验目的的是
A.用装置甲制取氨气
B.用装置乙制取二氧化碳
C.用装置丙制取碳酸氢钠
D.用装置丁分离碳酸氢钠固体与母液
(5)粗盐中含有Na2SO4、MgCl2、CaCl2等可溶性杂质,为制得纯净的NaCl晶体,操作如下:
①溶解;②依次滴加过量的BaCl2溶液、NaOH溶液、Na2CO3溶液;③
(6)检验纯碱样品中是否含NaCl,至少应选用的试剂是
(7)电解熔融氯化镁制镁,得到的镁蒸气可在下列哪种气体氛围中冷却(填序号)
A.H2 B.CO2 C.O2 D.N2
您最近一年使用:0次
名校
5 . 铁及其化合物在生产生活中具有重要的应用,高铁酸钾 是一种高效水处理剂,紫色固体.已知
是一种高效水处理剂,紫色固体.已知 具有下列性质:①可溶于水,溶液为紫色,微溶于浓
具有下列性质:①可溶于水,溶液为紫色,微溶于浓 溶液;②在
溶液;②在 、强碱性溶液中比较稳定.某实验小组制备并探究
、强碱性溶液中比较稳定.某实验小组制备并探究 性质,回答下列问题:
性质,回答下列问题:
(1)制备 (夹持装置略):
(夹持装置略):
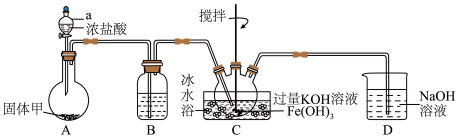
①A为氯气发生装置,其中仪器a的名称是______ ,固体甲的化学式为______ ,浓盐酸在该反应中表现的性质为______ ;将A中混合气体通过装置B可除去杂质,以免影响实验,B中的试剂是______ ;
②C为制备 的装置,采用冰水浴的原因是
的装置,采用冰水浴的原因是______ , 与
与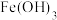 在碱性环境中反应生成
在碱性环境中反应生成 ,该氧化还原反应中氧化剂与还原剂的物质的量之比为
,该氧化还原反应中氧化剂与还原剂的物质的量之比为______ ;
③D为尾气处理装置,发生反应的离子方程式为______ 。
(2)探究 的性质:
的性质:
根据实验1和2的现象, 在酸性条件下发生反应,配平下列反应,用双线桥表示转移电子的方向和数目:
在酸性条件下发生反应,配平下列反应,用双线桥表示转移电子的方向和数目:______ 。
__ ___
___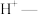 ___
___ ___
___ ___
___
 是一种高效水处理剂,紫色固体.已知
是一种高效水处理剂,紫色固体.已知 具有下列性质:①可溶于水,溶液为紫色,微溶于浓
具有下列性质:①可溶于水,溶液为紫色,微溶于浓 溶液;②在
溶液;②在 、强碱性溶液中比较稳定.某实验小组制备并探究
、强碱性溶液中比较稳定.某实验小组制备并探究 性质,回答下列问题:
性质,回答下列问题:(1)制备
 (夹持装置略):
(夹持装置略):
①A为氯气发生装置,其中仪器a的名称是
②C为制备
 的装置,采用冰水浴的原因是
的装置,采用冰水浴的原因是 与
与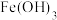 在碱性环境中反应生成
在碱性环境中反应生成 ,该氧化还原反应中氧化剂与还原剂的物质的量之比为
,该氧化还原反应中氧化剂与还原剂的物质的量之比为③D为尾气处理装置,发生反应的离子方程式为
(2)探究
 的性质:
的性质:| 实验1 | 取少量C中紫色溶液,加入过量稀硫酸,迅速产生大量气体,该气体能使带火星的木条复燃 |
| 实验2 | 取实验1中的溶液,滴加 溶液至过量,溶液呈红色. 溶液至过量,溶液呈红色. |
 在酸性条件下发生反应,配平下列反应,用双线桥表示转移电子的方向和数目:
在酸性条件下发生反应,配平下列反应,用双线桥表示转移电子的方向和数目:__
 ___
___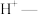 ___
___ ___
___ ___
___
您最近一年使用:0次
名校
解题方法
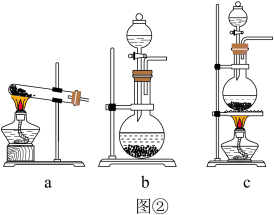
6 . 氯及其化合物在工业生产生活中有很重要的作用。图①中为实验室制取氧气及性质验证的装置图。

(1)盛放浓盐酸的仪器名称:___________ ;利用装置A制备Cl2,写出该反应的离子方程式:___________
(2)装置B的作用:___________ ;装置C中的试剂:___________
(3)若图①装置中a为干燥的有色布条,b为湿润的有色布条,可观察到的实验现象:___________ ;通过实验现象说明什么结论:___________ ;
(4)写出装置D中发生反应的离子方程式:___________ ;
(5)实验室也可用KMnO4和浓盐酸制取氯气,反应如下:2KMnO4+16HCl(浓)=2MnCl2+2KCl+5Cl2↑+8H2O。该反应中被氧化的HCl与起酸性的HCl物质的量比为___________ ;用单线桥标出电子转移的方向和数目:___________ ,图②作为最佳发生装置是___________ 。

(1)盛放浓盐酸的仪器名称:
(2)装置B的作用:
(3)若图①装置中a为干燥的有色布条,b为湿润的有色布条,可观察到的实验现象:
(4)写出装置D中发生反应的离子方程式:
(5)实验室也可用KMnO4和浓盐酸制取氯气,反应如下:2KMnO4+16HCl(浓)=2MnCl2+2KCl+5Cl2↑+8H2O。该反应中被氧化的HCl与起酸性的HCl物质的量比为

您最近一年使用:0次
2024-01-09更新
|
148次组卷
|
4卷引用:山东省聊城市2023-2024学年高一上学期11月期中化学试题
名校
解题方法
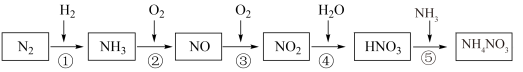
7 . 氮元素及其化合物的转化关系如图所示:___________ ,写出 的电子式
的电子式___________ 。
(2)浓、稀 的性质既相似又有差别,写出足量的铁与稀硝酸反应的离子方程式:
的性质既相似又有差别,写出足量的铁与稀硝酸反应的离子方程式:___________ 。
(3)氮氧化物 是大气污染物之一,处理
是大气污染物之一,处理 对于环境保护具有重要的意义。在一定条件下
对于环境保护具有重要的意义。在一定条件下 可将
可将 还原。甲同学在实验室对该反应进行了探究。实验设计如图(部分夹持装置省略)。
还原。甲同学在实验室对该反应进行了探究。实验设计如图(部分夹持装置省略)。 ,反应的化学方程式为
,反应的化学方程式为___________ ;装置B内的试剂是___________ 。
②在装置 中
中 和
和 充分反应,生成两种对环境友好的物质,该反应中
充分反应,生成两种对环境友好的物质,该反应中  和
和 的物质的量之比为
的物质的量之比为___________ 。
③工厂里常采用 溶液吸收
溶液吸收 的混合气体,使其转化为化工产品
的混合气体,使其转化为化工产品 ,试写出其化学方程式:
,试写出其化学方程式:___________ 。
④用不同浓度的 溶液吸收
溶液吸收 含量不同的尾气,关系如图:(
含量不同的尾气,关系如图:( 表示尾气里
表示尾气里 中
中 的含量)
的含量) 含量越大,氮氧化物的吸收率越大,当
含量越大,氮氧化物的吸收率越大,当 小于
小于 时,加入
时,加入  能提升氮氧化物的吸收率,原因是
能提升氮氧化物的吸收率,原因是___________ 。
(4) 是农业生产中常用的一种氮肥。实验室中检验某种化肥是铵态氮肥的方法是:
是农业生产中常用的一种氮肥。实验室中检验某种化肥是铵态氮肥的方法是:___________ (写出操作步骤、现象和结论)。
 的电子式
的电子式(2)浓、稀
 的性质既相似又有差别,写出足量的铁与稀硝酸反应的离子方程式:
的性质既相似又有差别,写出足量的铁与稀硝酸反应的离子方程式:(3)氮氧化物
 是大气污染物之一,处理
是大气污染物之一,处理 对于环境保护具有重要的意义。在一定条件下
对于环境保护具有重要的意义。在一定条件下 可将
可将 还原。甲同学在实验室对该反应进行了探究。实验设计如图(部分夹持装置省略)。
还原。甲同学在实验室对该反应进行了探究。实验设计如图(部分夹持装置省略)。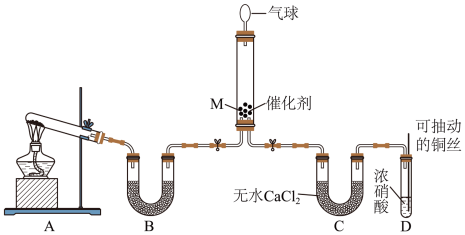
 ,反应的化学方程式为
,反应的化学方程式为②在装置
 中
中 和
和 充分反应,生成两种对环境友好的物质,该反应中
充分反应,生成两种对环境友好的物质,该反应中  和
和 的物质的量之比为
的物质的量之比为③工厂里常采用
 溶液吸收
溶液吸收 的混合气体,使其转化为化工产品
的混合气体,使其转化为化工产品 ,试写出其化学方程式:
,试写出其化学方程式:④用不同浓度的
 溶液吸收
溶液吸收 含量不同的尾气,关系如图:(
含量不同的尾气,关系如图:( 表示尾气里
表示尾气里 中
中 的含量)
的含量)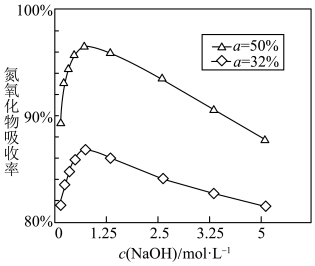
 含量越大,氮氧化物的吸收率越大,当
含量越大,氮氧化物的吸收率越大,当 小于
小于 时,加入
时,加入  能提升氮氧化物的吸收率,原因是
能提升氮氧化物的吸收率,原因是(4)
 是农业生产中常用的一种氮肥。实验室中检验某种化肥是铵态氮肥的方法是:
是农业生产中常用的一种氮肥。实验室中检验某种化肥是铵态氮肥的方法是:
您最近一年使用:0次
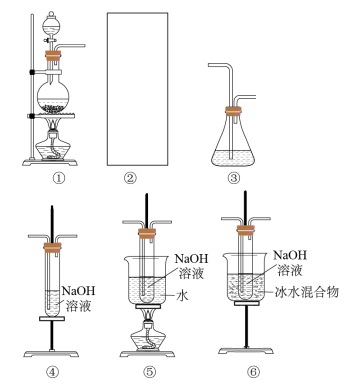
8 . 某研究性学习小组欲利用下列装置制取少量次氯酸钠,并进一步探究市场所售的84消毒液成分性质。
①中利用反应MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O制取氯气。
MnCl2+Cl2↑+2H2O制取氯气。
相关资料:已知制备84消毒液的反应属于放热反应,温度稍高时便发生副反应:3Cl2+6NaOH=NaClO3+5NaCl+3H2O。
(1)请在上图装置A、B、C中选择一个合适的装置放在②处制消毒液:___________ 。
(2)请写出②中制备消毒液的离子方程式___________ 。
(3)请用双线桥法标出下方副反应化学方程式的电子转移方向和数目:___________ 3Cl2+6NaOH=NaClO3+5NaCl+3H2O
(4)当收集了约448mL Cl2(标准状况下)时,反应消耗的HCl的物质的量为___________ mol。
(5)研究小组中部分同学想继续探究市场所售的84消毒液成分与性质,分别做了以下实验: 需将表格填写完整
需将表格填写完整
①中利用反应MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O制取氯气。
MnCl2+Cl2↑+2H2O制取氯气。
相关资料:已知制备84消毒液的反应属于放热反应,温度稍高时便发生副反应:3Cl2+6NaOH=NaClO3+5NaCl+3H2O。
(1)请在上图装置A、B、C中选择一个合适的装置放在②处制消毒液:
(2)请写出②中制备消毒液的离子方程式
(3)请用双线桥法标出下方副反应化学方程式的电子转移方向和数目:
(4)当收集了约448mL Cl2(标准状况下)时,反应消耗的HCl的物质的量为
(5)研究小组中部分同学想继续探究市场所售的84消毒液成分与性质,分别做了以下实验:
 需将表格填写完整
需将表格填写完整
| 实验操作 | 预期现象 | 实际现象 | 结论及解释 |
| 1.向少量84消毒液中滴入酚酞试液 | 变红 | 先变红,后慢慢褪色 | ① |
| 2.向少量84消毒液中加入FeCl3溶液 | 有红褐色沉淀产生 | 有红褐色沉淀产生,同时有气泡生成 | 产生了Fe(OH)3沉淀,同时可能产生了CO2气体 |
| 3.向少量84消毒液中加入AgNO3溶液,最后加入稀硝酸 | 有白色沉淀产生 | 有白色沉淀产生,加入稀硝酸,沉淀部分溶解,且有气泡产生 | ② |
您最近一年使用:0次
9 .  又称百毒净,可用于水的净化和纸张、纺织品的漂白等。用如图所示装置(夹持装置和加热装置省略)制备
又称百毒净,可用于水的净化和纸张、纺织品的漂白等。用如图所示装置(夹持装置和加热装置省略)制备 并探究
并探究 的某些性质,已知
的某些性质,已知 浓度较大时易分解爆炸。
浓度较大时易分解爆炸。
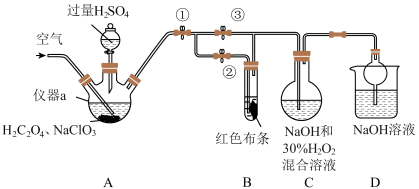
回答下列问题:
(1)通入空气的目的为_______ 。
(2)补充并配平实验中制备 的化学方程式:
的化学方程式:_______ 。
_______ _______
_______ _______
_______ _______
_______ _______
_______ _______+_______
_______+_______
工业上也可用 氧化
氧化 溶液制取
溶液制取 ,写出该反应的离子方程式,并用单线桥法标出电子转移的方向和数目:
,写出该反应的离子方程式,并用单线桥法标出电子转移的方向和数目:_______ 。
(3)关闭止水夹②,打开止水夹①③,通入空气一段时间后,装置C中生成了 和气体,反应中
和气体,反应中 表现出
表现出_______ (填“氧化”或“还原”)性;若关闭止水夹③,打开止水夹②,B中可观察到的现象为_______ 。
(4)D装置的作用是_______ 、_______ 。
(5) 和
和 在水处理过程中分别被还原为
在水处理过程中分别被还原为 和
和 。如果以单位质量的氧化剂所得到的电子数来表示消毒效率,那么
。如果以单位质量的氧化剂所得到的电子数来表示消毒效率,那么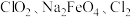 三种消毒杀菌剂的消毒效率由高到低的顺序是
三种消毒杀菌剂的消毒效率由高到低的顺序是_______ (填化学式)。
 又称百毒净,可用于水的净化和纸张、纺织品的漂白等。用如图所示装置(夹持装置和加热装置省略)制备
又称百毒净,可用于水的净化和纸张、纺织品的漂白等。用如图所示装置(夹持装置和加热装置省略)制备 并探究
并探究 的某些性质,已知
的某些性质,已知 浓度较大时易分解爆炸。
浓度较大时易分解爆炸。
回答下列问题:
(1)通入空气的目的为
(2)补充并配平实验中制备
 的化学方程式:
的化学方程式:_______
 _______
_______ _______
_______ _______
_______ _______
_______ _______+_______
_______+_______
工业上也可用
 氧化
氧化 溶液制取
溶液制取 ,写出该反应的离子方程式,并用单线桥法标出电子转移的方向和数目:
,写出该反应的离子方程式,并用单线桥法标出电子转移的方向和数目:(3)关闭止水夹②,打开止水夹①③,通入空气一段时间后,装置C中生成了
 和气体,反应中
和气体,反应中 表现出
表现出(4)D装置的作用是
(5)
 和
和 在水处理过程中分别被还原为
在水处理过程中分别被还原为 和
和 。如果以单位质量的氧化剂所得到的电子数来表示消毒效率,那么
。如果以单位质量的氧化剂所得到的电子数来表示消毒效率,那么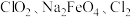 三种消毒杀菌剂的消毒效率由高到低的顺序是
三种消毒杀菌剂的消毒效率由高到低的顺序是
您最近一年使用:0次
名校
10 . 制备物质是化学工作者的重要任务之一,实验室用如图装置制备并收集干燥、纯净的 。
。
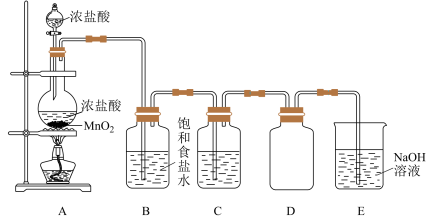
(1)装置A中发生反应的离子方程式是_______ ,反应中盐酸体现的性质有_______ 。
(2)装置B的作用是_______ 。
(3)装置C中盛放的物质是_______ 。
(4)装置D用于收集 ,请将装置D中的导气管在装置图上补充完整
,请将装置D中的导气管在装置图上补充完整_______ (→表示气流方向)。
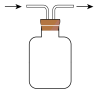
(5)装置中有一明显缺陷请指出_______
(6)写出工业上用氯气和石灰乳制取漂白粉的化学反应方程式:_______ 。
某化学兴趣小组欲在实验室探究氯气的氧化性并模拟工业制取漂白粉,设计如图装置进行实验:
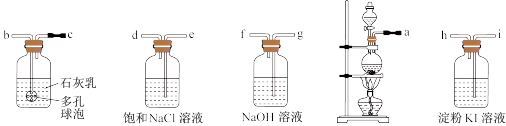
(7)装置的连接顺序为_______ (填接口字母)
(8)淀粉 溶液中的现象为
溶液中的现象为_______ 。
(9)多孔球泡的作用是_______ 。
(10)工业制取漂白粉为什么选用石灰乳而不是澄清石灰水_______ 。
 。
。
(1)装置A中发生反应的离子方程式是
(2)装置B的作用是
(3)装置C中盛放的物质是
(4)装置D用于收集
 ,请将装置D中的导气管在装置图上补充完整
,请将装置D中的导气管在装置图上补充完整
(5)装置中有一明显缺陷请指出
(6)写出工业上用氯气和石灰乳制取漂白粉的化学反应方程式:
某化学兴趣小组欲在实验室探究氯气的氧化性并模拟工业制取漂白粉,设计如图装置进行实验:

(7)装置的连接顺序为
(8)淀粉
 溶液中的现象为
溶液中的现象为(9)多孔球泡的作用是
(10)工业制取漂白粉为什么选用石灰乳而不是澄清石灰水
您最近一年使用:0次



