23-24高一上·福建南平·期末
解题方法
1 . 物质的类别和元素的化合价是研究物质性质的两个重要角度。下图是部分含氮和含氯物质的价类二维图,回答下列问题:
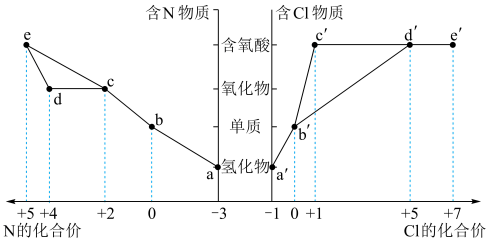
(1)b的化学式为___________ 。
(2)b′能溶于水还能与水反应,其水溶液显___________ 。(填“酸性、碱性或中性”)
(3)将a和a′两种气体混合产生的现象是___________ 。
(4)实验室制取b′气体用浓a′溶液滴入 中并加热,其反应的离子方程式为
中并加热,其反应的离子方程式为___________ 。
(5)工业上制备
___________ (填“能”或“不能”)通过a→b→c→e流程实现。
(6)由上述两种元素组成的液态化合物 ,遇水可生成化合物a和c′,该反应的化学方程式为
,遇水可生成化合物a和c′,该反应的化学方程式为___________ 。

(1)b的化学式为
(2)b′能溶于水还能与水反应,其水溶液显
(3)将a和a′两种气体混合产生的现象是
(4)实验室制取b′气体用浓a′溶液滴入
 中并加热,其反应的离子方程式为
中并加热,其反应的离子方程式为(5)工业上制备

(6)由上述两种元素组成的液态化合物
 ,遇水可生成化合物a和c′,该反应的化学方程式为
,遇水可生成化合物a和c′,该反应的化学方程式为
您最近一年使用:0次
23-24高一上·福建莆田·阶段练习
名校
2 . 回答下列问题:
(1)从海水中得到的粗盐中常含 、
、 、
、 等杂质离子,可依次加入
等杂质离子,可依次加入_______ 、_______ 、_______ 、稀盐酸来进行提纯。加入适量盐酸的目的是_______ 。
(2)用上述方法得到氯化钠,配制氯化钠饱和溶液进行如下图所示电解实验。
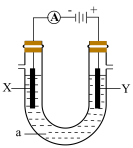
①写出该电解反应的化学方程式_______ 。
②简述检测Y极附近产生的气体的实验方案:_______
(3)下列方法可用于海水淡化的是_______ (填字母)。
A.蒸馏法 B.萃取法 C.过滤法
(4)①“84”消毒液是生活中常见的消毒剂, 与
与 溶液反应制取“84”消毒液的化学方程式为
溶液反应制取“84”消毒液的化学方程式为_______ 。
②“84”消毒液的稀溶液在浸泡餐具过程中,因吸收空气中 使消毒杀菌能力增强,产物中有小苏打,请用化学方程式说明原因:
使消毒杀菌能力增强,产物中有小苏打,请用化学方程式说明原因:_______ 。
(5)目前很多自来水厂使用 来消毒、杀菌。工业制取
来消毒、杀菌。工业制取 的反应:
的反应: ,请用双线桥表示反应中电子转移情况
,请用双线桥表示反应中电子转移情况_______ 。
(6)物质的制备是化学学科的基本研究方向。
①室温下,将氨水和 溶液混合,可制得
溶液混合,可制得 溶液。离子方程式为
溶液。离子方程式为_______ 。
②软锰矿(主要成分 )的水悬浊液可吸收烟气中的
)的水悬浊液可吸收烟气中的 并同时制备
并同时制备 。制备
。制备 反应的化学方程式为
反应的化学方程式为_______ 。
(1)从海水中得到的粗盐中常含
 、
、 、
、 等杂质离子,可依次加入
等杂质离子,可依次加入(2)用上述方法得到氯化钠,配制氯化钠饱和溶液进行如下图所示电解实验。

①写出该电解反应的化学方程式
②简述检测Y极附近产生的气体的实验方案:
(3)下列方法可用于海水淡化的是
A.蒸馏法 B.萃取法 C.过滤法
(4)①“84”消毒液是生活中常见的消毒剂,
 与
与 溶液反应制取“84”消毒液的化学方程式为
溶液反应制取“84”消毒液的化学方程式为②“84”消毒液的稀溶液在浸泡餐具过程中,因吸收空气中
 使消毒杀菌能力增强,产物中有小苏打,请用化学方程式说明原因:
使消毒杀菌能力增强,产物中有小苏打,请用化学方程式说明原因:(5)目前很多自来水厂使用
 来消毒、杀菌。工业制取
来消毒、杀菌。工业制取 的反应:
的反应: ,请用双线桥表示反应中电子转移情况
,请用双线桥表示反应中电子转移情况(6)物质的制备是化学学科的基本研究方向。
①室温下,将氨水和
 溶液混合,可制得
溶液混合,可制得 溶液。离子方程式为
溶液。离子方程式为②软锰矿(主要成分
 )的水悬浊液可吸收烟气中的
)的水悬浊液可吸收烟气中的 并同时制备
并同时制备 。制备
。制备 反应的化学方程式为
反应的化学方程式为
您最近一年使用:0次
3 . 在煤中加入适量生石灰,可以大大减少煤燃烧时SO2的排放,请你写出涉及反应的化学方程式_______ 。
您最近一年使用:0次
4 . 浓硝酸可以氧化非金属单质,如加热条件下可将C氧化为CO2,同时生成红棕色气体,反应的化学方程式为________________________ ,体现浓硝酸的________ 性。
您最近一年使用:0次
5 . 请根据条件书写画出方程式:
(1)银首饰在空气中容易发黄变黑,原因是与空气中的H2S和O2反应生成黑色的Ag2S,请写出该反应的化学方程式:___________ 。
(2)二氧化氯(ClO2)是一种在水处理等方面有广泛应用的高效安全消毒剂。可以用NaClO3、H2O2和H2SO4反应制备ClO2。写出该制备反应的化学方程式:___________ 。
(3)人体血红蛋白分子中含有Fe2+,正是这些Fe2+使血红蛋白分子具有载氧功能。亚硝酸钠(NaNO2)可将人体血红蛋白中的Fe2+转化为Fe3+,而自身被还原为+2价氧化物,试写出该反应的离子方程式:___________ 。
(1)银首饰在空气中容易发黄变黑,原因是与空气中的H2S和O2反应生成黑色的Ag2S,请写出该反应的化学方程式:
(2)二氧化氯(ClO2)是一种在水处理等方面有广泛应用的高效安全消毒剂。可以用NaClO3、H2O2和H2SO4反应制备ClO2。写出该制备反应的化学方程式:
(3)人体血红蛋白分子中含有Fe2+,正是这些Fe2+使血红蛋白分子具有载氧功能。亚硝酸钠(NaNO2)可将人体血红蛋白中的Fe2+转化为Fe3+,而自身被还原为+2价氧化物,试写出该反应的离子方程式:
您最近一年使用:0次
22-23高二上·上海·期末
名校
6 . 实验室常用如下装置制取溴乙烷。在圆底烧瓶中加入溴化钠、浓H2SO4、乙醇和适量的水,加热可收集到溴乙烷。所涉及的有关物质的物理性质见下表:

(1)写出用此法制备溴乙烷的化学方程式:
① NaBr + H2SO4 NaHSO4 + HBr;
NaHSO4 + HBr;
②_______ 。
(2)浓H2SO4在本实验中的作用是_______ ,其用量(物质的量)应_______ (填“大”“小”或“等”)于NaBr的用量。
(3)反应物中加入适量水,除了溶解NaBr使反应物接触更充分外,还可以_______ (任写一条)。
(4)下列最适宜作为溴乙烷收集装置的是_______ (选填编号)。
(5)制得的粗溴乙烷中会含有少量杂质Br2而呈黄色,可先用NaHSO3溶液洗涤,再水洗干燥后蒸馏。洗涤过程用到的主要玻璃仪器是_______ 。完成NaHSO3溶液洗涤时发生反应的离子方程式并标明电子转移方向和数目:_______ 。□HSO + □Br2 + □_______ → □SO
+ □Br2 + □_______ → □SO + □Br- + □H+
+ □Br- + □H+
能否改用氢氧化钠溶液洗涤粗溴乙烷?_______ (填“可以”或“不可以”),原因是_______ 。

| 乙醇 | 溴乙烷 | |
| 沸点(℃) | 78 | 38.4 |
| 密度(g/cm3) | 0.79 | 1.45 |
| 水溶性 | 互溶 | 不溶 |
① NaBr + H2SO4
 NaHSO4 + HBr;
NaHSO4 + HBr;②
(2)浓H2SO4在本实验中的作用是
(3)反应物中加入适量水,除了溶解NaBr使反应物接触更充分外,还可以
(4)下列最适宜作为溴乙烷收集装置的是
 |  |  |  |
| a | b | c | d |
 + □Br2 + □_______ → □SO
+ □Br2 + □_______ → □SO + □Br- + □H+
+ □Br- + □H+能否改用氢氧化钠溶液洗涤粗溴乙烷?
您最近一年使用:0次
7 . 某种煤气的主要成分是CO、 。
。
(1)分别写出该煤气和天然气在空气中燃烧的化学方程式_______ 。
(2)把一套以煤气为燃料的灶具改为以天然气为燃料的灶具时,应对空气和燃气的进气量做怎样的调整_______ ?
 。
。(1)分别写出该煤气和天然气在空气中燃烧的化学方程式
(2)把一套以煤气为燃料的灶具改为以天然气为燃料的灶具时,应对空气和燃气的进气量做怎样的调整
您最近一年使用:0次
解题方法
8 . 向氯化铁溶液中通入硫化氢气体(硫化氢的水溶液称作氢硫酸,是一种弱酸),发现溶液变浑浊。试写出发生反应的离子方程式_______ 。
您最近一年使用:0次
9 . 油画的白色颜料中含有 ,久置后会变成
,久置后会变成 而使油画变黑,如果用双氧水(
而使油画变黑,如果用双氧水( )擦拭则可恢复原貌。试写出用双氧水擦拭所发生反应的化学方程式
)擦拭则可恢复原貌。试写出用双氧水擦拭所发生反应的化学方程式____ 。
 ,久置后会变成
,久置后会变成 而使油画变黑,如果用双氧水(
而使油画变黑,如果用双氧水( )擦拭则可恢复原貌。试写出用双氧水擦拭所发生反应的化学方程式
)擦拭则可恢复原貌。试写出用双氧水擦拭所发生反应的化学方程式
您最近一年使用:0次
2022-11-24更新
|
277次组卷
|
2卷引用:苏教2020版化学必修第一册专题4 硫与环境保护 第二单元 硫及其化合物的相互转化课后习题
解题方法
10 . 以下是以铜和硫酸为原料制备硫酸铜的两种方法,请写出下列反应的化学方程式,比较这两种方法的优劣并说明理由_______ 。
①铜与浓硫酸反应直接生成硫酸铜。②铜与稀硫酸的混合物中通入氧气,反应生成硫酸铜。
①铜与浓硫酸反应直接生成硫酸铜。②铜与稀硫酸的混合物中通入氧气,反应生成硫酸铜。
您最近一年使用:0次



