名校
解题方法
1 . 填写下列空白:
(1)工业上湿法制备高铁酸钾( )的反应体系中有六种微粒:
)的反应体系中有六种微粒: 、
、 、
、 、
、 、
、 、
、 。写出并配平该反应的离子方程式
。写出并配平该反应的离子方程式___________ ;若反应过程中转移了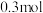 电子,则还原产物的物质的量为
电子,则还原产物的物质的量为___________  。
。
(2)一定条件下,下列物质可以通过化合反应制得的有(写序号)___________ 。
①小苏打 ②硫酸铝 ③氯化亚铁 ④磁性氧化铁 ⑤铜绿(碱式碳酸铜) ⑥氢氧化铁
(3)向一定量的 的混合物中加入
的混合物中加入 的盐酸,恰好使混合物完全溶解,放出
的盐酸,恰好使混合物完全溶解,放出 (标准状况)的气体,在所得溶液中加入
(标准状况)的气体,在所得溶液中加入 溶液无血红色出现。若用足量的
溶液无血红色出现。若用足量的 在高温下还原相同质量的此混合物,能得到铁的质量是
在高温下还原相同质量的此混合物,能得到铁的质量是___________ g。
(4)将 铁粉与含有
铁粉与含有 的
的 溶液完全反应,铁粉全部溶解,并得到
溶液完全反应,铁粉全部溶解,并得到 铜,则参加反应的
铜,则参加反应的 与
与 的物质的量之比为
的物质的量之比为___________ 。
(5)等质量的铝分别与 浓度均为
浓度均为 的盐酸和氢氧化钠溶液反应,生成气体体积比为
的盐酸和氢氧化钠溶液反应,生成气体体积比为 ,铝与氢氧化钠溶液反应的离子方程式:
,铝与氢氧化钠溶液反应的离子方程式:___________ ;铝的质量为___________ g。
(6)将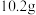 镁铝合金置于
镁铝合金置于 的盐酸中充分反应,无金属剩余,向反应后的溶液中加入
的盐酸中充分反应,无金属剩余,向反应后的溶液中加入 烧碱溶液,沉淀达到最大值,加入的烧碱的物质的量浓度为
烧碱溶液,沉淀达到最大值,加入的烧碱的物质的量浓度为___________  。
。
(1)工业上湿法制备高铁酸钾(
 )的反应体系中有六种微粒:
)的反应体系中有六种微粒: 、
、 、
、 、
、 、
、 、
、 。写出并配平该反应的离子方程式
。写出并配平该反应的离子方程式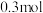 电子,则还原产物的物质的量为
电子,则还原产物的物质的量为 。
。(2)一定条件下,下列物质可以通过化合反应制得的有(写序号)
①小苏打 ②硫酸铝 ③氯化亚铁 ④磁性氧化铁 ⑤铜绿(碱式碳酸铜) ⑥氢氧化铁
(3)向一定量的
 的混合物中加入
的混合物中加入 的盐酸,恰好使混合物完全溶解,放出
的盐酸,恰好使混合物完全溶解,放出 (标准状况)的气体,在所得溶液中加入
(标准状况)的气体,在所得溶液中加入 溶液无血红色出现。若用足量的
溶液无血红色出现。若用足量的 在高温下还原相同质量的此混合物,能得到铁的质量是
在高温下还原相同质量的此混合物,能得到铁的质量是(4)将
 铁粉与含有
铁粉与含有 的
的 溶液完全反应,铁粉全部溶解,并得到
溶液完全反应,铁粉全部溶解,并得到 铜,则参加反应的
铜,则参加反应的 与
与 的物质的量之比为
的物质的量之比为(5)等质量的铝分别与
 浓度均为
浓度均为 的盐酸和氢氧化钠溶液反应,生成气体体积比为
的盐酸和氢氧化钠溶液反应,生成气体体积比为 ,铝与氢氧化钠溶液反应的离子方程式:
,铝与氢氧化钠溶液反应的离子方程式:(6)将
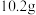 镁铝合金置于
镁铝合金置于 的盐酸中充分反应,无金属剩余,向反应后的溶液中加入
的盐酸中充分反应,无金属剩余,向反应后的溶液中加入 烧碱溶液,沉淀达到最大值,加入的烧碱的物质的量浓度为
烧碱溶液,沉淀达到最大值,加入的烧碱的物质的量浓度为 。
。
您最近一年使用:0次
名校
解题方法
2 . 计算
(1)已知酸性条件下, 可将
可将 还原为
还原为 。将标准状况下
。将标准状况下 的
的 气体通入足量酸性
气体通入足量酸性 溶液中,
溶液中,
①写出该反应的离子方程式______ 。
②被还原的 的质量为
的质量为______ 。
(2)为了检验某含有 杂质的
杂质的 样品的纯度,现将
样品的纯度,现将 样品充分加热,当固体质量不再变化时,再次称量固体质量为
样品充分加热,当固体质量不再变化时,再次称量固体质量为 ,则该样品的纯度(质量分数)为
,则该样品的纯度(质量分数)为______ (用含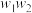 的代数式来表示)。
的代数式来表示)。
(3)有一块表面氧化成氧化钠的金属钠,总质量为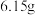 ,投入到足量水中,待充分反应后收集到氢气
,投入到足量水中,待充分反应后收集到氢气 (标准状况下),求未被氧化前金属钠质量是多少?写出计算过程
(标准状况下),求未被氧化前金属钠质量是多少?写出计算过程_____ 。
(1)已知酸性条件下,
 可将
可将 还原为
还原为 。将标准状况下
。将标准状况下 的
的 气体通入足量酸性
气体通入足量酸性 溶液中,
溶液中,①写出该反应的离子方程式
②被还原的
 的质量为
的质量为(2)为了检验某含有
 杂质的
杂质的 样品的纯度,现将
样品的纯度,现将 样品充分加热,当固体质量不再变化时,再次称量固体质量为
样品充分加热,当固体质量不再变化时,再次称量固体质量为 ,则该样品的纯度(质量分数)为
,则该样品的纯度(质量分数)为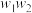 的代数式来表示)。
的代数式来表示)。(3)有一块表面氧化成氧化钠的金属钠,总质量为
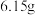 ,投入到足量水中,待充分反应后收集到氢气
,投入到足量水中,待充分反应后收集到氢气 (标准状况下),求未被氧化前金属钠质量是多少?写出计算过程
(标准状况下),求未被氧化前金属钠质量是多少?写出计算过程
您最近一年使用:0次
2023高三·全国·专题练习
3 . 硒和碲的单质是重要的高新技术材料。一种以含贵重金属的“酸泥”(含Se、Te、Ag、Pb、Cu等单质)为原料制备硒和碲的工艺流程如图所示。

要制取395g粗硒(质量分数为80%),理论上至少应通入标准状况下的SO2的体积为_______ L。

要制取395g粗硒(质量分数为80%),理论上至少应通入标准状况下的SO2的体积为
您最近一年使用:0次
解题方法
4 . 硅酸盐材料具有硬度高、难溶于水、耐高温等特点。硅酸盐中常含有Al、K等元素,如钾长石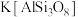 和钠长石
和钠长石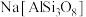 等。回答下列问题:
等。回答下列问题:
(1)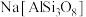 用氧化物形式表示为
用氧化物形式表示为_______ 。
(2)我国科学家发现在200℃熔盐体系中,采用金属Al还原钾长石等制备纳米硅材料的方法,将该材料应用于锂离子电池负极材料,展示出优异的电化学性能。配平下列方程式:_______ 。
______Al+______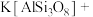 ______
______ →______Si+_____AlOCl+_____
→______Si+_____AlOCl+_____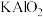 。
。
(3)将钾长石或钠长石用足量稀盐酸处理后,所得固体为_______ (填化学式)。
(4)将一定质量的铝粉和铁粉的混合物加入到一定量很稀的硝酸溶液中,充分反应,反应过程中无气体放出。向反应结束后的溶液中,逐滴加入5mol∙L-1的NaOH溶液,所加NaOH溶液的体积与产生沉淀的物质的量(n)关系如图所示:
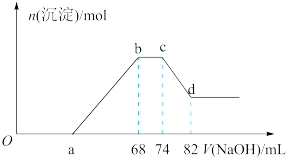
①根据关系图,写出Fe与稀硝酸反应的离子方程式:_______ 。
②样品中铝粉和铁粉的物质的量之比为_______ 。
③a点对应NaOH溶液的体积为_______ 。
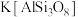 和钠长石
和钠长石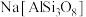 等。回答下列问题:
等。回答下列问题:(1)
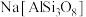 用氧化物形式表示为
用氧化物形式表示为(2)我国科学家发现在200℃熔盐体系中,采用金属Al还原钾长石等制备纳米硅材料的方法,将该材料应用于锂离子电池负极材料,展示出优异的电化学性能。配平下列方程式:
______Al+______
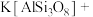 ______
______ →______Si+_____AlOCl+_____
→______Si+_____AlOCl+_____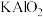 。
。(3)将钾长石或钠长石用足量稀盐酸处理后,所得固体为
(4)将一定质量的铝粉和铁粉的混合物加入到一定量很稀的硝酸溶液中,充分反应,反应过程中无气体放出。向反应结束后的溶液中,逐滴加入5mol∙L-1的NaOH溶液,所加NaOH溶液的体积与产生沉淀的物质的量(n)关系如图所示:

①根据关系图,写出Fe与稀硝酸反应的离子方程式:
②样品中铝粉和铁粉的物质的量之比为
③a点对应NaOH溶液的体积为
您最近一年使用:0次
5 . 把密度为1.6g/ cm3的液态S2Cl2 10mL溶于石油醚(一种溶剂), 得到100mL溶液,把它慢慢加入50 mL3.2mol/L的SO2水溶液中,振荡使之充分反应,当加入的S2Cl2溶液为67.5mL时,恰好反应完全。生成物用含0.32mol KOH的KOH溶液中和后,恰好完全转化为KCl和一种二元含氧酸的钾盐晶体。请计算
(1)参与反应的n(S2Cl2): n(SO2)=1:_______
(2)确定二元含氧酸的化学式_______ 。
(1)参与反应的n(S2Cl2): n(SO2)=1:
(2)确定二元含氧酸的化学式
您最近一年使用:0次
名校
解题方法
6 . 配平以下方程式并用单线桥法标出下列反应电子转移的方向和数目。(若系数为“1”,请标出)
(1)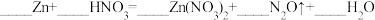
_______ 。
(2)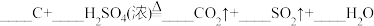
_______ 。
(3)
_______ 。
(4)
_______ 。
(5)
_______ 。
(6)
_______ 。
(1)
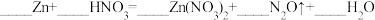
(2)
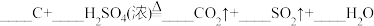
(3)

(4)

(5)

(6)

您最近一年使用:0次
解题方法
7 . 纳米级Cu2O可以作为太阳光分解水的催化剂,有这重要的应用前景。在加热的条件下用液态肼(N2H4)还原新制Cu(OH)2可制备纳米级Cu2O,同时生成N2,写出该反应的化学方程式_______ 。当收集的N2体积为3.36L(标准状况),计算制得纳米Cu2O的质量_______ 和转移电子数_______ 。
您最近一年使用:0次
8 . 甲酸和乙酸都是重要的化工原料。移取20.00mL甲酸和乙酸的混合溶液,以0.1000mol·L-1NaOH标准溶液滴定至终点,消耗25.00mL。另取20.00mL上述混合溶液,加入50.00mL0.02500mol·L-1KMnO4强碱性溶液,反应完全后,调节至酸性,加入40.00mL0.02000mol·L-1Fe2+标准溶液,用上述KMnO4标准溶液滴定至终点,消耗24.00mL。
(1)计算混合溶液中甲酸和乙酸的总量_______ 。
(2)写出氧化还原滴定反应的化学方程式_______ 。
(3)计算混合酸溶液中甲酸和乙酸的浓度_______ 。
(1)计算混合溶液中甲酸和乙酸的总量
(2)写出氧化还原滴定反应的化学方程式
(3)计算混合酸溶液中甲酸和乙酸的浓度
您最近一年使用:0次
9 . 尿磷是指尿中的全部无机磷酸盐,尿中尿磷的正常值成人为22 ~ 48 mmol/24h,儿童为16~ 48mmol/24h。某些疾病可引起尿磷升高,而另一些疾病会使尿磷降低。在测定磷酸盐的分光光度法中,大多是利用在酸性介质中磷酸盐与钼酸盐形成磷钼杂多酸的反应,反应产物是黄色的,又称磷钼黄。为提高灵敏度,一般采用钼蓝法:在温和条件下将磷钼黄还原为磷钼蓝(MoO2·4MoO3)2·H3PO4·4H2O,然后进行测定。一种测定尿磷 (原子量30.97) 的方法如下:尿液用钼(VI)处理,生成磷钼复合物,然后用4-氨基-3羟基-1-蔡磺酸还原,形成磷钼蓝,其最大吸收波长为690 nm。某患者24小时排尿总量1270 mL,今移取该尿液1.00 mL用钼试剂和4-氨基-3-羟基-1-蔡磺酸处理并稀释至50.0 mL,同法处理磷酸盐标准溶液系列,以试剂空白溶液作参比,在690 nm波长处测定吸光值,结果如下:
(1)该组测定数据符合一元线性回归方程y=bx+a,计算该患者每天排出的磷有多少克__________ 。
(2)计算该尿液中磷酸盐的浓度(mmol·L-1)__________ 。
(3)写出在酸性介质中磷酸盐与钼酸铵生成磷钼黄的离子反应方程式__________ 。
(4)写出用4-氨基-3-羟基-1-萘磺酸将磷钼黄还原为磷钼蓝的反应式(有机物用结构式表示)__________ 。
| 测试溶液 | 吸光值 |
| 1.00 ppm P | 0.205 |
| 2.00 ppm P | 0.410 |
| 3.00 ppm P | 0.615 |
| 4.00 ppm P | 0.820 |
| 尿样 | 0.625 |
(1)该组测定数据符合一元线性回归方程y=bx+a,计算该患者每天排出的磷有多少克
(2)计算该尿液中磷酸盐的浓度(mmol·L-1)
(3)写出在酸性介质中磷酸盐与钼酸铵生成磷钼黄的离子反应方程式
(4)写出用4-氨基-3-羟基-1-萘磺酸将磷钼黄还原为磷钼蓝的反应式(有机物用结构式表示)
您最近一年使用:0次
10 . 空气中含有少量臭氧(O3)可以起到消毒、杀菌的作用。但臭氧过量会对人体有害。我国的环境空气质量标准对空气中臭氧的最高浓度(单位体积的空气中所含臭氧的质量)限值如下表所示:
臭氧与KI溶液反应,生成1种可使带火星木条复燃的气体,反应后的溶液能使酚酞试液变红,也能使蘸有淀粉溶液的滤纸条变蓝。为测定某地臭氧的含量,将50m3的空气通过足量的KI溶液,使臭氧完全反应:在所得溶液中再加入适量的Na2S2O3溶液(含Na2S2O3的质量为47.4mg)。恰好完全反应(2Na2S2O3+I2=Na2S4O6+2NaI)。
①O3与KI反应的化学方程式:_______ 。
②通过计算确定该地区空气中臭氧浓度的级别_______ 。
| 浓度限值(mg/m3) | ||
| 一级标准0.12 | 二级标准0.16 | 三级标准0.20 |
臭氧与KI溶液反应,生成1种可使带火星木条复燃的气体,反应后的溶液能使酚酞试液变红,也能使蘸有淀粉溶液的滤纸条变蓝。为测定某地臭氧的含量,将50m3的空气通过足量的KI溶液,使臭氧完全反应:在所得溶液中再加入适量的Na2S2O3溶液(含Na2S2O3的质量为47.4mg)。恰好完全反应(2Na2S2O3+I2=Na2S4O6+2NaI)。
①O3与KI反应的化学方程式:
②通过计算确定该地区空气中臭氧浓度的级别
您最近一年使用:0次



