1 . 现有中学化学常见的物质 、
、 、
、 、
、 、
、 、
、 、
、 、
、 满足如下图所示转化关系。其中
满足如下图所示转化关系。其中 、
、 为气体单质,
为气体单质, 呈黄绿色,
呈黄绿色, 为淡黄色固体化合物,
为淡黄色固体化合物, 为生活中常见的液体化合物。回答下列问题:
为生活中常见的液体化合物。回答下列问题: :
:___________ ; :
:___________ 。
(2)写出反应②的化学方程式:___________ 。
(3)由于 发生③反应而不易于保存,故生产生活中往往用
发生③反应而不易于保存,故生产生活中往往用 与石灰乳反应生成易于保存运输的固体,该固体中的有效成分是
与石灰乳反应生成易于保存运输的固体,该固体中的有效成分是___________ (填化学式)。
(4)写出 的电子式:
的电子式:___________ 。
(5)下列关于 的说法正确的是
的说法正确的是___________ (填标号)。
a.只含离子键 b.含有离子键和共价键 c.阴、阳离子个数比为
(6)要增大氯水中次氯酸的浓度,可向氯水中加入少量的___________ (填“碳酸钙”或“氢氧化钠”)固体。
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 满足如下图所示转化关系。其中
满足如下图所示转化关系。其中 、
、 为气体单质,
为气体单质, 呈黄绿色,
呈黄绿色, 为淡黄色固体化合物,
为淡黄色固体化合物, 为生活中常见的液体化合物。回答下列问题:
为生活中常见的液体化合物。回答下列问题: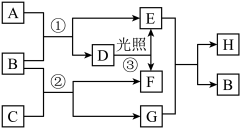
 :
: :
:(2)写出反应②的化学方程式:
(3)由于
 发生③反应而不易于保存,故生产生活中往往用
发生③反应而不易于保存,故生产生活中往往用 与石灰乳反应生成易于保存运输的固体,该固体中的有效成分是
与石灰乳反应生成易于保存运输的固体,该固体中的有效成分是(4)写出
 的电子式:
的电子式:(5)下列关于
 的说法正确的是
的说法正确的是a.只含离子键 b.含有离子键和共价键 c.阴、阳离子个数比为

(6)要增大氯水中次氯酸的浓度,可向氯水中加入少量的
您最近一年使用:0次
2 . 钠、氯及其化合物有如图转化关系,淡黄色物质M可在潜水艇中作为氧气的来源,常被用作供氧剂,N常⽤来杀菌消毒。请按要求填空:
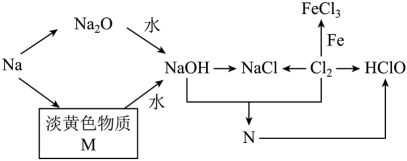
(1)淡黄色物质M是___________ (填化学式),物质N是___________ (填化学式)。
(2)写出M与水反应的离子方程式为___________ ,还原剂为___________ (填化学式)。
(3) 与
与 反应的化学反应方程式为
反应的化学反应方程式为___________ ,每消耗掉 ,转移电子的物质的量是
,转移电子的物质的量是___________ 。
(4)除去 固体中少量杂质
固体中少量杂质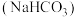 ,写出相关化学方程式:
,写出相关化学方程式:___________ 。除去 溶液中少量杂质
溶液中少量杂质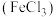 ,写出相关化学方程式:
,写出相关化学方程式:___________ 。

(1)淡黄色物质M是
(2)写出M与水反应的离子方程式为
(3)
 与
与 反应的化学反应方程式为
反应的化学反应方程式为 ,转移电子的物质的量是
,转移电子的物质的量是(4)除去
 固体中少量杂质
固体中少量杂质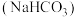 ,写出相关化学方程式:
,写出相关化学方程式: 溶液中少量杂质
溶液中少量杂质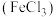 ,写出相关化学方程式:
,写出相关化学方程式:
您最近一年使用:0次
解题方法
3 .  是高效安全灭菌消毒剂,部分性质如下:
是高效安全灭菌消毒剂,部分性质如下:
实验室可利用反应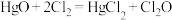 制取
制取 ,装置如图所示:
,装置如图所示:
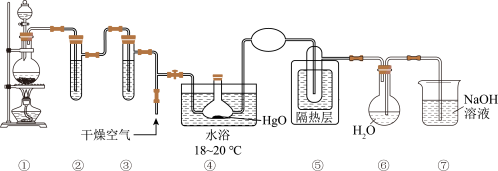
(1)装置⑥中仪器的名称为_______ 。
(2)装置①中制取氯气时需要 盐酸,若加入盐酸的体积是
盐酸,若加入盐酸的体积是 ,制取氯气的物质的量小于
,制取氯气的物质的量小于 ,除了考虑盐酸的挥发和生成水的因素外,最主要的原因是
,除了考虑盐酸的挥发和生成水的因素外,最主要的原因是_______ 。
(3)③中试剂的名称是_______ 。
(4)④中反应氧化剂和还原剂物质的量比值是_______ 。
(5)⑥中 与水反应制取
与水反应制取 ,反应的化学方程式是
,反应的化学方程式是_______ ; 中混有盐酸,原因是
中混有盐酸,原因是_______ (用化学方程式表示)。
(6)⑦中 溶液能吸收多余的氯气,防止污染空气,发生反应的离子方程式是
溶液能吸收多余的氯气,防止污染空气,发生反应的离子方程式是_______ 。
 是高效安全灭菌消毒剂,部分性质如下:
是高效安全灭菌消毒剂,部分性质如下:| 物理性质 | 化学性质 |
| 常温下,具有强烈刺激性气味的黄棕色气体 熔点:  ℃;沸点:3.8℃;42℃以上分解为 ℃;沸点:3.8℃;42℃以上分解为 和 和 。 。 | 强氧化性;与有机物、还原剂接触或浓度过高时会发生爆炸;易溶于水且会与水反应生成次氯酸 |
 制取
制取 ,装置如图所示:
,装置如图所示:
(1)装置⑥中仪器的名称为
(2)装置①中制取氯气时需要
 盐酸,若加入盐酸的体积是
盐酸,若加入盐酸的体积是 ,制取氯气的物质的量小于
,制取氯气的物质的量小于 ,除了考虑盐酸的挥发和生成水的因素外,最主要的原因是
,除了考虑盐酸的挥发和生成水的因素外,最主要的原因是(3)③中试剂的名称是
(4)④中反应氧化剂和还原剂物质的量比值是
(5)⑥中
 与水反应制取
与水反应制取 ,反应的化学方程式是
,反应的化学方程式是 中混有盐酸,原因是
中混有盐酸,原因是(6)⑦中
 溶液能吸收多余的氯气,防止污染空气,发生反应的离子方程式是
溶液能吸收多余的氯气,防止污染空气,发生反应的离子方程式是
您最近一年使用:0次
解题方法
4 . Ⅰ.如图所示,根据实验室制取氯气的原理制备氯气并进行性质验证,回答下列问题:

(1)装置A的名称为______ ,甲装置中发生反应的离子方程式为______ 。
(2)利用装置丙制取饱和氯水,并测其pH。
①证明氯水已饱和的现象是______ 。
②若撤去装置乙,直接将装置甲和丙相连,这样做对实验测定结果的影响是______ 。
Ⅱ.制备HClO溶液,可将氯气和空气(空气中所有成分不参与反应)按体积比1∶3混合后通入含水8%的 悬浊液中制备
悬浊液中制备 ,并用水吸收
,并用水吸收 制备HClO溶液,实验过程如图所示(夹持装置未画出)。
制备HClO溶液,实验过程如图所示(夹持装置未画出)。
已知:① 极易溶于水并与水反应生成HClO;
极易溶于水并与水反应生成HClO;
② 的沸点为3.8℃,42℃以上分解为和
的沸点为3.8℃,42℃以上分解为和 。
。

(3)A瓶中通入的是纯净的 ,写出装置A的两个作用
,写出装置A的两个作用______ 。
(4)装置B中每生成1mol 转移的电子为
转移的电子为______ mol。
(5)有同学提出B装置外围最好加一个水浴加热装置,控制温度范围在______ 之间,则效果会更好。
(6)装置C中发生的化学反应方程式为______ 。

(1)装置A的名称为
(2)利用装置丙制取饱和氯水,并测其pH。
①证明氯水已饱和的现象是
②若撤去装置乙,直接将装置甲和丙相连,这样做对实验测定结果的影响是
Ⅱ.制备HClO溶液,可将氯气和空气(空气中所有成分不参与反应)按体积比1∶3混合后通入含水8%的
 悬浊液中制备
悬浊液中制备 ,并用水吸收
,并用水吸收 制备HClO溶液,实验过程如图所示(夹持装置未画出)。
制备HClO溶液,实验过程如图所示(夹持装置未画出)。已知:①
 极易溶于水并与水反应生成HClO;
极易溶于水并与水反应生成HClO;②
 的沸点为3.8℃,42℃以上分解为和
的沸点为3.8℃,42℃以上分解为和 。
。
(3)A瓶中通入的是纯净的
 ,写出装置A的两个作用
,写出装置A的两个作用(4)装置B中每生成1mol
 转移的电子为
转移的电子为(5)有同学提出B装置外围最好加一个水浴加热装置,控制温度范围在
(6)装置C中发生的化学反应方程式为
您最近一年使用:0次
解题方法
5 . 某同学用下列各装置设计一个实验,验证氯气的性质。
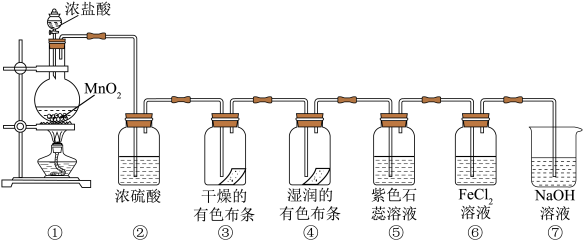
请回答:
(1)盛浓盐酸的仪器名称为___________ 。
(2)①中的化学方程式为___________ ;浓盐酸在反应中显示出来的性质是___________ 。(用字母填空)
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
②中浓硫酸的作用是___________ 。
(3)③中的实验现象是___________ ;④中的实验现象是___________ ;上述实验现象说明起漂白作用的是___________ (填分子式)。
(4)⑤中的现象是___________
(5)⑥中发生反应的离子方程式是___________
(6)⑦中NaOH溶液的作用是___________ ,试写出反应的离子方程式:___________ 。

请回答:
(1)盛浓盐酸的仪器名称为
(2)①中的化学方程式为
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
②中浓硫酸的作用是
(3)③中的实验现象是
(4)⑤中的现象是
(5)⑥中发生反应的离子方程式是
(6)⑦中NaOH溶液的作用是
您最近一年使用:0次
6 . 实验室制取氯气并验证其性质,装置如图所示。
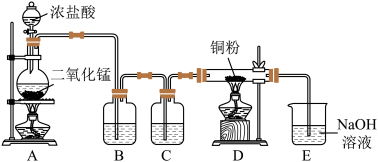
已知:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
回答下列问题:
(1)B中选用的试剂是饱和食盐水,作用是________ ,C中选用试剂是________ (填名称)。
(2)装置E的作用是________ ,写出E中发生反应的离子方程式:________ 。
(3)实验发现D中得到的无水CuCl2总是偏蓝色,请你提出改进方案:________ 。
(4)为证明氯气与水反应产物具有漂白性,某同学将A中产生的气体缓缓通过下列装置:
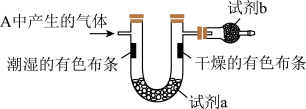
试剂a应选择________ (填名称,下同);
试剂b应选择________ 。

已知:MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O回答下列问题:
(1)B中选用的试剂是饱和食盐水,作用是
(2)装置E的作用是
(3)实验发现D中得到的无水CuCl2总是偏蓝色,请你提出改进方案:
(4)为证明氯气与水反应产物具有漂白性,某同学将A中产生的气体缓缓通过下列装置:

试剂a应选择
试剂b应选择
您最近一年使用:0次
7 . 某化学实验小组为了探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,设计了如图所示的实验装置(氯气易溶于CCl4,HCl不溶于CCl4)。

回答下列问题:
(1)盛有MnO2的装置名称__________ ,装置A中发生反应的离子方程式为__________ ,装置B中盛放的药品是__________ 。
(2)一段时间后,根据装置D与E中出现的不同现象可得出的结论是__________ 。
(3)装置F的作用是__________ 。
(4)乙同学认为上述实验装置有缺陷,不能确保最终通入AgNO3溶液中的气体只有一种。为了确保实验结论的可靠性,乙同学提出可在__________ (填字母)两个装置之间再加一个装有湿润的淀粉KI试纸的装置,发生反应的离子方程式为__________ 。

回答下列问题:
(1)盛有MnO2的装置名称
(2)一段时间后,根据装置D与E中出现的不同现象可得出的结论是
(3)装置F的作用是
(4)乙同学认为上述实验装置有缺陷,不能确保最终通入AgNO3溶液中的气体只有一种。为了确保实验结论的可靠性,乙同学提出可在
您最近一年使用:0次
8 . 某化学兴趣小组同学为验证氯气的性质并制备少量干燥的氯化铁,设计并进行如下实验:

回答下列问题:
(1)若要得到干燥的氯气,D中应盛放的试剂是__________ 。
(2)实验时C中可观察到的现象是_________________ ,氯气与水发生反应的化学方程式是___________________ ,检验该溶液中是否含有 的方法是
的方法是____________________
(3)E中发生反应的化学方程式是____________________ 。
(4)F瓶溶液的作用是____________________

回答下列问题:
(1)若要得到干燥的氯气,D中应盛放的试剂是
(2)实验时C中可观察到的现象是
 的方法是
的方法是(3)E中发生反应的化学方程式是
(4)F瓶溶液的作用是
您最近一年使用:0次
9 . 写出要求的方程式

(1)①离子方程式____________________________ ;
(2)②离子方程式______________________ ;
(3)③化学方程式____________________________ ;
(4)④溶液中,离子方程式______________________ ;
(5)⑤固体,化学方程式______________________ ;
(6)⑥溶液中,离子方程式______________________ ;
(7)⑦化学方程式____________________________ ;
(8)⑧离子方程式______________________ ;
(9)⑨离子方程式______________________ ;

(1)①离子方程式
(2)②离子方程式
(3)③化学方程式
(4)④溶液中,离子方程式
(5)⑤固体,化学方程式
(6)⑥溶液中,离子方程式
(7)⑦化学方程式
(8)⑧离子方程式
(9)⑨离子方程式
您最近一年使用:0次
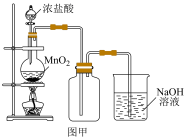
10 . 某化学学习小组同学用如图装置进行Cl2的制备和性质实验探究。回答下列问题:
(1)若采用图甲所示的装置制备并收集氯气,则氯气中含有的杂质是___________ ;该装置中制取氯气的化学方程式为___________ 。
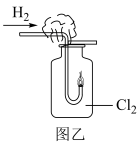
(2)在进行图乙实验中,可以观察到的现象是___________ 。
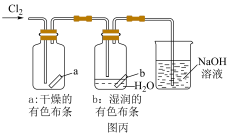
(3)在进行图丙实验时,NaOH溶液的作用是___________ (用离子方程式表示)。对比a和b中的实验现象,能得出的一个结论是___________ 。
(1)若采用图甲所示的装置制备并收集氯气,则氯气中含有的杂质是

(2)在进行图乙实验中,可以观察到的现象是

(3)在进行图丙实验时,NaOH溶液的作用是

您最近一年使用:0次



