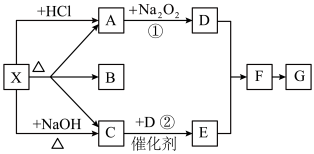
1 . 几种常见物质的转化关系如下图所示,图中每一方格表示有关的一种反应物或生成物,其中A、C为无色气体。
(1)物质X可以是_____ ,C是_____ ,F是_____ 。
(2)反应②的化学方程式是_______ 。
(1)物质X可以是
(2)反应②的化学方程式是
您最近一年使用:0次
2 . 硫酸铵在常温下是无色晶体或白色颗粒,280℃以上开始分解,500℃以上彻底分解为气体。某实验小组设计如下实验验证硫酸铵的分解产物并测量某气体产物的体积。回答下列问题。已知:氮气不能和氧化铜发生反应。_______ 。
(2)当图1与图2连接后,进行实验时可以观察到无水硫酸铜变蓝色,证明硫酸铵的分解产物有_______ (填化学式);观察到品红溶液褪色,酸性KMnO4溶液的紫色变浅,量气管中收集到一种气体单质(经检验该气体单质能使燃着的火柴熄灭),最后大试管中无固体剩余。
(3)当图1与图3连接后进行实验,可以观察到玻璃管中黑色固体变红色,能产生该现象的气体是_______ (填化学式),此时该气体表现出_______ 性(填“氧化”或“还原”)。且该气体极易溶于水,为了防止倒吸,可以用_______ 装置来处理该气体(填字母)。_______ 。

(2)当图1与图2连接后,进行实验时可以观察到无水硫酸铜变蓝色,证明硫酸铵的分解产物有
(3)当图1与图3连接后进行实验,可以观察到玻璃管中黑色固体变红色,能产生该现象的气体是

您最近一年使用:0次
3 . A~F的转化关系如图1所示(部分产物略去),其中A为盐类,B、D、E、F常温常压下均为气体,且E为红棕色气体,G为一种紫红色金属单质。反应①为分解反应,且产物只有B、C两种,反应④、⑤中C溶液的浓度不同。常温下,将Al片浸在不同质量分数的C溶液中,经过相同时间的腐蚀后,Al片的质量损失情况如图2所示。
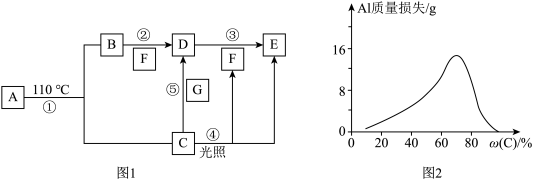
回答下列问题,
(1)写出下列物质的化学式:A___________ ,C___________ 。
(2)B的电子式为___________ 。
(3)写出下列反应的化学方程式。
反应②:___________ ;
反应④:___________ ;
反应⑤:___________ 。
(4)图2中Al质量损失随C溶液质量分数的变化先增大后减小,减小的原因为___________ 。

回答下列问题,
(1)写出下列物质的化学式:A
(2)B的电子式为
(3)写出下列反应的化学方程式。
反应②:
反应④:
反应⑤:
(4)图2中Al质量损失随C溶液质量分数的变化先增大后减小,减小的原因为
您最近一年使用:0次
名校
解题方法
4 . 某工厂的固体废渣中主要含 和
和 ,还含有少量
,还含有少量 和
和 。利用该固体废渣制取
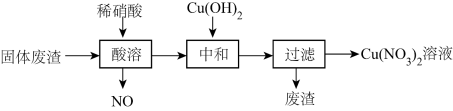
。利用该固体废渣制取 溶液的工艺流程如图所示:
溶液的工艺流程如图所示:
已知:①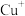 在酸性溶液中不稳定,会转变成
在酸性溶液中不稳定,会转变成 和
和 。
。
② 是酸性氧化物,难于水和酸。
是酸性氧化物,难于水和酸。
(1)写出 与稀硝酸反应的离子反应方程式为
与稀硝酸反应的离子反应方程式为___________ ;
(2)酸溶时,反应温度不宜超过 ,其主要原因是
,其主要原因是___________ ;
(3)酸溶试剂改用绿色氧化剂(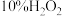 和
和 稀硝酸的混合液),基本无氮氧化物排放,写出废渣中
稀硝酸的混合液),基本无氮氧化物排放,写出废渣中 与绿色氧化剂反应的离子反应方程式
与绿色氧化剂反应的离子反应方程式___________ ;
(4)中和试剂选择 ,若改为
,若改为 ,缺点是
,缺点是___________ 。
 和
和 ,还含有少量
,还含有少量 和
和 。利用该固体废渣制取
。利用该固体废渣制取 溶液的工艺流程如图所示:
溶液的工艺流程如图所示:
已知:①
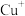 在酸性溶液中不稳定,会转变成
在酸性溶液中不稳定,会转变成 和
和 。
。②
 是酸性氧化物,难于水和酸。
是酸性氧化物,难于水和酸。(1)写出
 与稀硝酸反应的离子反应方程式为
与稀硝酸反应的离子反应方程式为(2)酸溶时,反应温度不宜超过
 ,其主要原因是
,其主要原因是(3)酸溶试剂改用绿色氧化剂(
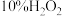 和
和 稀硝酸的混合液),基本无氮氧化物排放,写出废渣中
稀硝酸的混合液),基本无氮氧化物排放,写出废渣中 与绿色氧化剂反应的离子反应方程式
与绿色氧化剂反应的离子反应方程式(4)中和试剂选择
 ,若改为
,若改为 ,缺点是
,缺点是
您最近一年使用:0次
名校
5 . 盐酸羟胺(NH2OH•HCl是一种重要的分析试剂,化学性质与铵盐相似。实验室以丁酮肟( )、盐酸为原料制备盐酸羟胺的装置如图所示(加热、夹持装置省略)。
)、盐酸为原料制备盐酸羟胺的装置如图所示(加热、夹持装置省略)。

②盐酸羟胺的熔点为152℃,丁酮肟的沸点为153℃,丁酮的沸点为79.6℃。回答下列问题:
(1)直形冷凝管的进水口为
(2)甲装置中生成盐酸羟胺和丁酮的化学反应方程式为
(3)从反应后的溶液中获取盐酸羟胺的方法为
(4)测定产品纯度。
称取mg盐酸羟胺产品,配制成100mL溶液,量取25.00mL于锥形瓶中,加入适量稀硫酸酸化,再加入过量硫酸铁溶液,发生反应:2[NH3OH]++4Fe3+=4Fe2++N2O↑+6H++H2O,充分反应后,用cmol•L-1K2Cr2O7标准溶液滴定Fe2+(滴定过程中
 转化为Cr3+,Cl-不反应),滴定达终点时消耗K2Cr2O7溶液VmL。则样品中NH2OH•HCl的质量分数为
转化为Cr3+,Cl-不反应),滴定达终点时消耗K2Cr2O7溶液VmL。则样品中NH2OH•HCl的质量分数为
您最近一年使用:0次
2024-03-22更新
|
662次组卷
|
4卷引用:山东省临沂市2024届高三一模化学试题
6 . 我国锰矿资源主要为贫碳酸锰矿(主要成分为 ,还含有少量
,还含有少量 、
、 、
、 、
、 、
、 、
、 ),利用贫碳酸锰矿制取
),利用贫碳酸锰矿制取 的流程如图所示,回答下列问题。
的流程如图所示,回答下列问题。 ,
, 。
。
(1) 中锰元素的价态有+2价和+3价,则下列表示
中锰元素的价态有+2价和+3价,则下列表示 组成的式子正确的是___________(填标号)。
组成的式子正确的是___________(填标号)。
(2)“滤渣1”的主要成分是___________ (填化学式)。
(3)“氧化”的目的是将 转化为
转化为 ,写出发生反应的离子方程式
,写出发生反应的离子方程式___________ ,检测 是否完全氧化的试剂是
是否完全氧化的试剂是___________ (写试剂名称)。
(4)“除钙镁”后的滤液中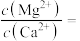
___________ 。
(5)“碳化”过程需要加热,但温度不能太高,试分析温度不能太高的原因___________ 。
(6)“焙烧”过程中随温度不同生成的锰的氧化物也不同。图中A点对应的氧化物是___________ ,为了获得 ,需要加热到
,需要加热到___________  (已知:A、B、C三点对应的物质均为纯净氧化物)。
(已知:A、B、C三点对应的物质均为纯净氧化物)。
 ,还含有少量
,还含有少量 、
、 、
、 、
、 、
、 、
、 ),利用贫碳酸锰矿制取
),利用贫碳酸锰矿制取 的流程如图所示,回答下列问题。
的流程如图所示,回答下列问题。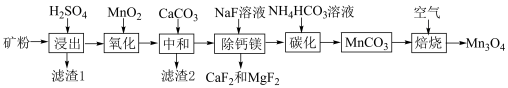
 ,
, 。
。(1)
 中锰元素的价态有+2价和+3价,则下列表示
中锰元素的价态有+2价和+3价,则下列表示 组成的式子正确的是___________(填标号)。
组成的式子正确的是___________(填标号)。A.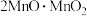 | B.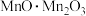 | C.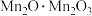 | D. |
(2)“滤渣1”的主要成分是
(3)“氧化”的目的是将
 转化为
转化为 ,写出发生反应的离子方程式
,写出发生反应的离子方程式 是否完全氧化的试剂是
是否完全氧化的试剂是(4)“除钙镁”后的滤液中
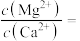
(5)“碳化”过程需要加热,但温度不能太高,试分析温度不能太高的原因
(6)“焙烧”过程中随温度不同生成的锰的氧化物也不同。图中A点对应的氧化物是
 ,需要加热到
,需要加热到 (已知:A、B、C三点对应的物质均为纯净氧化物)。
(已知:A、B、C三点对应的物质均为纯净氧化物)。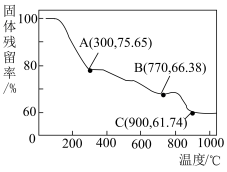
您最近一年使用:0次
2024-03-08更新
|
221次组卷
|
4卷引用:甘肃省张掖市某重点校2023-2024学年高三下学期模拟考化学试题
甘肃省张掖市某重点校2023-2024学年高三下学期模拟考化学试题(已下线)大题预测卷(黑龙江、吉林专用)-【大题精做】冲刺2024年高考化学大题突破+限时集训(新高考专用)陕西省延安市黄龙县中学2023-2024学年高三下学期开学考试理综试卷-高中化学陕西省西安工业大学附属中学2023-2024学年高三下学期3月月考理科综合试题-高中化学
名校
7 . 以氯化钾和钛白厂的副产品硫酸亚铁为原料生产硫酸钾、过二硫酸铵和氧化铁红颜料,原料的综合利用率较高。其主要流程如下:
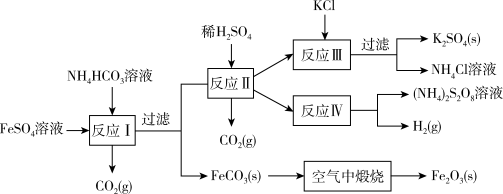
(1)反应Ⅰ前需在 溶液中加入___________(填字母),以除去溶液中的
溶液中加入___________(填字母),以除去溶液中的 ;
;
(2)反应Ⅰ需控制反应温度低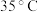 ,其目的是
,其目的是___________ 。
(3)反应Ⅳ常被用于电解生产 (过二硫酸铵)。电解时均用惰性电极,阳极发生的电极反应可表示为
(过二硫酸铵)。电解时均用惰性电极,阳极发生的电极反应可表示为___________ 。
(4)反应Ⅰ的离子方程式为___________ 。
(5)空气中煅烧的化学方程式为___________ 。

(1)反应Ⅰ前需在
 溶液中加入___________(填字母),以除去溶液中的
溶液中加入___________(填字母),以除去溶液中的 ;
;| A.锌粉 | B.铁屑 | C. 溶液 溶液 | D. |
(2)反应Ⅰ需控制反应温度低
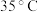 ,其目的是
,其目的是(3)反应Ⅳ常被用于电解生产
 (过二硫酸铵)。电解时均用惰性电极,阳极发生的电极反应可表示为
(过二硫酸铵)。电解时均用惰性电极,阳极发生的电极反应可表示为(4)反应Ⅰ的离子方程式为
(5)空气中煅烧的化学方程式为
您最近一年使用:0次
名校
解题方法
8 . 为应对全球气候的变化,我国科学家研发一种“氨气/石膏联合法”用于吸收工厂中排放的 ,同时获得产品
,同时获得产品 。其反应原理为:
。其反应原理为: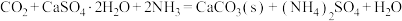
I.根据上述反应原理,在实验室模拟生产硫酸铵。请回答下列问题:
(1)应用下图装置,先通入 ,用干燥管替代长导管的目的是
,用干燥管替代长导管的目的是___________ ;再通入 ,当液体由红色变为浅红色时,立即停止通入,此时溶液的
,当液体由红色变为浅红色时,立即停止通入,此时溶液的 范围为
范围为___________ , 不通入过量,原因可能是
不通入过量,原因可能是___________ 。

(2)反应后的混合物经过过滤、蒸发浓缩、冷却结晶、过滤、洗涤及烘干。两次过滤依次得到的物质分别为___________ 和___________ ;烘干温度不宜过高的原因为___________ 。
II.为了测定样品中 的纯度,进行实验。取
的纯度,进行实验。取 硫酸铵在碱性溶液中反应,烝馏出生成的氨气,用
硫酸铵在碱性溶液中反应,烝馏出生成的氨气,用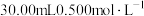 硫酸标准液吸收,再用氢氧化钠标准溶液滴定吸收氨气后过量的硫酸。
硫酸标准液吸收,再用氢氧化钠标准溶液滴定吸收氨气后过量的硫酸。
(3)若滴定时消耗了 的
的 溶液
溶液 ,则该硫酸铵产品的纯度为
,则该硫酸铵产品的纯度为________  。(保留3位有效数字)
。(保留3位有效数字)
(4)若氨气没有充分蒸出,则实验结果将___________ (选填“偏大”“偏小”或“无影响”)。
 ,同时获得产品
,同时获得产品 。其反应原理为:
。其反应原理为: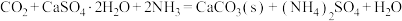
I.根据上述反应原理,在实验室模拟生产硫酸铵。请回答下列问题:
(1)应用下图装置,先通入
 ,用干燥管替代长导管的目的是
,用干燥管替代长导管的目的是 ,当液体由红色变为浅红色时,立即停止通入,此时溶液的
,当液体由红色变为浅红色时,立即停止通入,此时溶液的 范围为
范围为 不通入过量,原因可能是
不通入过量,原因可能是
(2)反应后的混合物经过过滤、蒸发浓缩、冷却结晶、过滤、洗涤及烘干。两次过滤依次得到的物质分别为
II.为了测定样品中
 的纯度,进行实验。取
的纯度,进行实验。取 硫酸铵在碱性溶液中反应,烝馏出生成的氨气,用
硫酸铵在碱性溶液中反应,烝馏出生成的氨气,用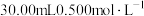 硫酸标准液吸收,再用氢氧化钠标准溶液滴定吸收氨气后过量的硫酸。
硫酸标准液吸收,再用氢氧化钠标准溶液滴定吸收氨气后过量的硫酸。(3)若滴定时消耗了
 的
的 溶液
溶液 ,则该硫酸铵产品的纯度为
,则该硫酸铵产品的纯度为 。(保留3位有效数字)
。(保留3位有效数字)(4)若氨气没有充分蒸出,则实验结果将
您最近一年使用:0次
2024-02-16更新
|
140次组卷
|
3卷引用:安徽省合肥市第一中学2023-2024学年高二上学期期末考试化学试题
9 . 柠檬酸亚铁是一种高效补铁剂。利用硫铁矿烧渣(主要含 及少量
及少量 、
、 )制备柠檬酸亚铁的工艺流程如图。
)制备柠檬酸亚铁的工艺流程如图。
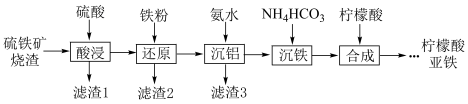
已知:常温下, 时
时 沉淀完全,
沉淀完全, 时
时 开始沉淀。
开始沉淀。
回答下列问题:
(1)滤渣1为________ (填化学式)。
(2)“还原”过程中发生反应的离子方程式为_______ 。检验“还原”过程中反应是否完全进行的试剂为_______ (填化学式)。
(3)“沉铝”过程应调节溶液的pH范围为_______ 。
(4)“沉铁”过程反应生成 和
和 的离子方程式为
的离子方程式为______ 。此过程需控制温度在35℃以下,可能原因是_______ 。
(5)“合成”过程中,需加入少量的抗氧化剂,下列试剂合适的是________(填标号)。
 及少量
及少量 、
、 )制备柠檬酸亚铁的工艺流程如图。
)制备柠檬酸亚铁的工艺流程如图。
已知:常温下,
 时
时 沉淀完全,
沉淀完全, 时
时 开始沉淀。
开始沉淀。回答下列问题:
(1)滤渣1为
(2)“还原”过程中发生反应的离子方程式为
(3)“沉铝”过程应调节溶液的pH范围为
(4)“沉铁”过程反应生成
 和
和 的离子方程式为
的离子方程式为(5)“合成”过程中,需加入少量的抗氧化剂,下列试剂合适的是________(填标号)。
A. | B.Fe | C.Cu | D. |
您最近一年使用:0次
名校
解题方法
10 . 下图中的每一个方格表示有关的一种反应物或生成物,其中A、C为无色气体
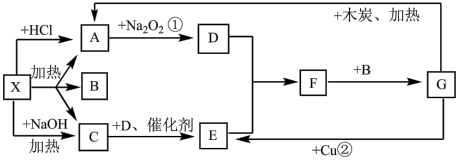
(1)写出有关物质的化学式X:_________ ;F_________ 。
(2)写出F→G的化学方程式_________ 。
(3)写出实验室制备C的化学方程式_________ 。
(4)分别取两份
 溶液,各向其中通入一定量的气体A,随后各取溶液10mL分别将其稀释到相同体积,得到溶液甲和乙,分别向甲和乙中逐滴加入
溶液,各向其中通入一定量的气体A,随后各取溶液10mL分别将其稀释到相同体积,得到溶液甲和乙,分别向甲和乙中逐滴加入 的
的 溶液,产生的A气体体积(标准状况下)与所加入的
溶液,产生的A气体体积(标准状况下)与所加入的 的体积之间的关系如图所示,试分析:
的体积之间的关系如图所示,试分析:
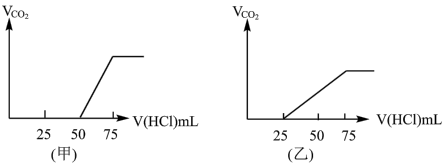
① 在吸收A气体后,乙图所示溶液中存在的溶质是:
在吸收A气体后,乙图所示溶液中存在的溶质是:_________ ,其物质的量之比是:_________ 。
②原 溶液的物质的量浓度是
溶液的物质的量浓度是_______  ,甲图所示溶液最多还能吸收A体积为
,甲图所示溶液最多还能吸收A体积为_______ mL(标准状况)

(1)写出有关物质的化学式X:
(2)写出F→G的化学方程式
(3)写出实验室制备C的化学方程式
(4)分别取两份

 溶液,各向其中通入一定量的气体A,随后各取溶液10mL分别将其稀释到相同体积,得到溶液甲和乙,分别向甲和乙中逐滴加入
溶液,各向其中通入一定量的气体A,随后各取溶液10mL分别将其稀释到相同体积,得到溶液甲和乙,分别向甲和乙中逐滴加入 的
的 溶液,产生的A气体体积(标准状况下)与所加入的
溶液,产生的A气体体积(标准状况下)与所加入的 的体积之间的关系如图所示,试分析:
的体积之间的关系如图所示,试分析:
①
 在吸收A气体后,乙图所示溶液中存在的溶质是:
在吸收A气体后,乙图所示溶液中存在的溶质是:②原
 溶液的物质的量浓度是
溶液的物质的量浓度是 ,甲图所示溶液最多还能吸收A体积为
,甲图所示溶液最多还能吸收A体积为
您最近一年使用:0次



