1 . 下列物质的性质与用途具有对应关系的是
A. 有氢键,常用作制冷剂 有氢键,常用作制冷剂 |
B. 溶液呈酸性,可用作氮肥 溶液呈酸性,可用作氮肥 |
C. 受热易分解,可用作制备 受热易分解,可用作制备 |
D. 具有强氧化性,可用于制备硝酸纤维 具有强氧化性,可用于制备硝酸纤维 |
您最近一年使用:0次
名校
2 . 实验室制备下列气体的方法可行的是
| 气体 | 方法 | |
| A | 氨气 | 加热氯化铵固体 |
| B | 二氧化氮 | 将铝片加到冷浓硝酸中 |
| C | 硫化氢 | 向硫化钠固体滴加浓硫酸 |
| D | 氯化氢 | 向氯化钠固体滴加浓硫酸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
3 . 加热 与
与 的固体混合物制备无水
的固体混合物制备无水 ,起始物质的量之比为
,起始物质的量之比为 ,升温,从200℃开始有
,升温,从200℃开始有 生成,同时生成副产物
生成,同时生成副产物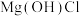 。混合物中
。混合物中 与
与 的质量分数
的质量分数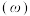 随温度的变化如图所示。
随温度的变化如图所示。

下列说法不正确 的是
 与
与 的固体混合物制备无水
的固体混合物制备无水 ,起始物质的量之比为
,起始物质的量之比为 ,升温,从200℃开始有
,升温,从200℃开始有 生成,同时生成副产物
生成,同时生成副产物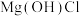 。混合物中
。混合物中 与
与 的质量分数
的质量分数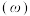 随温度的变化如图所示。
随温度的变化如图所示。
下列说法
A.200℃时,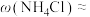 78%, 78%,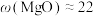 %,说明200℃之前体系中无化学反应 %,说明200℃之前体系中无化学反应 |
B.200~400℃时体系中存在反应: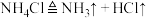 、 、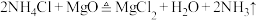 、 、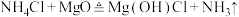 |
C.加热 与 与 的混合物可制备 的混合物可制备 ,原因之一是 ,原因之一是 可抑制 可抑制 转化为 转化为 和 和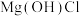 |
D.控制温度400℃左右,增大投料比 ,并使二者充分接触,利于提高 ,并使二者充分接触,利于提高 的产率 的产率 |
您最近一年使用:0次
4 . 锶与钙位于同一主族,其化合物应用广泛,SrSO4常用于陶瓷工业。以青石精矿(主要含SrSO4)为原料制备高纯硫酸锶的部分工艺流程如图所示:

A.气体 可以循环利用 可以循环利用 |
B.“转化”的总离子方程式为 |
| C.“转化”中反应温度不宜过高且控制氨水过量 |
| D.流程中涉及分解反应和化合反应 |
您最近一年使用:0次
2024-01-13更新
|
355次组卷
|
2卷引用:山西省大同市教育局2023-2024学年高三上学期冬季检测化学试卷
名校
5 . 一种以转炉钒渣(主要成分为V2O3、FeO、SiO2及少量MgO、CaO、Al2O3)为原料实现低成本回收钒资源的生产工艺如下:
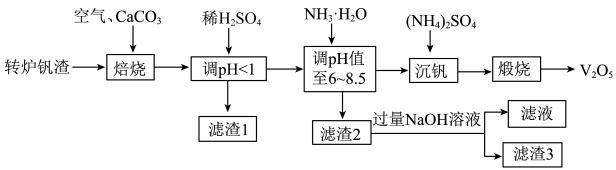
表一:相关金属离子[c0(Mn+) = 0.01 mol·L−1]形成氢氧化物沉淀的pH范围如下:
表二:部分含钒物质在水溶液中主要存在形式如下:
已知:①“焙烧”的主要反应之一为:CaCO3(s) = CaO(s) + CO2(g);
②在焙烧过程中产生Ca2V2O7;其中,Ca2V2O7在水中的溶解度小,易溶于稀硫酸和碱溶液。
(1)焙烧前将转炉钒渣研磨的目的是___________ 。
(2)Ca2V2O7中V的化合价为___________ ,写出在焙烧过程中产生Ca2V2O7的化学方程式___________ 。
(3)写出用稀H2SO4调pH<1的离子方程式为___________ 。
(4)“滤渣2”的主要成分是___________ 。
(5)“调pH值至6~8.5”时控制温度不超过40℃,原因是___________ 。
(6)沉钒后的操作是___________ 、干燥,得到NH4VO3.写出NH4VO3分解生成V2O5的化学方程式___________ 。

表一:相关金属离子[c0(Mn+) = 0.01 mol·L−1]形成氢氧化物沉淀的pH范围如下:
| 金属离子 | Fe2+ | Fe3+ | Al3+ | Mg2+ |
| 开始沉淀的pH | 7.5 | 2.2 | 3.7 | 9.4 |
| 沉淀完全的pH | 9.0 | 3.2 | 4.7 | 10.9 |
| pH | <1 | 1 ~ 4 | 6 ~ 8.5 | >13 |
| 主要形式 | VO | V2O5 | VO | VO |
| 备注 | 多钒酸盐在水中溶解度较小 | |||
②在焙烧过程中产生Ca2V2O7;其中,Ca2V2O7在水中的溶解度小,易溶于稀硫酸和碱溶液。
(1)焙烧前将转炉钒渣研磨的目的是
(2)Ca2V2O7中V的化合价为
(3)写出用稀H2SO4调pH<1的离子方程式为
(4)“滤渣2”的主要成分是
(5)“调pH值至6~8.5”时控制温度不超过40℃,原因是
(6)沉钒后的操作是
您最近一年使用:0次
6 . 下列说法正确的是
A.用加热的方法分离 和 和 的固体混合物 的固体混合物 |
B.向某溶液中滴加几滴 溶液,产生白色沉淀,则原溶液中一定含 溶液,产生白色沉淀,则原溶液中一定含 |
C.向某盐溶液中滴加浓NaOH溶液并加热,产生使湿润的蓝色石蕊试纸变红的气体,则原溶液含 |
D.除去NaCl固体中少量 ,应将固体溶解后蒸发结晶,趁热过滤,洗涤,干燥 ,应将固体溶解后蒸发结晶,趁热过滤,洗涤,干燥 |
您最近一年使用:0次
名校
解题方法
7 . 铁红(Fe2O3)是一种用途广泛的颜料,用某烧渣(主要成分为 ,含少量
,含少量 )制备铁红的流程如下:
)制备铁红的流程如下:

(1)“焙烧”时,CO将Fe2O3还原为FeO,该过程中参加反应的还原剂与氧化剂的物质的量之比是___________ 。
(2)“酸浸”时,生成 的离子方程式为
的离子方程式为___________ 。
(3)“沉铁”时,除了生成 白色沉淀,还生成一种气体,该气体为
白色沉淀,还生成一种气体,该气体为___________ (填化学式),该过程中加入适当过量的NH4HCO3的原因是___________ 。
(4)当温度超过30℃,沉铁反应的铁沉淀率随温度升高而下降的原因是___________ 。
(5)沉铁后过滤得到FeCO3粗产品,依次用去离子水和无水乙醇各洗涤2~3次,再低温干燥,得到纯净的FeCO3,用无水乙醇洗涤的目的是___________
(6)“煅烧”时,在一定温度下加热颗粒状 。一段时间后所得产物有两种成分,其中外层产物为
。一段时间后所得产物有两种成分,其中外层产物为 ,内层产物为
,内层产物为 ,分别从
,分别从受热的温度 和接触的气体 分析,产生该现象的可能原因是___________ 。
(7)产品中 的质量分数测定:称取已干燥的产品1.000 g,将其置于500 mL锥形瓶中,加入适量的盐酸并加热使其完全反应,然后滴加足量的
的质量分数测定:称取已干燥的产品1.000 g,将其置于500 mL锥形瓶中,加入适量的盐酸并加热使其完全反应,然后滴加足量的 溶液,发生反应
溶液,发生反应 ,充分反应后,除去其中过量
,充分反应后,除去其中过量 ;再向锥形瓶中逐滴加入0.1000 mol·L-1
;再向锥形瓶中逐滴加入0.1000 mol·L-1  溶液,发生反应
溶液,发生反应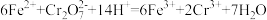 ,恰好完全反应时消耗
,恰好完全反应时消耗 溶液18.75 mL,计算产品中
溶液18.75 mL,计算产品中 的质量分数 (写出计算过程)
的质量分数 (写出计算过程)________ 。
 ,含少量
,含少量 )制备铁红的流程如下:
)制备铁红的流程如下:
(1)“焙烧”时,CO将Fe2O3还原为FeO,该过程中参加反应的还原剂与氧化剂的物质的量之比是
(2)“酸浸”时,生成
 的离子方程式为
的离子方程式为(3)“沉铁”时,除了生成
 白色沉淀,还生成一种气体,该气体为
白色沉淀,还生成一种气体,该气体为(4)当温度超过30℃,沉铁反应的铁沉淀率随温度升高而下降的原因是
(5)沉铁后过滤得到FeCO3粗产品,依次用去离子水和无水乙醇各洗涤2~3次,再低温干燥,得到纯净的FeCO3,用无水乙醇洗涤的目的是
(6)“煅烧”时,在一定温度下加热颗粒状
 。一段时间后所得产物有两种成分,其中外层产物为
。一段时间后所得产物有两种成分,其中外层产物为 ,内层产物为
,内层产物为 ,分别从
,分别从(7)产品中
 的质量分数测定:称取已干燥的产品1.000 g,将其置于500 mL锥形瓶中,加入适量的盐酸并加热使其完全反应,然后滴加足量的
的质量分数测定:称取已干燥的产品1.000 g,将其置于500 mL锥形瓶中,加入适量的盐酸并加热使其完全反应,然后滴加足量的 溶液,发生反应
溶液,发生反应 ,充分反应后,除去其中过量
,充分反应后,除去其中过量 ;再向锥形瓶中逐滴加入0.1000 mol·L-1
;再向锥形瓶中逐滴加入0.1000 mol·L-1  溶液,发生反应
溶液,发生反应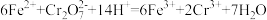 ,恰好完全反应时消耗
,恰好完全反应时消耗 溶液18.75 mL,计算产品中
溶液18.75 mL,计算产品中 的质量分数 (写出计算过程)
的质量分数 (写出计算过程)
您最近一年使用:0次
名校
8 . 下列实验操作正确的是
| A.pH试纸使用时不需要润湿,用红色石蕊试纸检测氨气时需要润湿 |
| B.用NaOH溶液和分液漏斗萃取溴水中的溴 |
C.用 溶液鉴别 溶液鉴别 溶液和 溶液和 溶液 溶液 |
D.用 溶液蒸干制备 溶液蒸干制备 固体 固体 |
您最近一年使用:0次
9 . 以下实验装置或操作(部分夹持仪器省略)正确的是
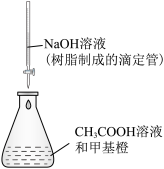 | 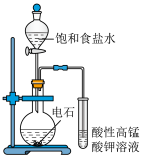 | 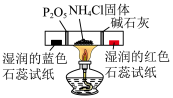 | 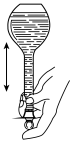 |
| A.一定浓度的NaOH溶液测定未知浓度的CH3COOH | B.检验生成的乙炔 | C.验证NH4Cl分解 | D.配一定物质的量浓度的溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
10 . 用如图所示装置(夹持装置省略)进行实验,能达到目的的是
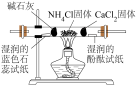 | 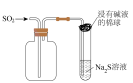 | 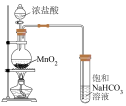 |  |
A.检验 受热分解产物 受热分解产物 | B.探究二氧化硫的氧化性 | C.验证氯气与水反应有盐酸生成 | D.制备 胶体 胶体 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



