名校
解题方法
1 . 化学变化总是伴随着能量的变化。“铝热反应”是将单质铝与金属氧化物混合物反应获得金属单质的化学反应。在野外焊接钢轨时可利用此反应。实验室中可用如图装置实现:_______ 。
(2)实验中能观察到的现象有(例举两点):_______ 。
(3)可表示铝与氧化铁反应的热效应的图是_______ 。
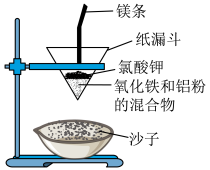
(2)实验中能观察到的现象有(例举两点):
(3)可表示铝与氧化铁反应的热效应的图是
A.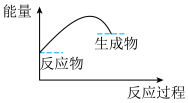 B.
B. C.
C.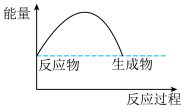
| A.铝还原性较强 | B.锰、钒熔点高 |
| C.铝能形成多种合金 | D.反应放出大量热 |
您最近一年使用:0次
名校
解题方法
2 . 将铝与氧化铁混合制备单质铁的反应称为铝热反应,反应装置如图所示:_____ 。
(2)该铝热反应的化学方程式为_____ ,引发铝热反应的实验操作是_____ 。
(3)取少量反应所得的固体混合物,将其溶于足量稀 ,滴加KSCN溶液无明显现象,能否说明固体混合物中已无
,滴加KSCN溶液无明显现象,能否说明固体混合物中已无 ,请判断并说明理由
,请判断并说明理由_____ 。
(4)写出一种铝热反应的实际应用_____ 。
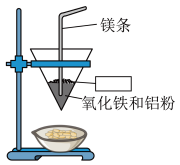
(2)该铝热反应的化学方程式为
(3)取少量反应所得的固体混合物,将其溶于足量稀
 ,滴加KSCN溶液无明显现象,能否说明固体混合物中已无
,滴加KSCN溶液无明显现象,能否说明固体混合物中已无 ,请判断并说明理由
,请判断并说明理由(4)写出一种铝热反应的实际应用
您最近一年使用:0次
名校
解题方法
3 . 钼(Mo)及其化合物广泛地应用于医疗卫生、国防等领域。某镍钼矿中的镍和钼以 和
和 形式存在,从镍钼矿中分离钼,并得到
形式存在,从镍钼矿中分离钼,并得到 的一种工艺流程。
的一种工艺流程。
已知“浸取”过程中发生如下反应: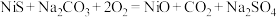
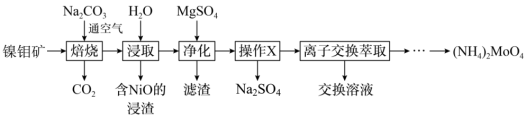
(1) 位于元素周期表第
位于元素周期表第________ 周期第________ 族。
(2)“焙烧”中生成 的反应如下所示,请配平该化学方程式
的反应如下所示,请配平该化学方程式______ 。

上述反应中共价化合物的中心原子杂化方式是________ 杂化。
(3)下列说法正确的是________。(不定项)
 用量对钼浸出率和浸取液中
用量对钼浸出率和浸取液中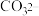 浓度的影响如左下图所示,
浓度的影响如左下图所示, 的溶解度曲线如右下图所示。
的溶解度曲线如右下图所示。

(4)分析实际生产中选择用量为理论用量1.2倍的原因是:________________ 。
(5)为充分分离 ,工艺流程中的“操作
,工艺流程中的“操作 ”应为________。
”应为________。
(6)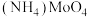 中存在的相互作用有________。
中存在的相互作用有________。
(7)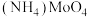 分解可得
分解可得 。高温下,用铝粉还原
。高温下,用铝粉还原 得到金属钼的化学方程式为:
得到金属钼的化学方程式为:________________ 。
 和
和 形式存在,从镍钼矿中分离钼,并得到
形式存在,从镍钼矿中分离钼,并得到 的一种工艺流程。
的一种工艺流程。已知“浸取”过程中发生如下反应:
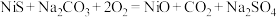

(1)
 位于元素周期表第
位于元素周期表第(2)“焙烧”中生成
 的反应如下所示,请配平该化学方程式
的反应如下所示,请配平该化学方程式
上述反应中共价化合物的中心原子杂化方式是
(3)下列说法正确的是________。(不定项)
A.电负性: | B.离子半径: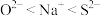 |
C.第一电离能: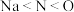 | D.基态 的简化电子排布式 的简化电子排布式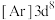 |
 用量对钼浸出率和浸取液中
用量对钼浸出率和浸取液中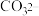 浓度的影响如左下图所示,
浓度的影响如左下图所示, 的溶解度曲线如右下图所示。
的溶解度曲线如右下图所示。
(4)分析实际生产中选择用量为理论用量1.2倍的原因是:
(5)为充分分离
 ,工艺流程中的“操作
,工艺流程中的“操作 ”应为________。
”应为________。| A.蒸发结晶 | B.低温结晶 | C.蒸馏 | D.萃取 |
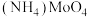 中存在的相互作用有________。
中存在的相互作用有________。| A.分子间作用力 | B.金属键 | C.共价键 | D.离子键 |
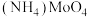 分解可得
分解可得 。高温下,用铝粉还原
。高温下,用铝粉还原 得到金属钼的化学方程式为:
得到金属钼的化学方程式为:
您最近一年使用:0次
名校
解题方法
4 . “铝热反应”是将单质铝与金属氧化物混合物反应获得金属单质的化学反应。在野外焊接钢轨时可利用此反应。实验室中可用如下装置实现:
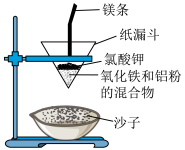
(1)写出该反应的化学方程式_______ 。
(2)实验中能观察到的现象有_______ 、_______ (例举两点)。
(3)可表示铝与氧化铁反应的热效应的图是
A .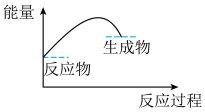 B.
B.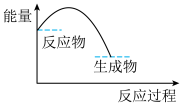 C.
C.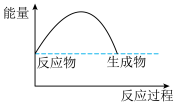
(4)工业上可用铝热反应冶炼锰、钒等金属,其原因与下列无关的是_______
(5)以下实验中属于放热反应的是_______
A.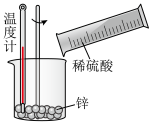 B.
B.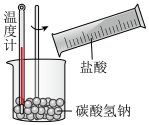 C.
C.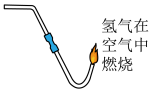

(1)写出该反应的化学方程式
(2)实验中能观察到的现象有
(3)可表示铝与氧化铁反应的热效应的图是
A .
 B.
B. C.
C.
(4)工业上可用铝热反应冶炼锰、钒等金属,其原因与下列无关的是_______
| A.铝还原性较强 | B.锰、钒熔点高 | C.铝能形成多种合金 | D.反应放出大量热 |
(5)以下实验中属于放热反应的是
A.
 B.
B. C.
C.
您最近一年使用:0次
名校
解题方法
5 . 以下是有关铝的实验探究,请回答相关问题:
(1)用铝粉和 Fe2O3做铝热反应实验,需要的试剂还有___________。
(2)镁能发生和铝类似的“镁热反应”,写出镁在高温下和 Fe2O3反应的化学方程式___________ 。
(3)向集满CO2的铝制易拉罐中加入过量 NaOH 浓溶液,立即封闭罐口,易拉罐渐渐凹瘪; 再过一段时间,罐壁又重新凸起。写出罐壁又重新凸起发生的相关离子方程式:___________ 。
(4)向铝粉中添加少量 NH4Cl固体并充分混合,将其加热到1000℃时可与 N₂反应制备 AlN,下列说法正确的是___________
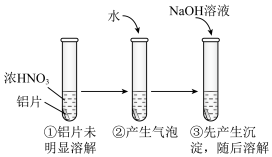
(5)用打磨过的铝片进行如下实验, 下列分析不合理的是___________
(6)为探究铝片(未打磨)与Na2CO3溶液的反应,实验如下:
下列说法不正确的是___________
(7)某铝土矿的主要成分为Al2O3·xH2O,还含有Fe2O3和 SiO2杂质。称取 17.50g铝土矿样品,加入 200mL1.65mol/L 的稀硫酸,恰好完全反应,过滤得沉淀0.30g,然后在滤液中加入足量的 NaOH 溶液,得到沉淀 2.14g。
①该试样中Fe2O3的物质的量为___________ mol。
② 样品中Al2O3·xH2O的x=__________ 。
(1)用铝粉和 Fe2O3做铝热反应实验,需要的试剂还有___________。
| A.KCl | B.KClO3 | C.MnO2 | D.Mg |
(2)镁能发生和铝类似的“镁热反应”,写出镁在高温下和 Fe2O3反应的化学方程式
(3)向集满CO2的铝制易拉罐中加入过量 NaOH 浓溶液,立即封闭罐口,易拉罐渐渐凹瘪; 再过一段时间,罐壁又重新凸起。写出罐壁又重新凸起发生的相关离子方程式:
(4)向铝粉中添加少量 NH4Cl固体并充分混合,将其加热到1000℃时可与 N₂反应制备 AlN,下列说法正确的是___________
| A.AlN是一种金属材料 |
| B.AlN与足量氢氧化钠溶液共热时生成氢氧化铝和氨气 |
| C.少量 NH4Cl能够破坏 Al表面的 Al2O3薄膜 |
| D.AlN与足量盐酸反应的离子方程式为AlN+3H+=Al3++NH3↑ |
(5)用打磨过的铝片进行如下实验, 下列分析不合理的是___________

| A.①中铝片发生了钝化 |
| B.②中产生的气泡是氮氧化合物,不是氢气 |
| C.③中沉淀溶解的离子方程式是Al(OH)3+OH-=[Al(OH)4]- |
| D.②中加水稀释过程中,仅发生了氧化还原反应 |
(6)为探究铝片(未打磨)与Na2CO3溶液的反应,实验如下:
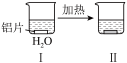 |  | |
| 无明显现象 | 铝片表面产生细小气泡 | 出现白色沉淀,产生大量气泡(经检验为H2和CO2) |
A.Na2CO3溶液中存在水解平衡:  |
| B.对比Ⅰ 、Ⅲ,推测 Na2CO3溶液能破坏铝表面的氧化膜 |
| C.Ⅳ溶液中可能存在大量 Al3+ |
D.推测出现白色浑浊的可能原因:[Al(OH)4]-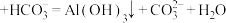 |
(7)某铝土矿的主要成分为Al2O3·xH2O,还含有Fe2O3和 SiO2杂质。称取 17.50g铝土矿样品,加入 200mL1.65mol/L 的稀硫酸,恰好完全反应,过滤得沉淀0.30g,然后在滤液中加入足量的 NaOH 溶液,得到沉淀 2.14g。
①该试样中Fe2O3的物质的量为
② 样品中Al2O3·xH2O的x=
您最近一年使用:0次
名校
6 . 铝与氧化铁混合后可称为铝热剂,以下混合物也能作为铝热剂的是
| A.氧化铝与铁 | B.氧化铝与四氧化三铁 |
| C.铝与氧化镁 | D.铝与五氧化二钒 |
您最近一年使用:0次
名校
解题方法
7 . 将铝与氧化铁混合制备单质铁的反应称为铝热反应,反应装置如图所示:

(1)空白处还需加入的试剂为___________ 。
(2)写出一种铝热反应的实际应用___________ 。

(1)空白处还需加入的试剂为
(2)写出一种铝热反应的实际应用
您最近一年使用:0次
8 . 野外焊接钢轨的原理如图所示
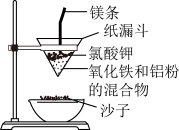
(1)写出铝粉参加反应的化学方程式:__________________ ,该反应的混合物称为:____________ 。铝能用于冶炼难熔金属,是因为:①铝还原性强,②____________
(2)反应所得块状熔融物中很可能含有金属铝,能证明含金属铝的化学试剂为:______
(3)能说明Fe粉与S粉的反应是放热反应的实验现象是:________________________
(4)原电池是把______ 能转化为______ 能的装置。
铜-锌稀硫酸原电池的总反应的离子反应方程式为__________ ;
正极的电极反应式:_____________ ;
相关判断正确的是________ ;
A.质量减轻的电极是正极 B.发生还原反应的是负极
C.锌电极是负极 D.电子从铜片流出

(1)写出铝粉参加反应的化学方程式:
(2)反应所得块状熔融物中很可能含有金属铝,能证明含金属铝的化学试剂为:
(3)能说明Fe粉与S粉的反应是放热反应的实验现象是:
(4)原电池是把
铜-锌稀硫酸原电池的总反应的离子反应方程式为
正极的电极反应式:
相关判断正确的是
A.质量减轻的电极是正极 B.发生还原反应的是负极
C.锌电极是负极 D.电子从铜片流出
您最近一年使用:0次
名校
9 . 从石器、青铜器到铁器时代,金属的冶炼体现了人类文明的进程,铁是应用最广泛的金属,被人类誉为金属之王;而铝在地壳中的含量比铁更高,居于榜首。
(1)野外铺设钢轨时,通常用铝和氧化铁混合粉末反应得到的液态铁来焊接钢轨。常用如图所示装置,下列叙述错误的是

(2)写出上述反应的化学方程式________ ,其中铝作________ 。(填“氧化剂”或“还原剂”)
(1)野外铺设钢轨时,通常用铝和氧化铁混合粉末反应得到的液态铁来焊接钢轨。常用如图所示装置,下列叙述错误的是

| A.该反应属于置换反应 |
| B.有“熔融铁珠”生成说明该反应为放热反应 |
| C.该反应的化学能全部转化为热能 |
| D.该反应中生成物的总能量小于反应物的总能量 |
您最近一年使用:0次
10 . 铁是人类较早使用的金属之一,运用所学知识,回答下列问题。
(1)Fe(OH)2很不稳定,露置在空气中容易被氧化,该反应的化学方程式为___________ ,现象为___________ 。
(2)为了获得白色的Fe(OH)2沉淀,在用硫酸亚铁晶体配置硫酸亚铁溶液时,往往会加入___________ ,目的是___________ 。
(3)Fe3+比 Fe2+稳定,请写出 Fe3+的检验过程和现象___________ ,涉及反应的离子方程式是___________ 。
(4)野外铺设钢轨时,通常用铝和氧化铁混合粉末反应得到的液态铁来焊接钢轨。写出反应的化学方程式___________ ,该反应是___________ (吸或放)热反应,其中铝发生___________ (氧化或还原)反应。
(1)Fe(OH)2很不稳定,露置在空气中容易被氧化,该反应的化学方程式为
(2)为了获得白色的Fe(OH)2沉淀,在用硫酸亚铁晶体配置硫酸亚铁溶液时,往往会加入
(3)Fe3+比 Fe2+稳定,请写出 Fe3+的检验过程和现象
(4)野外铺设钢轨时,通常用铝和氧化铁混合粉末反应得到的液态铁来焊接钢轨。写出反应的化学方程式
您最近一年使用:0次



