名校
1 . 将浓度均为0.02mol•L-1的H2O2、H2SO4、KI、Na2S2O3溶液及淀粉混合,一定时间后溶液变为蓝色。该实验是一种“碘钟实验”。某小组同学再室温下对该“碘钟实验”的原理进行探究。
资料:该“碘钟实验”的总反应为H2O2+2S2O +2H+=S4O
+2H+=S4O +2H2O,反应分两步进行,反应A:……;反应B:I2+2S2O
+2H2O,反应分两步进行,反应A:……;反应B:I2+2S2O =2I-+S4O
=2I-+S4O 。
。
(1)反应A的离子方程式是_____ ;对于总反应,I-的作用相当于_____ 。
(2)为证明反应A、B的存在,进行实验I.
实验I:
a.向酸化的H2O2溶液中加入试剂X的水溶液,溶液变为蓝色。
b.再向得到的蓝色溶液中加入Na2S2O3溶液,溶液的蓝色褪去。
试剂X是_____
(3)为探究硫酸浓度对溶液变蓝快慢的影响,进行实验Ⅱ、实验Ⅲ.
(各溶液浓度均为0.02mol•L-1)
溶液从混合时的无色变为蓝色的时间:实验Ⅱ是15min,实验Ⅲ是20min。
①实验Ⅲ中,x、y、z所对应的数值分别是_____ 。
②对比试验Ⅱ、实验Ⅲ,可得出的实验结论是_____ 。
(4)为探究其他因素对该“碘钟实验”的影响,进行实验Ⅳ.(各溶液浓度均为0.02mol•L-1)
实验过程中,溶液始终未出现变蓝的现象。试结合该“碘钟实验”总反应方程式,推测反应A与反应B速率的相对快慢关系:_____ 。
资料:该“碘钟实验”的总反应为H2O2+2S2O
 +2H+=S4O
+2H+=S4O +2H2O,反应分两步进行,反应A:……;反应B:I2+2S2O
+2H2O,反应分两步进行,反应A:……;反应B:I2+2S2O =2I-+S4O
=2I-+S4O 。
。(1)反应A的离子方程式是
(2)为证明反应A、B的存在,进行实验I.
实验I:
a.向酸化的H2O2溶液中加入试剂X的水溶液,溶液变为蓝色。
b.再向得到的蓝色溶液中加入Na2S2O3溶液,溶液的蓝色褪去。
试剂X是
(3)为探究硫酸浓度对溶液变蓝快慢的影响,进行实验Ⅱ、实验Ⅲ.
(各溶液浓度均为0.02mol•L-1)
| 用量/mL | H2O2溶液 | H2SO4溶液 | Na2S2O3溶液 | 试剂X溶液 | H2O |
| 实验Ⅱ | 5 | 4 | 8 | 3 | 0 |
| 实验Ⅲ | 5 | 2 | x | y | z |
①实验Ⅲ中,x、y、z所对应的数值分别是
②对比试验Ⅱ、实验Ⅲ,可得出的实验结论是
(4)为探究其他因素对该“碘钟实验”的影响,进行实验Ⅳ.(各溶液浓度均为0.02mol•L-1)
| 用量/mL | H2O2溶液 | H2SO4溶液 | Na2S2O3溶液 | 试剂X溶液 | H2O |
| 实验Ⅳ | 4 | 4 | 9 | 3 | 0 |
您最近一年使用:0次
2 . 通过电化学、热化学等方法,将 转化为
转化为 等化学品,是实现“双碳”目标的途径之一。请回答:
等化学品,是实现“双碳”目标的途径之一。请回答:
(1)某研究小组采用电化学方法将 转化为
转化为 ,装置如图。电极B上的电极反应式是
,装置如图。电极B上的电极反应式是_______ 。
 :
: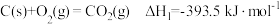
Ⅱ:
Ⅲ: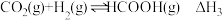
①
_______  。
。
②反应Ⅲ在恒温、恒容的密闭容器中进行, 和
和 的投料浓度均为
的投料浓度均为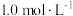 ,平衡常数
,平衡常数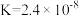 ,则
,则 的平衡转化率为
的平衡转化率为_______ 。
③用氨水吸收 ,得到
,得到 氨水和
氨水和 甲酸铵的混合溶液,
甲酸铵的混合溶液,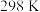 时该混合溶液的
时该混合溶液的
_______ 。[已知: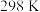 时,电离常数
时,电离常数 、
、 ]
]
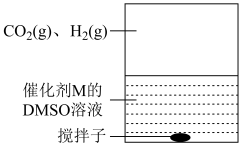
(3)为提高效率,该研究小组参考文献优化热化学方法,在如图密闭装置中充分搅拌催化剂M的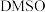 (有机溶剂)溶液,
(有机溶剂)溶液, 和
和 在溶液中反应制备
在溶液中反应制备 ,反应过程中保持
,反应过程中保持 和
和 的压强不变,总反应
的压强不变,总反应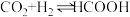 的反应速率为v,反应机理如下列三个基元反应,各反应的活化能
的反应速率为v,反应机理如下列三个基元反应,各反应的活化能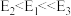 (不考虑催化剂活性降低或丧失)。
(不考虑催化剂活性降低或丧失)。
Ⅳ:

V: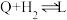

VI: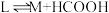

_______ 。
A.v与 的压强无关 B.v与溶液中溶解
的压强无关 B.v与溶液中溶解 的浓度无关
的浓度无关
C.温度升高,v不一定增大 D.在溶液中加入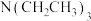 ,可提高
,可提高 转化率
转化率
②实验测得: ,
, 下,v随催化剂M浓度c变化如图。
下,v随催化剂M浓度c变化如图。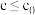 时,v随c增大而增大:
时,v随c增大而增大: 时,v不再显著增大。请解释原因
时,v不再显著增大。请解释原因_______ 。
 转化为
转化为 等化学品,是实现“双碳”目标的途径之一。请回答:
等化学品,是实现“双碳”目标的途径之一。请回答:(1)某研究小组采用电化学方法将
 转化为
转化为 ,装置如图。电极B上的电极反应式是
,装置如图。电极B上的电极反应式是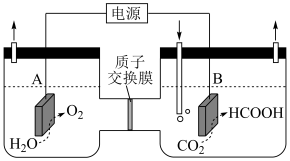
 :
: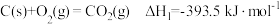
Ⅱ:

Ⅲ:
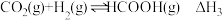
①

 。
。②反应Ⅲ在恒温、恒容的密闭容器中进行,
 和
和 的投料浓度均为
的投料浓度均为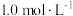 ,平衡常数
,平衡常数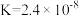 ,则
,则 的平衡转化率为
的平衡转化率为③用氨水吸收
 ,得到
,得到 氨水和
氨水和 甲酸铵的混合溶液,
甲酸铵的混合溶液,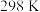 时该混合溶液的
时该混合溶液的
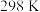 时,电离常数
时,电离常数 、
、 ]
](3)为提高效率,该研究小组参考文献优化热化学方法,在如图密闭装置中充分搅拌催化剂M的
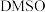 (有机溶剂)溶液,
(有机溶剂)溶液, 和
和 在溶液中反应制备
在溶液中反应制备 ,反应过程中保持
,反应过程中保持 和
和 的压强不变,总反应
的压强不变,总反应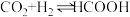 的反应速率为v,反应机理如下列三个基元反应,各反应的活化能
的反应速率为v,反应机理如下列三个基元反应,各反应的活化能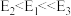 (不考虑催化剂活性降低或丧失)。
(不考虑催化剂活性降低或丧失)。Ⅳ:


V:
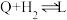

VI:
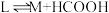

A.v与
 的压强无关 B.v与溶液中溶解
的压强无关 B.v与溶液中溶解 的浓度无关
的浓度无关C.温度升高,v不一定增大 D.在溶液中加入
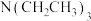 ,可提高
,可提高 转化率
转化率②实验测得:
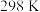 ,
, 下,v随催化剂M浓度c变化如图。
下,v随催化剂M浓度c变化如图。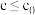 时,v随c增大而增大:
时,v随c增大而增大: 时,v不再显著增大。请解释原因
时,v不再显著增大。请解释原因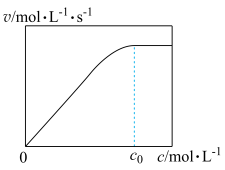
您最近一年使用:0次
2024-02-02更新
|
2167次组卷
|
3卷引用:2024年浙江高考真题化学(1月)
3 . 从富钒废渣( 、
、 、
、 )中回收
)中回收 的工艺过程可表示为
的工艺过程可表示为
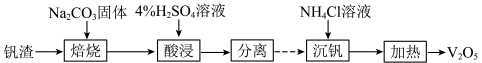
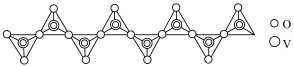
(1)“焙烧”所得钠盐的阴离子呈如图(其中钒为+5价)的无限链状结构,写出“焙烧”的化学方程式:___________ 。
(2)“沉钒”反应是向含有 的溶液中加入
的溶液中加入 溶液,析出
溶液,析出 沉淀。
沉淀。
①写出“沉钒”反应的离子方程式:___________ 。
②已知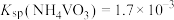 。室温下,测得“分离”后所得溶液中
。室温下,测得“分离”后所得溶液中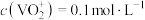 ,为使“沉钒”时钒元素的沉淀率达到99%,应使“沉钒”后的溶液中
,为使“沉钒”时钒元素的沉淀率达到99%,应使“沉钒”后的溶液中 不低于
不低于___________  。
。
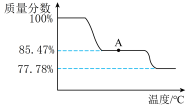
③为研究 受热发生的化学变化,某化学兴趣小组称取一定质量的
受热发生的化学变化,某化学兴趣小组称取一定质量的  在空气中加热,剩余固体质量分数(剩余固体质量/起始质量)随温度变化的曲线如图所示,则点A所得物质的化学式为
在空气中加热,剩余固体质量分数(剩余固体质量/起始质量)随温度变化的曲线如图所示,则点A所得物质的化学式为___________ 。
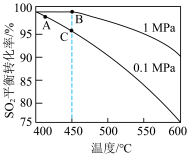
(3)一定温度下,恒压密闭容器中发生反应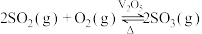 ,
, 反应温度和压强的关系如图所示。实际生产选择图中C点的反应条件,不选择A、B点的理由分别是
反应温度和压强的关系如图所示。实际生产选择图中C点的反应条件,不选择A、B点的理由分别是___________ 。
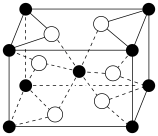
(4)还原V2O5 可以制备VO2 ,VO2的晶胞结构如图,该晶胞中矾的配位数为___________ 。
 、
、 、
、 )中回收
)中回收 的工艺过程可表示为
的工艺过程可表示为
(1)“焙烧”所得钠盐的阴离子呈如图(其中钒为+5价)的无限链状结构,写出“焙烧”的化学方程式:

(2)“沉钒”反应是向含有
 的溶液中加入
的溶液中加入 溶液,析出
溶液,析出 沉淀。
沉淀。①写出“沉钒”反应的离子方程式:
②已知
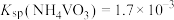 。室温下,测得“分离”后所得溶液中
。室温下,测得“分离”后所得溶液中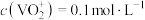 ,为使“沉钒”时钒元素的沉淀率达到99%,应使“沉钒”后的溶液中
,为使“沉钒”时钒元素的沉淀率达到99%,应使“沉钒”后的溶液中 不低于
不低于 。
。③为研究
 受热发生的化学变化,某化学兴趣小组称取一定质量的
受热发生的化学变化,某化学兴趣小组称取一定质量的  在空气中加热,剩余固体质量分数(剩余固体质量/起始质量)随温度变化的曲线如图所示,则点A所得物质的化学式为
在空气中加热,剩余固体质量分数(剩余固体质量/起始质量)随温度变化的曲线如图所示,则点A所得物质的化学式为
(3)一定温度下,恒压密闭容器中发生反应
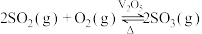 ,
, 反应温度和压强的关系如图所示。实际生产选择图中C点的反应条件,不选择A、B点的理由分别是
反应温度和压强的关系如图所示。实际生产选择图中C点的反应条件,不选择A、B点的理由分别是
(4)还原V2O5 可以制备VO2 ,VO2的晶胞结构如图,该晶胞中矾的配位数为

您最近一年使用:0次
4 . 完成下列问题
(1)已知:
反应Ⅰ:N2(g)+O2(g) 2NO(g) ΔH1=akJ/mol
2NO(g) ΔH1=akJ/mol
反应Ⅱ;2NO(g)+O2(g) 2NO2(g) ΔH2=bkJ/mol
2NO2(g) ΔH2=bkJ/mol
反应Ⅲ:2N2O(g) 2N2(g)+O2(g) ΔH3=ckJ/mol
2N2(g)+O2(g) ΔH3=ckJ/mol
反应Ⅳ:N2O(g)+NO2(g) 3NO(g) ΔH=
3NO(g) ΔH=___________ kJ/mol
(2)汽车尾气中的NO和CO可在催化剂作用下生成无污染的气体。在密闭容器中充入反应物,测得平衡时NO的体积分数与温度、压强的关系如图。
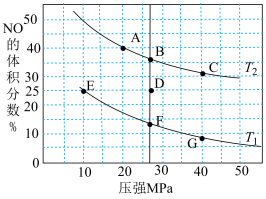
①反应2NO(g)+2CO(g) N2(g)+2CO2(g) ΔH<0,则T1
N2(g)+2CO2(g) ΔH<0,则T1___________ T2(填“>”“=”或“<”)
②该反应达到平衡后,为同时提高反应速率和NO的转化率,可采取的措施有___________ (答两点即可)。
③在D点,对反应容器降温的同时缩小体积至体系压强增大,重新达到的平衡状态可能是图中A~G点中的___________ 点。
(3)在催化剂作用下,利用反应C(s)+2NO(g) N2(g)+CO2(g) ΔH=-34.0kJ/mol,用活性炭对NO进行吸附。已知在密闭容器中加入足量的C和一定量的NO气体,保持恒容,在相同时间内测得NO的转化率随温度的变化如图所示:
N2(g)+CO2(g) ΔH=-34.0kJ/mol,用活性炭对NO进行吸附。已知在密闭容器中加入足量的C和一定量的NO气体,保持恒容,在相同时间内测得NO的转化率随温度的变化如图所示:
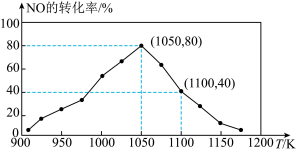
①由图可知,1050K前反应中NO的转化率随温度升高而增大,其原因为___________ ;在1050K时,CO2的体积分数为___________ 。
②用某物质的平衡分压代替其物质的量浓度也可以表示化学平衡常数(记作Kp)。在1100K、1.1×106Pa时,该反应的化学平衡常数Kp=___________ [已知:气体分压(P分)=气体总压(Pa)×体积分数]。
(4)含铈溶液可以处理大气中的氮氧化物,并可通过电解法再生。铈元素(Ce)常见的化合价有+3价、+4价。NO可以被含Ce4+的溶液吸收,生成等物质的量的 、
、 。可采用电解法将上述吸收液中等物质的量
。可采用电解法将上述吸收液中等物质的量 、
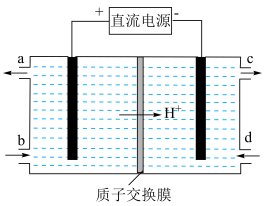
、 转化为无毒物质,其原理如图所示。阴极的电极反应式为
转化为无毒物质,其原理如图所示。阴极的电极反应式为___________ 。
(1)已知:
反应Ⅰ:N2(g)+O2(g)
 2NO(g) ΔH1=akJ/mol
2NO(g) ΔH1=akJ/mol反应Ⅱ;2NO(g)+O2(g)
 2NO2(g) ΔH2=bkJ/mol
2NO2(g) ΔH2=bkJ/mol反应Ⅲ:2N2O(g)
 2N2(g)+O2(g) ΔH3=ckJ/mol
2N2(g)+O2(g) ΔH3=ckJ/mol反应Ⅳ:N2O(g)+NO2(g)
 3NO(g) ΔH=
3NO(g) ΔH=(2)汽车尾气中的NO和CO可在催化剂作用下生成无污染的气体。在密闭容器中充入反应物,测得平衡时NO的体积分数与温度、压强的关系如图。

①反应2NO(g)+2CO(g)
 N2(g)+2CO2(g) ΔH<0,则T1
N2(g)+2CO2(g) ΔH<0,则T1②该反应达到平衡后,为同时提高反应速率和NO的转化率,可采取的措施有
③在D点,对反应容器降温的同时缩小体积至体系压强增大,重新达到的平衡状态可能是图中A~G点中的
(3)在催化剂作用下,利用反应C(s)+2NO(g)
 N2(g)+CO2(g) ΔH=-34.0kJ/mol,用活性炭对NO进行吸附。已知在密闭容器中加入足量的C和一定量的NO气体,保持恒容,在相同时间内测得NO的转化率随温度的变化如图所示:
N2(g)+CO2(g) ΔH=-34.0kJ/mol,用活性炭对NO进行吸附。已知在密闭容器中加入足量的C和一定量的NO气体,保持恒容,在相同时间内测得NO的转化率随温度的变化如图所示:
①由图可知,1050K前反应中NO的转化率随温度升高而增大,其原因为
②用某物质的平衡分压代替其物质的量浓度也可以表示化学平衡常数(记作Kp)。在1100K、1.1×106Pa时,该反应的化学平衡常数Kp=
(4)含铈溶液可以处理大气中的氮氧化物,并可通过电解法再生。铈元素(Ce)常见的化合价有+3价、+4价。NO可以被含Ce4+的溶液吸收,生成等物质的量的
 、
、 。可采用电解法将上述吸收液中等物质的量
。可采用电解法将上述吸收液中等物质的量 、
、 转化为无毒物质,其原理如图所示。阴极的电极反应式为
转化为无毒物质,其原理如图所示。阴极的电极反应式为
您最近一年使用:0次
名校
解题方法
5 . I.近年来,研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储。过程如下:
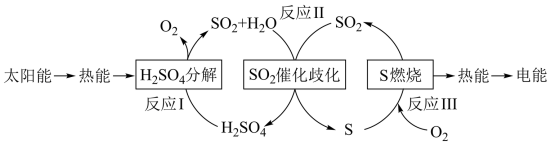
(1)反应Ⅰ:2H2SO4(l)=2SO2(g)+2H2O(g)+O2(g) ΔH1=+551 kJ·mol-1
反应Ⅲ:S(s)+O2(g)=SO2(g) ΔH3=-297 kJ·mol-1
反应Ⅱ的热化学方程式:___________ 。
(2)对反应Ⅱ,在某一投料比时,两种压强下,H2SO4在平衡体系中物质的量分数随温度的变化关系如图所示。

p2___________ p 1(填“>”或“<”),得出该结论的理由是___________ 。
(3)I-可以作为水溶液中SO2歧化反应的催化剂,可能的催化过程如下。将ii补充完整。
i.SO2+4I-+4H+=S↓+2I2+2H2O
ii.________
I2+2H2O+___________=___________+___________+2 I-
(4)探究i、ii反应速率与SO2歧化反应速率的关系,实验如下:分别将18 mL SO2饱和溶液加入到2 mL下列试剂中,密闭放置观察现象。(已知:I2易溶解在KI溶液中)
①B是A的对比实验,则a=___________ 。
②比较A、B、C,可得出的结论是___________ 。
③实验表明,SO2的歧化反应速率D>A,结合i、ii反应速率解释原因:___________
(5)一定温度下,反应I2(g)+H2(g)⇌2Hl(g)在密闭容器中达到平衡时,测得c(I2)=0.11mmol•L-1,c(H2)=0.11mmol•L-1,c(HI)=0.78mmol•L-1.相同度温下,按下列4组初始浓度进行实验,反应逆向进行的是___________ 。
(注:1mmol•L-1=10-3mol•L-1)
Ⅱ.以银锰精矿(主要含Ag2S、MnS、FeS2)和氧化锰矿(主要含MnO2)为原料联合提取银和锰的一种流程示意图如下。
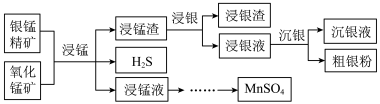
已知:酸性条件下,MnO2的氧化性强于Fe3+。
“浸银”时,使用过量FeCl3、HCl和CaCl2的混合液作为浸出剂,将Ag2S中的银以[AgCl2]-形式浸出。
(6)将“浸银”反应的离子方程式补充完整:_______
□Fe3+ + Ag2S + □ ___________ □ ___________ + 2[AgCl2]- + S
□ ___________ + 2[AgCl2]- + S
(7)结合平衡移动原理,解释浸出剂中Cl-、H+的作用:___________ 。

(1)反应Ⅰ:2H2SO4(l)=2SO2(g)+2H2O(g)+O2(g) ΔH1=+551 kJ·mol-1
反应Ⅲ:S(s)+O2(g)=SO2(g) ΔH3=-297 kJ·mol-1
反应Ⅱ的热化学方程式:
(2)对反应Ⅱ,在某一投料比时,两种压强下,H2SO4在平衡体系中物质的量分数随温度的变化关系如图所示。

p2
(3)I-可以作为水溶液中SO2歧化反应的催化剂,可能的催化过程如下。将ii补充完整。
i.SO2+4I-+4H+=S↓+2I2+2H2O
ii.
I2+2H2O+___________=___________+___________+2 I-
(4)探究i、ii反应速率与SO2歧化反应速率的关系,实验如下:分别将18 mL SO2饱和溶液加入到2 mL下列试剂中,密闭放置观察现象。(已知:I2易溶解在KI溶液中)
| 序号 | A | B | C | D |
| 试剂组成 | 0.4 mol·L-1 KI | a mol·L-1 KI 0.2 mol·L-1 H2SO4 | 0.2 mol·L-1 H2SO4 | 0.2 mol·L-1 KI 0.0002 mol I2 |
| 实验现象 | 溶液变黄,一段时间后出现浑浊 | 溶液变黄,出现浑浊较A快 | 无明显现象 | 溶液由棕褐色很快褪色,变成黄色,出现浑浊较A快 |
②比较A、B、C,可得出的结论是
③实验表明,SO2的歧化反应速率D>A,结合i、ii反应速率解释原因:
(5)一定温度下,反应I2(g)+H2(g)⇌2Hl(g)在密闭容器中达到平衡时,测得c(I2)=0.11mmol•L-1,c(H2)=0.11mmol•L-1,c(HI)=0.78mmol•L-1.相同度温下,按下列4组初始浓度进行实验,反应逆向进行的是
| A | B | C | D | |
| c(I2)/mmol•L-1 | 1.00 | 0.22 | 0.44 | 0.11 |
| c(H2)/mmol•L-1 | 1.00 | 0.22 | 0.44 | 0.44 |
| c(HI)/mmol•L-1 | 1.00 | 1.56 | 4.00 | 1.56 |
Ⅱ.以银锰精矿(主要含Ag2S、MnS、FeS2)和氧化锰矿(主要含MnO2)为原料联合提取银和锰的一种流程示意图如下。

已知:酸性条件下,MnO2的氧化性强于Fe3+。
“浸银”时,使用过量FeCl3、HCl和CaCl2的混合液作为浸出剂,将Ag2S中的银以[AgCl2]-形式浸出。
(6)将“浸银”反应的离子方程式补充完整:
□Fe3+ + Ag2S + □ ___________
 □ ___________ + 2[AgCl2]- + S
□ ___________ + 2[AgCl2]- + S(7)结合平衡移动原理,解释浸出剂中Cl-、H+的作用:
您最近一年使用:0次
解题方法
6 . 回答下列问题。
Ⅰ.某实验小组用 100mL0.50mol·L-1NaOH 溶液与 60mL0.50mol·L-1 硫酸溶液进行中和热的测定,装置如图1所示。回答下列问题:
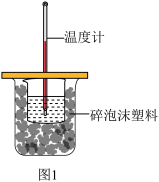
(1)图中装置缺少的仪器是___________ 。
(2)硫酸稍过量的原因是___________ 。
(3)某小组同学实验数据记录如下表,若近似认为 0.50mol•L-1NaOH 溶液与 0.50mol•L-1硫酸溶液的密度都是1g•cm-3,中和后生成溶液的比热容 c=4.18J•g-1•℃-1,则上述实验测得的中和热△H =___________ (结果保留至小数点后一位)。
(4)上述实验测得中和热的数值小于 57.3kJ·mol-1,产生偏差的原因可能是___________(填字母)。
Ⅱ.甲、乙两位同学探究外界条件对化学反应速率的影响。
【实验原理】反应:Na2S2O3+H2SO4=Na2SO4+SO2↑+S↓+H2O,反应过程中溶液出现乳白色浑浊和有刺激性气味的 气体。
【实验用品】0.1mol/LNa2S2O3溶液、0.1mol/LH2SO4溶液、蒸馏水、试管、烧杯、量筒、胶头滴管等。
实验一:甲同学利用如图装置测定化学反应速率。
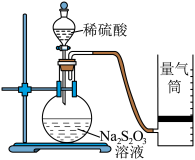
(5)为保证实验的准确性和可靠性,利用该装置进行实验前应先进行的操作是___________ 。除如图所示的实验用品外,还需要的实验仪器 是___________ 。
(6)若在 2min 时收集到 224mL(已折算成标准状况)气体,可计算出在 2min 内的反应速率v(H+)=0.02mol/(L·min),而该速率值比实际值偏小,其原因是_____________________ 。
实验二:乙同学得到各组实验数据如下表。
(7)实验Ⅰ、Ⅱ探究___________ 对化学反应速率的影响,a=___________ ,V=___________ 。
(8)实验Ⅱ、Ⅲ探究温度对化学反应速率的影响。实验表明,实验Ⅲ的反应速率最快,支持这一结论的实验现象是___________ 。
Ⅰ.某实验小组用 100mL0.50mol·L-1NaOH 溶液与 60mL0.50mol·L-1 硫酸溶液进行中和热的测定,装置如图1所示。回答下列问题:

(1)图中装置缺少的仪器是
(2)硫酸稍过量的原因是
(3)某小组同学实验数据记录如下表,若近似认为 0.50mol•L-1NaOH 溶液与 0.50mol•L-1硫酸溶液的密度都是1g•cm-3,中和后生成溶液的比热容 c=4.18J•g-1•℃-1,则上述实验测得的中和热△H =
| 实验序号 | 起始温度t1/℃ | 终止温度T2/℃ | 平均温度差(t2-t1)/℃ | ||
| HCl | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | _____ |
| 2 | 27.0 | 27.2 | 27.1 | 33.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 | |
| A.量取 NaOH 溶液时仰视读数 |
| B.为了使反应充分,向酸溶液中分次加入碱溶液 |
| C.实验装置保温隔热效果差 |
| D.用铜丝代替玻璃搅拌器搅拌 |
Ⅱ.甲、乙两位同学探究外界条件对化学反应速率的影响。
【实验原理】反应:Na2S2O3+H2SO4=Na2SO4+SO2↑+S↓+H2O,反应过程中溶液出现乳白色浑浊和有刺激性气味的 气体。
【实验用品】0.1mol/LNa2S2O3溶液、0.1mol/LH2SO4溶液、蒸馏水、试管、烧杯、量筒、胶头滴管等。
实验一:甲同学利用如图装置测定化学反应速率。

(5)为保证实验的准确性和可靠性,利用该装置进行实验前应先进行的操作是
(6)若在 2min 时收集到 224mL(已折算成标准状况)气体,可计算出在 2min 内的反应速率v(H+)=0.02mol/(L·min),而该速率值比实际值偏小,其原因是
实验二:乙同学得到各组实验数据如下表。
| 实验编号 | Na2S2O3溶液 | H2SO4溶液 | 蒸馏水 | |||
| 浓度/(mol/L) | 体积/mL | 浓度/(mol/L) | 体积/mL | 体积/mL | 温度/℃ | |
| I | 0.1 | 3.0 | 0.1 | 3.0 | V | 20 |
| Ⅱ | 0.1 | 5.0 | 0.1 | 3.0 | 0 | a |
| Ⅲ | 0.1 | 5.0 | 0.1 | 3.0 | 0 | 30 |
(8)实验Ⅱ、Ⅲ探究温度对化学反应速率的影响。实验表明,实验Ⅲ的反应速率最快,支持这一结论的实验现象是
您最近一年使用:0次
名校
7 . FeCl3是中学化学常用试剂,在化学实验中有广泛应用。
(1)已知: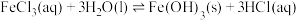 。配制一定浓度FeCl3溶液时,将FeCl3固体溶于浓盐酸中,加入蒸馏水稀释至指定浓度。盐酸的作用是
。配制一定浓度FeCl3溶液时,将FeCl3固体溶于浓盐酸中,加入蒸馏水稀释至指定浓度。盐酸的作用是___________ 。
(2)探究外界条件对双氧水分解速率的影响,设计如下实验(忽略溶液混合时的体积变化):
①实验Ⅱ中,V=___________ 。
②根据实验Ⅱ、Ⅲ中b>c不能确认 对双氧水分解催化效率小于
对双氧水分解催化效率小于 ,其原因是
,其原因是___________ 。
③为了探究温度对H2O2分解速率的影响,宜选择实验___________ (填序号)。
(3)向 溶液中滴加1滴KSCN溶液,将溶液分成甲、乙、丙、丁四份,进一步进行如下实验:
溶液中滴加1滴KSCN溶液,将溶液分成甲、乙、丙、丁四份,进一步进行如下实验:
①丙中不形成AgSCN沉淀,则丙中可观察到溶液颜色___________ (填“变深”“变浅”或“不变”)。
②甲的作用是___________ ;由丁中实验现象可得出的结论是___________ 。
(4)为探究FeCl3溶液和KI溶液反应,设计实验装置如图所示。

①实验Ⅳ中,电流表指针___________ (填“向左”“向右”或“不”)偏转。由此可推知,上述反应是可逆反应,其判断依据是___________ 。
②实验Ⅳ发生反应的离子方程式为___________ 。
(1)已知:
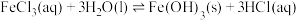 。配制一定浓度FeCl3溶液时,将FeCl3固体溶于浓盐酸中,加入蒸馏水稀释至指定浓度。盐酸的作用是
。配制一定浓度FeCl3溶液时,将FeCl3固体溶于浓盐酸中,加入蒸馏水稀释至指定浓度。盐酸的作用是(2)探究外界条件对双氧水分解速率的影响,设计如下实验(忽略溶液混合时的体积变化):
| 实验 | 30%双氧水/mL | 温度/℃ | 添加物质 | 加入蒸馏水/mL | 收集10mLO2用时/min |
| Ⅰ | 20 | 30 | 无 | 4 | a |
| Ⅱ | 20 | 30 | 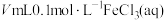 | 2 | b |
| Ⅲ | 20 | 30 |  | 2 | c |
| Ⅳ | 20 | 40 | 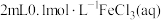 | 2 | d |
②根据实验Ⅱ、Ⅲ中b>c不能确认
 对双氧水分解催化效率小于
对双氧水分解催化效率小于 ,其原因是
,其原因是③为了探究温度对H2O2分解速率的影响,宜选择实验
(3)向
 溶液中滴加1滴KSCN溶液,将溶液分成甲、乙、丙、丁四份,进一步进行如下实验:
溶液中滴加1滴KSCN溶液,将溶液分成甲、乙、丙、丁四份,进一步进行如下实验:| 代号 | 加入少量物质 | 溶液颜色变化 |
| 甲 | 无 | 仍为红色 |
| 乙 | 1gNaOH(s) | 变浅 |
| 丙 | 1gAgNO3(s) | ? |
| 丁 | 1gFeCl3(s) | 变深 |
②甲的作用是
(4)为探究FeCl3溶液和KI溶液反应,设计实验装置如图所示。

| 步骤 | 操作及现象 | 测定数据 |
| Ⅰ | 向烧杯中加入如图所示试剂,左侧烧杯液体颜色变浅,右侧烧杯液体变为棕色,电流表指针向左偏转 | 测得电流强度为a(a>0) |
| Ⅱ | 随后,左侧烧杯液体变浅绿色,右侧烧杯液体棕色加深 | 测得电流强度为b(b<a) |
| Ⅲ | 一段时间后,指针回到零 | 测得电流强度为0 |
| Ⅳ | 在左侧烧杯中加入少量FeCl2(s),电流表指针偏转 | 测得电流强度为x |
②实验Ⅳ发生反应的离子方程式为
您最近一年使用:0次
2023-10-09更新
|
67次组卷
|
2卷引用:安徽省部分重点中学2023-2024学年高二上学期10月大联考化学试题
22-23高一下·上海浦东新·期末
名校
8 . 某实验小组为探究外界条件对化学反应速率的影响进行如下实验:
实验1:探究常温下影响等质量金属与酸反应生成氢气速率的因素:
(1)实验Ⅰ、Ⅱ探究的是_______ 对反应速率的影响。
(2)实验Ⅰ、Ⅲ及相应实验现象得到的结论是_______ 。
(3)甲同学在进行实验Ⅲ时又加入了少量硫酸铜固体,发现生成气体速率明显加快,试分析其原因:_______ 。
实验2:探究影响反应 的因素。
的因素。
(4)表中
_______ 。
(5)通过实验Ⅳ和实验Ⅵ可探究_______ 对化学反应速率的影响。
(6)该小组同学依据实Ⅴ条件进行反应并测定其化学反应速率,所得数据如图所示。

 内用
内用 表示的平均反应速率为
表示的平均反应速率为_______  。
。
实验1:探究常温下影响等质量金属与酸反应生成氢气速率的因素:
| 实验编号 | 金属 | c(酸)/ | 溶液体积/mL |
| Ⅰ | 铁粉 |  硫酸 硫酸 | 10 |
| Ⅱ | 铁粉 |  盐酸 盐酸 | 10 |
| Ⅲ | 铁块 |  硫酸 硫酸 | 10 |
(2)实验Ⅰ、Ⅲ及相应实验现象得到的结论是
(3)甲同学在进行实验Ⅲ时又加入了少量硫酸铜固体,发现生成气体速率明显加快,试分析其原因:
实验2:探究影响反应
 的因素。
的因素。| 实验编号 |  溶液的体积mL 溶液的体积mL | 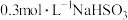 溶液的体积mL 溶液的体积mL | 水的体积/mL | 反应温度 |
| Ⅳ | 10 | 10 | 0 | 25℃ |
| Ⅴ | 10 | 5 | a | 25℃ |
| Ⅵ | 10 | 10 | 0 | 60℃ |

(5)通过实验Ⅳ和实验Ⅵ可探究
(6)该小组同学依据实Ⅴ条件进行反应并测定其化学反应速率,所得数据如图所示。

 内用
内用 表示的平均反应速率为
表示的平均反应速率为 。
。
您最近一年使用:0次
名校
解题方法
9 . 燃煤烟气中主要成分是空气,SO2和NO的含量小于1%。一种用CO(NH2)2(尿素)和H2O2在固体催化剂作用下脱硫、脱硝。其流程如下:

(1)CO(NH2)2可以水解生成(NH4)2CO3,CO(NH2)2、(NH4)2CO3与烟气中的NO不反应。脱硫后所得吸收液中含CO(NH2)2、(NH4)2SO3、(NH4)2SO4。其他条件一定,反应相同时间,测得SO2的脱除率与温度的关系如图1所示。30~70℃时,SO2的脱除率随温度升高先增大后减小的原因是___________ 。

(2)烟气中的NO与O2反应缓慢。雾化后的H2O2在催化剂中Fe元素作用下可以产生具有极强氧化活性的·OH(羟基自由基),·OH能将NO快速氧化为NO2、HNO3等物质。H2O2在一种固体催化剂表面转化的过程如图2所示:

①脱硝时,NO2与吸收液中(NH4)2SO3反应生成(NH4)2SO4,同时排放出的气体不会污染空气。写出脱硝时NO2与(NH4)2SO3反应的化学方程式:___________ 。
②化学式为LaFeO2.6的催化剂中,Fe3+和Fe2+的物质的量之比为___________ 。
(3)如不使用固体催化剂,用含Fe3+的溶液也能催化H2O2发生类似的转化生成·OH,且相同条件下速率更快。与使用含Fe3+的溶液相比,使用固体催化剂的优点是___________ 。

(1)CO(NH2)2可以水解生成(NH4)2CO3,CO(NH2)2、(NH4)2CO3与烟气中的NO不反应。脱硫后所得吸收液中含CO(NH2)2、(NH4)2SO3、(NH4)2SO4。其他条件一定,反应相同时间,测得SO2的脱除率与温度的关系如图1所示。30~70℃时,SO2的脱除率随温度升高先增大后减小的原因是

(2)烟气中的NO与O2反应缓慢。雾化后的H2O2在催化剂中Fe元素作用下可以产生具有极强氧化活性的·OH(羟基自由基),·OH能将NO快速氧化为NO2、HNO3等物质。H2O2在一种固体催化剂表面转化的过程如图2所示:

①脱硝时,NO2与吸收液中(NH4)2SO3反应生成(NH4)2SO4,同时排放出的气体不会污染空气。写出脱硝时NO2与(NH4)2SO3反应的化学方程式:
②化学式为LaFeO2.6的催化剂中,Fe3+和Fe2+的物质的量之比为
(3)如不使用固体催化剂,用含Fe3+的溶液也能催化H2O2发生类似的转化生成·OH,且相同条件下速率更快。与使用含Fe3+的溶液相比,使用固体催化剂的优点是
您最近一年使用:0次
名校
解题方法
10 . 某化学小组为了研究外界条件对化学反应速率的影响,进行了如下实验:
【实验原理】
【实验内容及记录】
(1)请完成此实验设计,其中:
_____________ 。
(2)探究浓度对化学反应速率的影响,应选择_____________ (填实验编号)。
(3)根据上表中实验①、③的数据,可以得到的结论是_______________________________________ 。
(4)该小组同学根据经验绘制了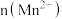 随时间变化的趋势如图1所示,但有同学查阅已有的实验资料发现,该实验过程中
随时间变化的趋势如图1所示,但有同学查阅已有的实验资料发现,该实验过程中 随时间变化的实际趋势如图2所示。
随时间变化的实际趋势如图2所示。

该小组同学根据图2所示信息提出了新的假设,并设计以下实验方案继续进行实验探究。
①该小组同学提出的假设是_________________________________________________________________ 。
②若该小组同学提出的假设成立,t的大小范围是_____________ 。
(5)某研究小组同学要测定市售草酸晶体样品的纯度,先称取5.0g样品配成100mL溶液,分别量取25.00mL溶液于锥形瓶中,用0.2mol/L 标准溶液滴定,滴定到达终点的现象是
标准溶液滴定,滴定到达终点的现象是________ ,若三次滴定消耗 标准溶液的平均体积为25.00mL,则该草酸样品的纯度为
标准溶液的平均体积为25.00mL,则该草酸样品的纯度为_____________ 。
【实验原理】

【实验内容及记录】
实验编号 | 实验温度 | 试管中所加试剂及其用量/mL | 溶液褪至无色所需时间/min | |||
0.6mol/L
|
| 3mol/L 稀 | 0.05mol/L
| |||
① | 25 | 5.0 | 3.0 | 2.0 | 5.0 | 1.4 |
② | 25 | 4.0 |
| 2.0 | 5.0 | 2.6 |
③ | 50 | 5.0 | 3.0 | 2.0 | 5.0 | 0.9 |

(2)探究浓度对化学反应速率的影响,应选择
(3)根据上表中实验①、③的数据,可以得到的结论是
(4)该小组同学根据经验绘制了
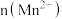 随时间变化的趋势如图1所示,但有同学查阅已有的实验资料发现,该实验过程中
随时间变化的趋势如图1所示,但有同学查阅已有的实验资料发现,该实验过程中 随时间变化的实际趋势如图2所示。
随时间变化的实际趋势如图2所示。
该小组同学根据图2所示信息提出了新的假设,并设计以下实验方案继续进行实验探究。
实验编号 | 实验温度/℃ | 试管中所加试剂及其用量/mL | 再向试管中加入某种固体 | 溶液褪至无色所需时间/min | |||
0.6mol/L
|
| 3mol/L 稀 | 0.05mol/L | ||||
④ | 25 | 5.0 | 3.0 | 2.0 | 5.0 |
| t |
②若该小组同学提出的假设成立,t的大小范围是
(5)某研究小组同学要测定市售草酸晶体样品的纯度,先称取5.0g样品配成100mL溶液,分别量取25.00mL溶液于锥形瓶中,用0.2mol/L
 标准溶液滴定,滴定到达终点的现象是
标准溶液滴定,滴定到达终点的现象是 标准溶液的平均体积为25.00mL,则该草酸样品的纯度为
标准溶液的平均体积为25.00mL,则该草酸样品的纯度为
您最近一年使用:0次

 溶液
溶液
 溶液
溶液



