(I)小明同学想通过比较两种最高价氧化物水化物的酸性强弱来验证S与C的非金属性的强弱,他查阅了资料:可以利用强酸制备弱酸的原理来判断酸性强弱。于是小明采用了下图所示的装置进行实验。请回答:

(1)仪器A的名称是________ ,应盛放下列药品中的__________ 。
a.稀硫酸 b.亚硫酸 c.氢硫酸 d.盐酸
(2)仪器B的名称是________ ,应盛放下列药品中的__________ 。
a.碳酸钙 b.硫酸钠 c.氯化钠 d.碳酸钠
(3)仪器C中盛放的药品是澄清石灰水,如果看到的现象是澄清石灰水变浑浊,证明B中发生反应生成了_____________ ,即可说明H2SO4 比H2CO3 酸性强,非金属性S比C强,B中发生反应的离子方程式为______________________________ 。
(II)(1)用电子式表示下列化合物的形成过程:
CaF2:_____________________________________________
H2S:______________________________________________
(2)有下列物质:①NaOH ②I2 ③MgCl2 ④Na2O2 ⑤氩气 回答下列问题:
①不存在化学键的是_________________________ ,
②既存在离子键又存在极性键的是__________________ 。

(1)仪器A的名称是
a.稀硫酸 b.亚硫酸 c.氢硫酸 d.盐酸
(2)仪器B的名称是
a.碳酸钙 b.硫酸钠 c.氯化钠 d.碳酸钠
(3)仪器C中盛放的药品是澄清石灰水,如果看到的现象是澄清石灰水变浑浊,证明B中发生反应生成了
(II)(1)用电子式表示下列化合物的形成过程:
CaF2:
H2S:
(2)有下列物质:①NaOH ②I2 ③MgCl2 ④Na2O2 ⑤氩气 回答下列问题:
①不存在化学键的是
②既存在离子键又存在极性键的是
更新时间:2020-04-13 20:13:40
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】①在实验室里,要证明钠、镁、铝的金属性依次减弱的实验,除钠、镁、铝以外,还需的试剂为______ 。
②在实验室里,要做证明Cl、Br、I的非金属性依次减弱的实验,所需的试剂除:NaCl溶液,NaBr溶液,KI溶液外,还需要的试剂为______ 。反应的离子方程式为:______
②在实验室里,要做证明Cl、Br、I的非金属性依次减弱的实验,所需的试剂除:NaCl溶液,NaBr溶液,KI溶液外,还需要的试剂为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】Ⅰ、某实验小组同学进行如下实验,以检验化学反应中的能量变化。请回答下列问题:
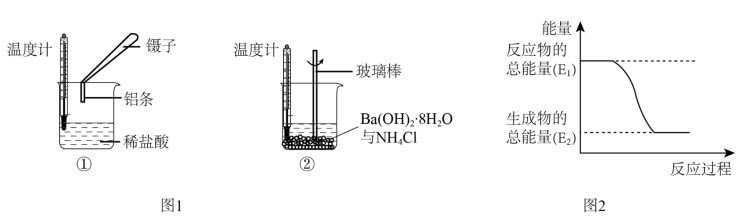
(1)实验中发现,反应后①中的温度升高;②中的温度降低.由此判断铝条与盐酸的反应是________ ,Ba(OH)2•8H2O与NH4Cl的反应是________ .反应过程________ (填“①”或“②”)的能量变化可用图2表示。
(2)现有如下两个反应:A、NaOH+HCl=NaCl+H2O;B、2FeCl3+Cu=2FeCl2+CuCl2,以上两个反应能设计成原电池的是________ ,负极材料为:________ ,电解质溶液为:________ ,负极的电极反应式为:________ 。
Ⅱ、某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验。利用如图装置可验证同主族元素非金属性的变化规律

(1)仪器A的名称为________ ,干燥管D的作用为________ 。
(2)若要证明非金属性:Cl>I,则A中加浓盐酸,B中加KMnO4(KMnO4与浓盐酸常温下反应生成氯气),C中加淀粉碘化钾混合溶液,观察到C中溶液________ (填现象)即可证明。从环境保护的观点考虑,此装置缺少尾气处理装置,可用NaOH溶液吸收尾气。
(3)若要证明非金属性:C>Si,则在A中加盐酸、B中加CaCO3、C中可加________ 溶液,观察到C中溶液________ (填现象),即可证明,反应的离子方程式为:________ ,但有的同学认为该实验不严谨,应在两装置间添加装有________ 溶液的洗气瓶,目的是________ 。

(1)实验中发现,反应后①中的温度升高;②中的温度降低.由此判断铝条与盐酸的反应是
(2)现有如下两个反应:A、NaOH+HCl=NaCl+H2O;B、2FeCl3+Cu=2FeCl2+CuCl2,以上两个反应能设计成原电池的是
Ⅱ、某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验。利用如图装置可验证同主族元素非金属性的变化规律

(1)仪器A的名称为
(2)若要证明非金属性:Cl>I,则A中加浓盐酸,B中加KMnO4(KMnO4与浓盐酸常温下反应生成氯气),C中加淀粉碘化钾混合溶液,观察到C中溶液
(3)若要证明非金属性:C>Si,则在A中加盐酸、B中加CaCO3、C中可加
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】某同学做同周期元素性质递变规律实验时,自己设计了一套实验方案,并记录了有关实验现象如下表。
请你帮助该同学整理并完成实验报告。
实验目的:验证同周期元素金属性、非金属性的变化规律。
实验用品:略。
实验报告:
(1)实验内容:(在下表空格横线处填写实验步骤标号对应的实验现象,并写出有关的离子方程式 )
(2)实验结论:_______ 。
| 实验方案 | 实验现象 |
| ①用砂纸打磨后的镁带与沸水反应,再向反应液中滴加少量酚酞溶液 | 产生气体,气体可燃,溶液变浅红色 |
②向新制的 饱和溶液中滴加新制氯水 饱和溶液中滴加新制氯水 | |
| ③钠与滴有酚酞试液的冷水反应 | 浮于水面,熔成小球,四处游动,逐渐缩小,溶液变红色 |
④镁带与 的盐酸反应 的盐酸反应 | 剧烈反应,产生的气体可燃 |
⑤铝条与 的盐酸反应 的盐酸反应 | 反应不十分强烈,产生的气体可燃 |
⑥向 溶液中滴加浓氨水溶液至过量 溶液中滴加浓氨水溶液至过量 |
请你帮助该同学整理并完成实验报告。
实验目的:验证同周期元素金属性、非金属性的变化规律。
实验用品:略。
实验报告:
(1)实验内容:(在下表空格横线处填写实验步骤标号对应的实验现象,并写出有关的
| 实验步骤 | 实验现象 | 有关离子方程式 |
| ① | 不填 | |
| ② | 不填 | |
| ③ | 不填 | |
| ④ | 不填 | 不填 |
| ⑤ | 不填 | 不填 |
| ⑥ |
(2)实验结论:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】下列叙述正确的是________ 。
A.带相反电荷离子之间的相互吸引称为离子键
B.金属元素与非金属元素化合时,不一定形成离子键
C.某元素的原子最外层只有一个电子,它跟卤素结合时所形成的化学键不一定是离子键
D.非金属原子间不可能形成离子键,只含有非金属元素的化合物不可能是离子化合物
E.离子化合物中一定含有金属元素,含金属元素的化合物一定是离子化合物
F.离子键只存在于离子化合物中,离子化合物中一定含有离子键,不可能含有非极性键
G.强酸、强碱和大多数盐都属于离子化合物
H.离子化合物受热熔化破坏化学键,吸收热量,属于化学变化
I.NaCl和CsCl晶体中,每个离子周围带相反电荷离子的数目分别是6和8,由此可以说明离子键有饱和性
A.带相反电荷离子之间的相互吸引称为离子键
B.金属元素与非金属元素化合时,不一定形成离子键
C.某元素的原子最外层只有一个电子,它跟卤素结合时所形成的化学键不一定是离子键
D.非金属原子间不可能形成离子键,只含有非金属元素的化合物不可能是离子化合物
E.离子化合物中一定含有金属元素,含金属元素的化合物一定是离子化合物
F.离子键只存在于离子化合物中,离子化合物中一定含有离子键,不可能含有非极性键
G.强酸、强碱和大多数盐都属于离子化合物
H.离子化合物受热熔化破坏化学键,吸收热量,属于化学变化
I.NaCl和CsCl晶体中,每个离子周围带相反电荷离子的数目分别是6和8,由此可以说明离子键有饱和性
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】根据要求回答下列问题:
I. 写出下列物质或微粒的电子式:
(1)CO2_________________
(2)N2__________________
(3) Na2O_____________
(4)NaOH________________
II. 下列物质:①CaBr2 ②H2O ③NH4Cl ④H2O2 ⑤Na2O2 ⑥Ca(OH)2 ⑦HClO ⑧ I2 ⑨He
(1)含有共价键的离子化合物是(用序号回答)_____________
含有共价键的共价化合物是(用序号回答)_______________
(2)当其熔化时,不破坏化学键的是(用序号回答)______________ .
I. 写出下列物质或微粒的电子式:
(1)CO2
(2)N2
(3) Na2O
(4)NaOH
II. 下列物质:①CaBr2 ②H2O ③NH4Cl ④H2O2 ⑤Na2O2 ⑥Ca(OH)2 ⑦HClO ⑧ I2 ⑨He
(1)含有共价键的离子化合物是(用序号回答)
含有共价键的共价化合物是(用序号回答)
(2)当其熔化时,不破坏化学键的是(用序号回答)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】Ⅰ.下面是同学们熟悉的物质:
①O2 ②H2SO4 ③NaBr ④NH4Cl ⑤NaHSO4 ⑥Ne ⑦Na2O2 ⑧NaOH
(1)这些物质中,既含有共价键又含有离子键的是_________ ;不存在化学键的是____ 。(填序号)
(2)属于共价化合物的是________ ;属于离子化合物的是________ 。(填序号)
(3)将NaHSO4固体溶于水,破坏了NaHSO4中的_______ (填化学键类型),NaHSO4在熔融状态下电离,破坏了NaHSO4中的________ (填化学键类型)。
Ⅱ.氯化铝的物理性质非常特殊,如:氯化铝的熔点为190℃(2.02×105Pa),但在180℃就开始升华。据此判断,氯化铝是___________ (填“共价化合物”或“离子化合物”),可以证明你的判断正确的实验依据是__________________ 。
①O2 ②H2SO4 ③NaBr ④NH4Cl ⑤NaHSO4 ⑥Ne ⑦Na2O2 ⑧NaOH
(1)这些物质中,既含有共价键又含有离子键的是
(2)属于共价化合物的是
(3)将NaHSO4固体溶于水,破坏了NaHSO4中的
Ⅱ.氯化铝的物理性质非常特殊,如:氯化铝的熔点为190℃(2.02×105Pa),但在180℃就开始升华。据此判断,氯化铝是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】(1)干冰易升华但却不易分解的主要原因是____ 。
(2)羟胺(NH2OH)是共价化合物,各原子均满足稀有气体稳定结构。羟胺的电子式是____ 。
(3)苯酚和乙醇分子中都含有羟基,但在与氢氧化钠反应时,羟基的性质表现出较大的差异。原因是____ 。
(2)羟胺(NH2OH)是共价化合物,各原子均满足稀有气体稳定结构。羟胺的电子式是
(3)苯酚和乙醇分子中都含有羟基,但在与氢氧化钠反应时,羟基的性质表现出较大的差异。原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】下表是元素周期表的一部分,回答下列有关问题:

(1)写出下列元素符号:①_________ ,⑥_________ ,⑦_______ 。
(2)画出原子的结构示意图:④__________ ,⑧____________ 。
(3)在①~12元素中,金属性最强的元素是______ ,非金属性最强的元素是____ ,最不活泼的元素是_____ 。(均填元素符号)
(4)元素⑦与元素⑧相比,非金属性较强的是______ (用元素符号表示),下列表述中能证明这一事实的是________ 。
a.常温下⑦的单质和⑧的单质状态不同
b.⑧的氢化物比⑦的氢化物稳定
c.一定条件下⑦和⑧的单质都能与氢氧化钠溶液反应
(5)第三周期中原子半径最大的元素是___ (填序号),跟它同周期原子半径最小的元素是__ (填序号),它们可以形成____ (填离子或共价)化合物,用电子式表示其形成过程:____ 。(6)已知某元素原子最外层电子数是其次外层电子数的2倍,该元素可以与⑧形成一种AB4型的化合物,请用电子式表示其形成过程:_____

(1)写出下列元素符号:①
(2)画出原子的结构示意图:④
(3)在①~12元素中,金属性最强的元素是
(4)元素⑦与元素⑧相比,非金属性较强的是
a.常温下⑦的单质和⑧的单质状态不同
b.⑧的氢化物比⑦的氢化物稳定
c.一定条件下⑦和⑧的单质都能与氢氧化钠溶液反应
(5)第三周期中原子半径最大的元素是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】在HF、H2S、PH3、CS2、CCl4、H2O2、N2分子中:(将所选的物质化学式填入空白)
(1)以非极性键结合的非极性分子是_______
(2)以极性键相结合,具有直线型结构的非极性分子是_______
(3)以极性键相结合,具有正四面体结构的非极性分子是_______
(4)以极性键相结合,具有三角锥型结构的极性分子是______
(5)以极性键相结合,具有V型结构的极性分子是_______
(6)以极性键相结合,而且分子极性最大的是_______
(7)与N2O互为等电子体的是_________
(8)含有非极性键的极性分子是________ 。
(1)以非极性键结合的非极性分子是
(2)以极性键相结合,具有直线型结构的非极性分子是
(3)以极性键相结合,具有正四面体结构的非极性分子是
(4)以极性键相结合,具有三角锥型结构的极性分子是
(5)以极性键相结合,具有V型结构的极性分子是
(6)以极性键相结合,而且分子极性最大的是
(7)与N2O互为等电子体的是
(8)含有非极性键的极性分子是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】研究小组利用如图所示装置制备CO2气体,其中K为止水夹,多孔塑料板固定在试管的某一位置。请问答以下问题:
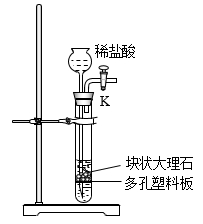
(1)当止水夹K打开时,大理石即可与稀盐酸反应产生CO2气体;当止水夹关闭后,该反应可随后停止。起到这种随关随停作用的主要原因是__________
(2)实验室可以利用上述装置制备某些气体,能达到随开随用,随关随停的有__________
A.锌粒和稀硫酸制氢气B.浓盐酸和二氧化锰制取氯气
C.Na2SO3固体和硫酸反应制备SO2D.利用FeS块状固体与稀硫酸反应制备H2S气体
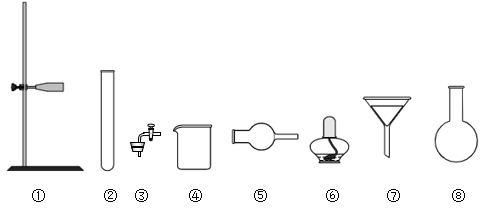
(3)请你选用如图所示的部分仪器,装配成一个简易的、能随开随用、随关随停的CO2气体发生装置。应选用的仪器是__________ (填仪器的编号)

(1)当止水夹K打开时,大理石即可与稀盐酸反应产生CO2气体;当止水夹关闭后,该反应可随后停止。起到这种随关随停作用的主要原因是
(2)实验室可以利用上述装置制备某些气体,能达到随开随用,随关随停的有
A.锌粒和稀硫酸制氢气B.浓盐酸和二氧化锰制取氯气
C.Na2SO3固体和硫酸反应制备SO2D.利用FeS块状固体与稀硫酸反应制备H2S气体

(3)请你选用如图所示的部分仪器,装配成一个简易的、能随开随用、随关随停的CO2气体发生装置。应选用的仪器是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】观察下列实验装置图,试回答下列问题:

⑴写出图中实验操作对应的名称 ①:_______________ 、 ③:______________ 。
⑵下列实验需要在哪套装置中进行(填序号): a、分离植物油和水:____________ ; b、从海水中提取蒸馏水: __________ ;
⑶装置①中玻璃棒的作用是__________________________________ ;
⑷ 实验室需要490mL 0.5mol•L-1 NaOH溶液,请回答下列问题:
①需称取___________ g的烧碱固体.
②配制的玻璃仪器除烧杯和玻璃棒、胶头滴管,还需要___________________________ 。
③下列各项中,可能导致实际浓度偏高的是_________ (填标号).
A.定容时,仰视容量瓶的刻度线
B.NaOH溶解时放出大量的热,未冷却立即配制溶液
C.溶解NaOH固体之后的烧杯未洗涤
D.向容量瓶中转移溶液时不慎洒出

⑴写出图中实验操作对应的名称 ①:
⑵下列实验需要在哪套装置中进行(填序号): a、分离植物油和水:
⑶装置①中玻璃棒的作用是
⑷ 实验室需要490mL 0.5mol•L-1 NaOH溶液,请回答下列问题:
①需称取
②配制的玻璃仪器除烧杯和玻璃棒、胶头滴管,还需要
③下列各项中,可能导致实际浓度偏高的是
A.定容时,仰视容量瓶的刻度线
B.NaOH溶解时放出大量的热,未冷却立即配制溶液
C.溶解NaOH固体之后的烧杯未洗涤
D.向容量瓶中转移溶液时不慎洒出
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】某84”消毒液部分标签如下图所示,回答下列问题:
(1) 中
中 的化合价为
的化合价为___________ , 具有较强的
具有较强的___________ (填“氧化”或“还原)性,是常用的消毒剂和漂白剂的有效成分。
(2)计算该“84”消毒液的物质的量浓度___________  (保留小数点后一位)。
(保留小数点后一位)。
(3)某实验需用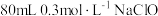 的溶液
的溶液
①若用上述“84消毒液配制,需要量取___________  。
。
②在配制过程中,除需要烧杯、量筒、玻璃棒外还必需的仪器有___________ 、___________ (写仪器名称)。
③下列操作可能使配制溶液浓度偏高的是(填字母)___________ 。
A.转移溶液时,未洗涤烧杯内壁和玻璃棒
B.溶解后未经冷却就移液
C.将量筒残留液洗入烧杯中
D.定容时,俯视刻度线
E.容量瓶用蒸馏水洗净后,没烘干就直接使用
净含量: 密度: 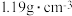 主要成分: 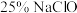 注意事项:密封保存 |
 中
中 的化合价为
的化合价为 具有较强的
具有较强的(2)计算该“84”消毒液的物质的量浓度
 (保留小数点后一位)。
(保留小数点后一位)。(3)某实验需用
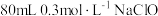 的溶液
的溶液①若用上述“84消毒液配制,需要量取
 。
。②在配制过程中,除需要烧杯、量筒、玻璃棒外还必需的仪器有
③下列操作可能使配制溶液浓度偏高的是(填字母)
A.转移溶液时,未洗涤烧杯内壁和玻璃棒
B.溶解后未经冷却就移液
C.将量筒残留液洗入烧杯中
D.定容时,俯视刻度线
E.容量瓶用蒸馏水洗净后,没烘干就直接使用
您最近一年使用:0次



