工业生产的纯碱常含有少量的氯化钠杂质。如图是测定产品中碳酸钠质量分数的实验装置,下列说法不正确的是( )
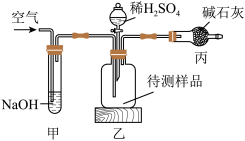

| A.装置乙中发生的反应方程式为H2SO4+Na2CO3=Na2SO4+CO2↑+H2O |
| B.装置甲的作用是除去空气中的二氧化碳气体 |
| C.反应结束后再需缓缓鼓入空气数分钟 |
| D.若实验操作无误,该装置测得的碳酸钠的质量分数结果偏小 |
19-20高一上·浙江台州·阶段练习 查看更多[2]
更新时间:2020-04-15 10:12:49
|
【知识点】 探究物质组成或测量物质的含量解读
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】某白色粉末由两种物质组成,取少量样品加入适量水中有少量气泡并有少量不溶物,再向其中加入足量盐酸,固体不溶解;将上述悬浊液过滤,滤渣中加入浓硝酸并加热,固体全部溶解。则可推得该白色粉末可能为
| A.Na2S2O3、NaHSO4 | B.NaHCO3、KAl(SO4)2·12H2O |
| C.Na2SiO3、NH4Cl | D.(NH4)2SO4、Ba(OH)2 |
您最近半年使用:0次
单选题
|
较易
(0.85)
【推荐2】测定胆矾晶体中结晶水含量的实验中,必须做恒重操作的原因是
| A.判断加热时有无晶体飞溅 |
| B.判断是否已失去全部结晶水 |
| C.判断是否有其他杂质 |
| D.防止失水后又吸潮 |
您最近半年使用:0次



