(1)分别取wg钠、铁、铝与足量的稀盐酸反应,在相同条件下产生氢气的体积之比是__________ 。
(2)分别取0.1 mol钠、铁、铝与足量的稀盐酸反应,在相同条件下产生氢气的体积之比是___________ 。
(3)若产生相同物质的量的氢气,所需钠、铁、铝的质量之比是_________ 。
(4)若产生相同体积(同温同压下)的氢气,所需钠、铁、铝的物质的量之比是__________ 。
(2)分别取0.1 mol钠、铁、铝与足量的稀盐酸反应,在相同条件下产生氢气的体积之比是
(3)若产生相同物质的量的氢气,所需钠、铁、铝的质量之比是
(4)若产生相同体积(同温同压下)的氢气,所需钠、铁、铝的物质的量之比是
20-21高一上·全国·期中 查看更多[1]
(已下线)【南昌新东方】2019 湾里一中 高一上期中
更新时间:2020-04-18 21:10:17
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】按要求完成下列填空。
(1)49gH2SO4中氧原子数为___________ 。
(2)标准状况下,氮气的密度为___________ 。
(3)同温同压下,0.4gH2与1.6gCH4的体积之比为______ ;二者混合后,所含H原子总数为_______ 。
(4)某金属氯化物MCl240.5g,含有0.6molCl-,则金属M的相对原子质量为_______ 。
(5)有下列物质:①熔融氯化钠②铜③氯化氢气体④稀硫酸⑤二氧化碳⑥碳酸氢钠粉末⑦蔗糖晶体⑧硫酸钡固体,请用序号填空:
i.属于电解质的是___________ (填序号,下同)。
ii.属于非电解质的是___________ 。
iii.写出碳酸氢钠的电离方程式___________ 。
(1)49gH2SO4中氧原子数为
(2)标准状况下,氮气的密度为
(3)同温同压下,0.4gH2与1.6gCH4的体积之比为
(4)某金属氯化物MCl240.5g,含有0.6molCl-,则金属M的相对原子质量为
(5)有下列物质:①熔融氯化钠②铜③氯化氢气体④稀硫酸⑤二氧化碳⑥碳酸氢钠粉末⑦蔗糖晶体⑧硫酸钡固体,请用序号填空:
i.属于电解质的是
ii.属于非电解质的是
iii.写出碳酸氢钠的电离方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)0.3 mol CH4 含有的电子数目为____ ;它与____ 克 CO2 的原子总数相同;O2 与 SO2 等质量混合,该混合物中 O2 与 SO2 的物质的量之比为______ 。
(2)某常见气体在标准状况下的密度为 1.25 g/L,若该气体的分子式为 A2 型, 则其名称是______ 。
(3)取 100 mL 1mol/L NaCl 溶液与 300 mL0.5mol/L MgCl2 溶液配成混合溶液,则该混合溶液中 Cl-的物质的量浓度为______ 。
(2)某常见气体在标准状况下的密度为 1.25 g/L,若该气体的分子式为 A2 型, 则其名称是
(3)取 100 mL 1mol/L NaCl 溶液与 300 mL0.5mol/L MgCl2 溶液配成混合溶液,则该混合溶液中 Cl-的物质的量浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】电解饱和食盐水可产生氯气、氢气和氢氧化钠,氯气与石灰乳反应可制得漂白粉。
(1)请写出上述过程中发生反应的化学方程式________ 。
(2)若电解饱和食盐水时消耗NaCl 117g, 试计算理论上最多可得到氯气的体积(标准状况)________ 。
(3)若将2 mol氯气通入足量石灰乳中,理论上可得到次氯酸钙多少克________ ?
(1)请写出上述过程中发生反应的化学方程式
(2)若电解饱和食盐水时消耗NaCl 117g, 试计算理论上最多可得到氯气的体积(标准状况)
(3)若将2 mol氯气通入足量石灰乳中,理论上可得到次氯酸钙多少克
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题:
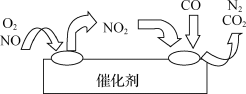
(1)汽车排出的尾气中含有氮氧化物,为避免污染,常给汽车安装尾气净化装置。净化装置里装有催化剂,气体在催化剂表面吸附与解吸作用的机理如下图所示。写出净化过程中的总化学方程式:_______ 。
(2)国家规定氮氧化物的排放标准不超过400mg/L。氮氧化物可以用酸性硫酸亚铁溶液来吸收,反应原理为NO+Fe2+=[Fe(NO)]2+;NO2+3Fe2++2H+=2Fe3++[Fe(NO)]2++H2O。现测定某地下水脱硝过程中氮氧化物的排放量:收集500.00mL排放的气体,缓慢通过250.00mL0.6240mol/L酸性FeSO4溶液(过量),充分反应,量取吸收气体后的溶液25.00mL置于锥形瓶中,用0.2000mol/L酸性KMnO4溶液与之反应,重复上述实验操作3次,平均消耗酸性KMnO4溶液的体积为15.00mL。试通过计算分析地下水脱硝过程中氮氧化物的排放是否符合国家标准_______ (写出计算过程)。已知:①[Fe(NO)]2+与酸性KMnO4溶液不反应;②H++MnO +Fe2+=Mn2++Fe3++H2O(未配平)
+Fe2+=Mn2++Fe3++H2O(未配平)
(1)汽车排出的尾气中含有氮氧化物,为避免污染,常给汽车安装尾气净化装置。净化装置里装有催化剂,气体在催化剂表面吸附与解吸作用的机理如下图所示。写出净化过程中的总化学方程式:

(2)国家规定氮氧化物的排放标准不超过400mg/L。氮氧化物可以用酸性硫酸亚铁溶液来吸收,反应原理为NO+Fe2+=[Fe(NO)]2+;NO2+3Fe2++2H+=2Fe3++[Fe(NO)]2++H2O。现测定某地下水脱硝过程中氮氧化物的排放量:收集500.00mL排放的气体,缓慢通过250.00mL0.6240mol/L酸性FeSO4溶液(过量),充分反应,量取吸收气体后的溶液25.00mL置于锥形瓶中,用0.2000mol/L酸性KMnO4溶液与之反应,重复上述实验操作3次,平均消耗酸性KMnO4溶液的体积为15.00mL。试通过计算分析地下水脱硝过程中氮氧化物的排放是否符合国家标准
 +Fe2+=Mn2++Fe3++H2O(未配平)
+Fe2+=Mn2++Fe3++H2O(未配平)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】储氢纳米碳管的研究成功体现了科技的进步,但用电弧法合成的碳纳米管常伴有大量的杂质——碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯其反应式为C+K2Cr2O7+H2SO4=CO2+K2SO4+Cr2(SO4)3+H2O(未配平)
(1)配平上述方程式__ C+__ K2Cr2O7+__ H2SO4=__ CO2+ __ K2SO4+__ Cr2(SO4)3+__ H2O
(2)上述反应中氧化剂是_______ (填化学式),氧化产物是__________ (填化学式)
(3)H2SO4在上述发应中表现出来的性质是_______ (填序号)
a.氧化性 b.氧化性和酸性 c.酸性 d.还原性和酸性
(4)若反应中电子转移了0.8mol,则产生的气体在标准状况下的体积为__________ L
(5)要使10mL0.5mol/L的K2Cr2O7,溶液被还原,至少要加入________ mL2mol/L的H2SO4溶液
(1)配平上述方程式
(2)上述反应中氧化剂是
(3)H2SO4在上述发应中表现出来的性质是
a.氧化性 b.氧化性和酸性 c.酸性 d.还原性和酸性
(4)若反应中电子转移了0.8mol,则产生的气体在标准状况下的体积为
(5)要使10mL0.5mol/L的K2Cr2O7,溶液被还原,至少要加入
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】按要求回答下列问题:
(1)胆矾的化学式___ 。
(2)NaHCO3溶于水的电离方程式:___ 。
(3)铁与水蒸气反应的化学方程式:___ 。
(4)H3PO2属于一元酸,写出它与足量氢氧化钠溶液反应的化学方程式:___ 。
(5)从原子结构角度解释金属性钾比钠强的原因:___ 。
(1)胆矾的化学式
(2)NaHCO3溶于水的电离方程式:
(3)铁与水蒸气反应的化学方程式:
(4)H3PO2属于一元酸,写出它与足量氢氧化钠溶液反应的化学方程式:
(5)从原子结构角度解释金属性钾比钠强的原因:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】依据信息书写下列反应的方程式
⑴K2O2可用于潜水设备中作供氧剂,写出K2O2与CO2反应的化学方程式:________ 。
⑵SO2是一种酸性氧化物,可制取Na2SO3,从括号内所给试剂(NaCl溶液、NaOH溶液、Na2SO4溶液)中选择合适的,完成这一反应,写出该反应的化学方程式:________ 。
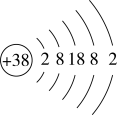
⑶锶(Sr)原子的结构示意图如图所示,锶能与水发生剧烈反应生成碱和氢气,写出单质锶与水反应的化学方程式:________ 。
⑷MnO2可经过下图所示的转化制取MnCO3。已知“反应Ⅱ”为复分解反应。
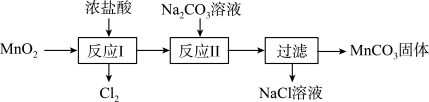
①写出“反应Ⅰ”的化学方程式:________ 。
②写出“反应Ⅱ”的离子方程式:________ 。
⑴K2O2可用于潜水设备中作供氧剂,写出K2O2与CO2反应的化学方程式:
⑵SO2是一种酸性氧化物,可制取Na2SO3,从括号内所给试剂(NaCl溶液、NaOH溶液、Na2SO4溶液)中选择合适的,完成这一反应,写出该反应的化学方程式:
⑶锶(Sr)原子的结构示意图如图所示,锶能与水发生剧烈反应生成碱和氢气,写出单质锶与水反应的化学方程式:

⑷MnO2可经过下图所示的转化制取MnCO3。已知“反应Ⅱ”为复分解反应。

①写出“反应Ⅰ”的化学方程式:
②写出“反应Ⅱ”的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】元素铬(Cr)在溶液中主要以Cr3+(蓝紫色)、Cr(OH)4(绿色)、Cr2O72-(橙红色)、CrO42-(黄色)等形式存在。Cr(OH)3为难溶于水的灰蓝色固体,回答下列问题:
(1)Cr2O72-中元素铬(Cr)的化合价为_____ 。
(2)Cr3+与Al3+的化学性质相似。在Cr2(SO4)3溶液中逐滴加入 溶液直至过量,可观察到的现象是
溶液直至过量,可观察到的现象是____ 。
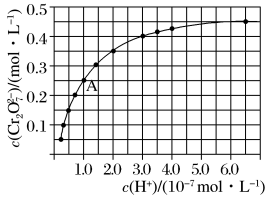
(3)CrO42-和Cr2O72-在溶液中可相互转化:2CrO42-+2H+⇌Cr2O72-+H2O,室温下,初始浓度为1.0mol•L-1的Na2CrO4溶液中,c(Cr2O72-)随c(H+)的变化如图所示。
①溶液酸性增大,CrO42-的平衡转化率_________ 。(填“增大”“减小”或“不变”)。
②根据A点数据,计算出该转化反应的平衡常数为___________ 。
③温度升高,溶液中CrO42-的平衡转化率减小,则该反应的ΔH____ 0(填“>、=、<”)。

(1)Cr2O72-中元素铬(Cr)的化合价为
(2)Cr3+与Al3+的化学性质相似。在Cr2(SO4)3溶液中逐滴加入
 溶液直至过量,可观察到的现象是
溶液直至过量,可观察到的现象是(3)CrO42-和Cr2O72-在溶液中可相互转化:2CrO42-+2H+⇌Cr2O72-+H2O,室温下,初始浓度为1.0mol•L-1的Na2CrO4溶液中,c(Cr2O72-)随c(H+)的变化如图所示。
①溶液酸性增大,CrO42-的平衡转化率
②根据A点数据,计算出该转化反应的平衡常数为
③温度升高,溶液中CrO42-的平衡转化率减小,则该反应的ΔH
您最近一年使用:0次



