分析如图所示的四个原电池装置,其中结论正确的是( )
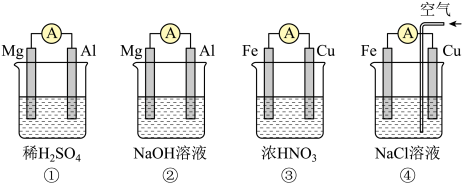

| A.①②中Mg作负极,③④中Fe作负极 |
| B.②中Mg作正极,电极反应式为6H2O+6e-=6OH-+3H2↑ |
| C.③中Fe作负极,电极反应式为Fe-3e-=Fe3+ |
| D.④中Cu作正极,电极反应式为2H++2e-=H2↑ |
2019高三·浙江·专题练习 查看更多[8]
河南省郑州市河南省实验中学2019-2020学年高一下学期月考化学试卷广东省汕头市金山中学2019-2020学年高一下学期6月月考化学试题(已下线)考点09 电化学原理-2020年【衔接教材·暑假作业】新高三一轮复习化学山东省滕州市第一中学2019-2020学年高一5月摸底考试化学试题吉林省延边市长白山第一高级中学2019-2020学年高一下学期验收考试化学试题福建省宁德市福鼎六中2019-2020学年高二上学期第一次月考化学试题河北省黄骅中学2018-2019学年高一下学期第二次月考化学试题(已下线)考点09 原电池原理及其应用——备战2019年浙江新高考化学考点
更新时间:2020-04-28 08:51:35
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】水系钠离子电池安全性能好、价格低廉、对环境友好,有巨大的市场前景。某钠离子二次电池总反应为2NaFePO4F+Na3Ti2(PO4)3 2Na2FePO4F+NaTi2(PO4)3。下列说法正确的是
2Na2FePO4F+NaTi2(PO4)3。下列说法正确的是
 2Na2FePO4F+NaTi2(PO4)3。下列说法正确的是
2Na2FePO4F+NaTi2(PO4)3。下列说法正确的是| A.放电时,溶液中的Na+向负极移动 |
| B.充电时,溶液中的Na+在阴极上得电子被还原 |
| C.充电时,阳极电极反应式为Na2FePO4F-e- = NaFePO4F+Na+ |
| D.放电时,电路中通过1mol e-时,正极增重46g |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】利用微生物燃料电池(MFC)处理废水,可实现碳氮联合转化。某微生物燃料电池的工作原理如图所示。下列说法不正确的是
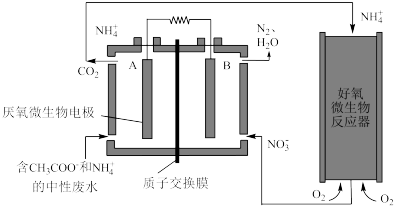

A.电子移动方向是从A电极流向B电极,溶液中 的移动方向从左到右 的移动方向从左到右 |
B.B电极反应式为: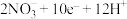  |
C.相同条件下,A极区生成的 与B极区生成的 与B极区生成的 的体积之比为5∶4 的体积之比为5∶4 |
| D.该电池在高温情况下无法正常工作 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】为探究原电池的形成条件和反应原理,某同学设计了如下实验并记录了现象:
① 向一定浓度的稀硫酸中插入锌片,看到有气泡生成;
② 向上述稀硫酸中插入铜片,没有看到有气泡生成;
③ 将锌片与铜片上端用导线连接,一起插入稀硫酸中,看到铜片上有气泡生成,且生成气泡的速率比实验①中快
④ 在锌片和铜片中间接上电流计,再将锌片和铜片插入稀硫酸中,发现电流计指针偏转。
下列关于以上实验设计及现象的分析,不正确 的是
① 向一定浓度的稀硫酸中插入锌片,看到有气泡生成;
② 向上述稀硫酸中插入铜片,没有看到有气泡生成;
③ 将锌片与铜片上端用导线连接,一起插入稀硫酸中,看到铜片上有气泡生成,且生成气泡的速率比实验①中快
④ 在锌片和铜片中间接上电流计,再将锌片和铜片插入稀硫酸中,发现电流计指针偏转。
下列关于以上实验设计及现象的分析,
| A.实验①、②说明锌能与稀硫酸反应产生氢气,而铜不能 |
| B.实验③说明发生原电池反应时会加快化学反应速率 |
| C.实验③说明在该条件下铜可以与稀硫酸反应生成氢气 |
| D.实验④说明该装置可形成原电池 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】 是一种剧毒气体,对H2S废气资源化利用途径之一是回收能量并得到单质硫,反应原理为:
是一种剧毒气体,对H2S废气资源化利用途径之一是回收能量并得到单质硫,反应原理为: 。如图为质子膜
。如图为质子膜 燃料电池的示意图。下列说法正确的是
燃料电池的示意图。下列说法正确的是

 是一种剧毒气体,对H2S废气资源化利用途径之一是回收能量并得到单质硫,反应原理为:
是一种剧毒气体,对H2S废气资源化利用途径之一是回收能量并得到单质硫,反应原理为: 。如图为质子膜
。如图为质子膜 燃料电池的示意图。下列说法正确的是
燃料电池的示意图。下列说法正确的是
| A.电池工作时,电流从电极a经负载流向电极b |
B.电极a上发生的电极反应为: |
| C.当反应生成64gS2时,电池内部释放632kJ热能 |
| D.当电路中通过4mol电子时,有4mol H+经质子膜进入正极区 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】利用微生物电池可处理有机废水和废气NO,下列说法正确的是


| A.外电路中电流的方向为:M极→导线→N极 |
| B.H+透过阳离子交换膜由右向左移动 |
| C.有机废水在微生物作用下发生了还原反应 |
| D.正极的电极反应式为:2NO+4H++4e-=N2+2H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】一种新型酸性乙醇电池用磺酸类质子作溶剂,比甲醇电池效率高出32倍,电池反应式为:C2H5OH+3O2===2CO2+3H2O,电池构造如下图所示。下列关于该电池的说法正确的是
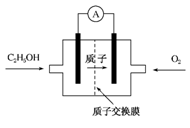

| A.放电过程中,电源内部的H+从正极区向负极区迁移 |
| B.通入乙醇的电极是正极 |
| C.该电池的正极反应为:4H++O2+4e-===2H2O |
| D.用该电池做电源,用惰性电极电解饱和NaCl溶液时,每消耗0.2 mol C2H5OH,阴极产生标准状况下气体的体积为13.44 L |
您最近一年使用:0次



