除去食盐溶液中的Ca2+、Mg2+、SO42-等杂质,需加入NaOH、Na2CO3、BaCl2和盐酸,加入顺序正确的是
| A.NaOH Na2CO3 BaCl2 HCl | B.Na2CO3 BaCl2 HCl NaOH |
| C.BaCl2 HCl NaOH Na2CO3 | D.NaOH BaCl2 Na2CO3 HCl |
更新时间:2020-05-05 09:27:54
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】除去粗盐中的杂质CaCl2、MgCl2和Na2SO4,过程如下:下列有关说法中,不正确的是


| A.除去Mg2+的主要反应:MgCl2+2NaOH=Mg(OH)2↓+2NaCl |
| B.试剂①可以是Na2CO3溶液 |
C.检验 是否除净:取少量滤液,加稀盐酸酸化,再加BaCl2溶液 是否除净:取少量滤液,加稀盐酸酸化,再加BaCl2溶液 |
| D.滤液加稀盐酸时发生反应:HCl+NaOH=H2O+NaCl和2HCl+Na2CO3=2NaCl+CO2↑+H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】食盐是日常生活的必需品,也是重要的化工原料。为除去粗盐中的 、
、 、
、 以及泥沙等杂质,实验方案如下,下列说法错误的是
以及泥沙等杂质,实验方案如下,下列说法错误的是

 、
、 、
、 以及泥沙等杂质,实验方案如下,下列说法错误的是
以及泥沙等杂质,实验方案如下,下列说法错误的是
A.试剂 为 为 溶液,其目的是除溶液中的 溶液,其目的是除溶液中的 |
| B.若先加盐酸再过滤,将对实验结果产生影响 |
| C.粗盐提纯的整个操作过程中共有两处需要使用玻璃棒 |
D.加入试剂 的主要目的是除去 的主要目的是除去 和 和 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】粗盐中含有较多的杂质,有不溶性的泥沙,还有可溶性的 CaCl2、MgCl2、Na2SO4 等杂质, 通过如下几个实验步骤,可制得纯净的食盐水,其中错误的是
| A.可以先加入稍过量的 BaCl2 溶液,以便除去 Na2SO4 |
| B.Na2CO3 溶液必须在BaCl2 溶液之后加入,且稍过量一些 |
| C.加入的NaOH 溶液的顺序没有要求,只要稍过量就可以了 |
| D.在上述步骤完成后,不需要任何操作,直接加入稀盐酸至无气泡产生,即可达到目的 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】锡酸钠(Na2SnO3)是重要的化工产品,主要用于电镀行业,以及锡合金、锌锡合金、铝合金等。用铅锡锑冶炼浮渣(主要是铅、锡、锑的氧化物及相应的盐构成)制备Na2SnO3产品的工艺流程如下图所示:
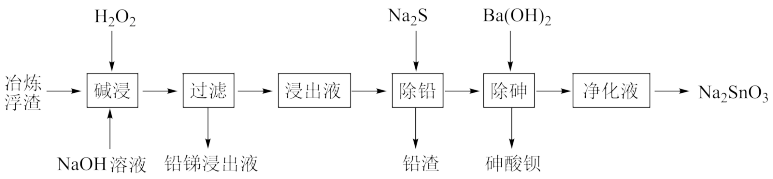
已知:①“浸出液”中含有有大量Na2PbO2、Na3AsO4等,“净化液”中含有少量Na2PbO2、Na3AsO4等;
②Na2SnO3的溶解度随温度升高而减小,Na2PbO2、Na3AsO4的溶解度随温度升高而增大。
下列叙述正确的是

已知:①“浸出液”中含有有大量Na2PbO2、Na3AsO4等,“净化液”中含有少量Na2PbO2、Na3AsO4等;
②Na2SnO3的溶解度随温度升高而减小,Na2PbO2、Na3AsO4的溶解度随温度升高而增大。
下列叙述正确的是
| A.露天堆存铅锡锑冶炼浮渣对环境无任何影响 |
| B.“碱浸”时,H2O2可用浓硝酸代替 |
| C.“除铅”时的离子方程式为Pb2++S2-=PbS↓ |
| D.分离出Na2SnO3的操作为浓缩结晶、趁热过滤、洗涤、干燥 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】以菱镁矿(主要成分为MgCO3,含少量FeCO3等物质)为原料制备MgCl2•6H2O的实验流程如图所示。下列说法正确的是
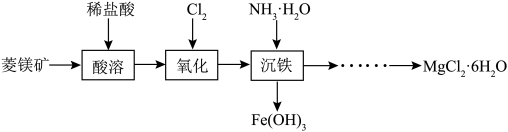

A.MgCO3与稀盐酸反应的离子方程式为CO +2H+=CO2↑+H2O +2H+=CO2↑+H2O |
| B.氧化过程说明氧化性:Cl2>Fe3+ |
C.“沉铁”后的溶液中大量存在Mg2+、NH 、OH-、Cl- 、OH-、Cl- |
| D.“沉铁”的方程式为:Fe3++3OH-=Fe(OH)3↓ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
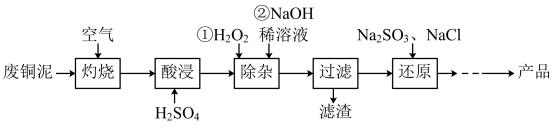
【推荐2】由工业废铜泥(主要成分为 、
、 、
、 ,含少量Fe)制备难溶于水的氯化亚铜,其工艺流程如图。下列说法错误的是
,含少量Fe)制备难溶于水的氯化亚铜,其工艺流程如图。下列说法错误的是
 、
、 、
、 ,含少量Fe)制备难溶于水的氯化亚铜,其工艺流程如图。下列说法错误的是
,含少量Fe)制备难溶于水的氯化亚铜,其工艺流程如图。下列说法错误的是
A.灼烧时可将CuS、 等转化为CuO 等转化为CuO |
| B.除杂②过程中还需加热 |
C.流程中可循环使用的物质有 、 、 |
D.还原中的反应为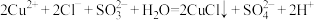 |
您最近一年使用:0次



