前一段时间,各地报刊纷纷转载了不要将不同品牌洁污剂混合使用的警告。据报道,在全国各地发生了多起混合洁污剂发生氯气中毒的事件。发生反应的离子方程式是:ClO+Cl+2H+=Cl2↑+H2O。根据你所掌握的化学知识作出如下判断:当事人使用的液态洁污剂之一必定含氯,其中氯最可能的存在形式是_________ 和_______ (填离子),当另一种具有_______ (性质)的液态洁污剂与之混合,可能发生上述反应而产生氯气。举例说明这两种洁污剂的名称(家用洁污剂的商品名称)___________ 、____________ 。
更新时间:2020-05-05 16:14:50
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】按要求回答下列问题
(1)国家质检部门检出人们端午节包粽子的“返青粽叶”多以胆矾为添加剂,长期食用有害健康。请写出胆矾的化学式___________ 。
(2)次磷酸(H3PO2)是磷的一种含氧酸,与足量NaOH溶液反应生成NaH2PO2,在工业上可做还原剂。
①NaH2PO2属于___________ (选填“正盐”或“酸式盐”)
②请从化合价的角度解释H3PO2可做还原剂的原因___________ 。
(3)钠与水反应的离子方程式是___________ 。
(4)用化学方程式解释新制氯水光照一段时间后,pH减小的原因___________ 。
(5)向FeSO4溶液中滴加NaOH溶液,观察到的现象是___________ 。
(6)打印机使用的墨粉中含有Fe3O4.它的一种制备方法是:将FeSO4溶液、Fe2(SO4)3溶液按一定比例混合,再加入一定量的NaOH溶液,水浴加热。反应如下:
___Fe2++_____Fe3++___OH—=__Fe3O4+____H2O
请配平上述反应___________ 。
(1)国家质检部门检出人们端午节包粽子的“返青粽叶”多以胆矾为添加剂,长期食用有害健康。请写出胆矾的化学式
(2)次磷酸(H3PO2)是磷的一种含氧酸,与足量NaOH溶液反应生成NaH2PO2,在工业上可做还原剂。
①NaH2PO2属于
②请从化合价的角度解释H3PO2可做还原剂的原因
(3)钠与水反应的离子方程式是
(4)用化学方程式解释新制氯水光照一段时间后,pH减小的原因
(5)向FeSO4溶液中滴加NaOH溶液,观察到的现象是
(6)打印机使用的墨粉中含有Fe3O4.它的一种制备方法是:将FeSO4溶液、Fe2(SO4)3溶液按一定比例混合,再加入一定量的NaOH溶液,水浴加热。反应如下:
___Fe2++_____Fe3++___OH—=__Fe3O4+____H2O
请配平上述反应
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】氯水中含有多种成分,因而具有多种性质,根据新制氯水分别与如图四种物质发生的反应填空(a、b、c、d中重合部分代表物质间反应,且氯水足量)。

(1)能证明氯水具有漂白性的是_______ (填“a”、“b”、“c”或“d”);
(2)c过程中的现象是_______ ;d过程中的现象是_______ ;e过程中的现象是_______ ;b过程中的离子方程式为_______ ;e过程的化学方程式_______ ;
(3)久置的氯水变为_______ ,用化学反应方程式表示为_______ ;
(4)实验室保存饱和氯水的方法是_______ 。

(1)能证明氯水具有漂白性的是
(2)c过程中的现象是
(3)久置的氯水变为
(4)实验室保存饱和氯水的方法是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】氯和氯的化合物在生产、生活中都有广泛的应用。
(1)工业上盛放浓盐酸的容器上往往贴有多个安全标识,下列标识中不宜 贴上的是_______
(2)如图是我们课本上“铁丝在氯气中燃烧”的实验。

该反应生成的棕褐色烟的主要成分是_______ 。如果把“反应后加入水”改为“反应后加入NaOH溶液”,则NaOH可能参与两个反应,相应的化学方程式分别为:_______ 、_______ 。
(3)新制的氯水中存在多种微粒。
①向氯水不滴加硝酸银溶液,有白色沉淀生成,证明氯水中含_______ 离子。
②用pH计测出,氯水的pH=1.03,说明了氯水中含_______ 离子。
③把新制的氯水滴在有色纸片上,色纸被漂白了。设计实验证明起漂白作用的是氯水中HClO而不是Cl2_______ 。
(4)把氯气溶于水得到新制氯水,把该氯水加入滴有酚酞的NaOH溶液中,发现溶液红色褪去。为探究褪色的原因,有同学提出三种猜想:
猜想1:氯水消耗了NaOH;
猜想2:氯水消耗了酚酞;
猜想3:氯水同时消耗了NaOH和酚酞。
为验证上述猜想,该同学取上述褪色后的溶液于甲、乙两支试管中。向甲试管中滴加足量NaOH溶液,向乙试管中滴加足量酚酞溶液。如果甲试管中溶液变红,则_______ 成立;如果观察到_______ (填实验现象),则猜想3成立。
(5)工业上通常把氯气通入潮湿的石灰中制漂白粉,日常生活中在使用漂白粉时,为了促进其漂白效果,可采取的方法_______ (任举一例)。漂白粉久置于空气中会变质,写出变质的化学方程式_______ 、_______ 。
(1)工业上盛放浓盐酸的容器上往往贴有多个安全标识,下列标识中
A. | B. | C. | D. |

该反应生成的棕褐色烟的主要成分是
(3)新制的氯水中存在多种微粒。
①向氯水不滴加硝酸银溶液,有白色沉淀生成,证明氯水中含
②用pH计测出,氯水的pH=1.03,说明了氯水中含
③把新制的氯水滴在有色纸片上,色纸被漂白了。设计实验证明起漂白作用的是氯水中HClO而不是Cl2
(4)把氯气溶于水得到新制氯水,把该氯水加入滴有酚酞的NaOH溶液中,发现溶液红色褪去。为探究褪色的原因,有同学提出三种猜想:
猜想1:氯水消耗了NaOH;
猜想2:氯水消耗了酚酞;
猜想3:氯水同时消耗了NaOH和酚酞。
为验证上述猜想,该同学取上述褪色后的溶液于甲、乙两支试管中。向甲试管中滴加足量NaOH溶液,向乙试管中滴加足量酚酞溶液。如果甲试管中溶液变红,则
(5)工业上通常把氯气通入潮湿的石灰中制漂白粉,日常生活中在使用漂白粉时,为了促进其漂白效果,可采取的方法
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】利用氯元素价类二维图可以从不同角度研究含氯物质的性质及其转化关系。图中①⑩均含氯元素。回答下列问题:

(1)④的化学式为_______ ,⑦的酸性比碳酸_______ (填“强”或“弱”)。
(2)比较等浓度的⑥和⑦溶液的酸性强弱_______ (填“可以”或“不可以”)用 试纸分别测定。
试纸分别测定。
(3)工业制漂白粉是将①通入_______ 中(填名称)制成的,漂白粉放置时间长了就会失效,写出漂白粉失效的化学方程式_______ ,_______ 。
(4)某一淡黄色粉末与⑥相似,也具有漂白性,这种粉末能与⑤反应生成⑧,请写出该反应的化学方程式_______ 。

(1)④的化学式为
(2)比较等浓度的⑥和⑦溶液的酸性强弱
 试纸分别测定。
试纸分别测定。(3)工业制漂白粉是将①通入
(4)某一淡黄色粉末与⑥相似,也具有漂白性,这种粉末能与⑤反应生成⑧,请写出该反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】工业上用 和碱制漂白粉、漂粉精及漂白液。请回答下列问题:
和碱制漂白粉、漂粉精及漂白液。请回答下列问题:
(1) Ca(ClO)2中Cl元素的化合价是___________ ;工业上将氯气制成漂白粉的主要目的是___________ 。工业上制成漂白粉的化学方程式:___________ 。
(2)下列物质露置在空气中会变质,在变质过程中既有非氧化还原反应发生,又有氧化还原反应发生的是___________(填字母)。
(3)浸泡衣物时加入漂粉精(有效成分Ca(ClO)2)在空气中放置一段时间漂白效果更好,请用化学方程式解释原因:___________ 。
(4)若将漂白液(有效成分NaClO)与洁厕灵(主要成分是盐酸)混合使用,则会产生有毒气体,其反应的离子方程式是___________ 。
(5)有效氯是漂白粉中有效成分Ca(ClO)2含量大小的标志。
已知:①Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O;
②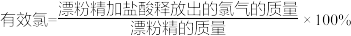 。
。
若某漂粉精的有效氯为60%,该漂粉精中Ca(ClO)2的质量分数为___________ (计算结果保留一位小数)。
 和碱制漂白粉、漂粉精及漂白液。请回答下列问题:
和碱制漂白粉、漂粉精及漂白液。请回答下列问题:(1) Ca(ClO)2中Cl元素的化合价是
(2)下列物质露置在空气中会变质,在变质过程中既有非氧化还原反应发生,又有氧化还原反应发生的是___________(填字母)。
| A.生石灰 | B.漂白粉 |
| C.NaOH | D. |
(4)若将漂白液(有效成分NaClO)与洁厕灵(主要成分是盐酸)混合使用,则会产生有毒气体,其反应的离子方程式是
(5)有效氯是漂白粉中有效成分Ca(ClO)2含量大小的标志。
已知:①Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O;
②
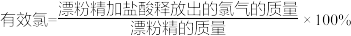 。
。若某漂粉精的有效氯为60%,该漂粉精中Ca(ClO)2的质量分数为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】现有下列物质:①铜②硫酸溶液③CO2④NaHCO3固体⑤Ba(OH)2 固体⑥熔化的KNO3⑦漂粉精⑧红褐色的氢氧化铁胶体 ⑨氨水⑩稀硝酸
(1)⑦的主要成分的化学式是______ ,写出工业上制备⑦的化学方程式______ 。
(2)上述物质属于电解质的有_______ (填编号)。
(3)将④的溶液滴加到NaOH溶液中反应的离子方程式_______ 。
(4)工业废水中含有的重铬酸根离子( )有毒,必须处理达标后才能排放。工业上常用绿矾(FeSO4·7H2O) 做处理剂。将下面的离子方程式配平;
)有毒,必须处理达标后才能排放。工业上常用绿矾(FeSO4·7H2O) 做处理剂。将下面的离子方程式配平;_______ 。口Fe2++口 + 口_______= 口Fe3++口Cr3++ 口。
+ 口_______= 口Fe3++口Cr3++ 口。
(1)⑦的主要成分的化学式是
(2)上述物质属于电解质的有
(3)将④的溶液滴加到NaOH溶液中反应的离子方程式
(4)工业废水中含有的重铬酸根离子(
 )有毒,必须处理达标后才能排放。工业上常用绿矾(FeSO4·7H2O) 做处理剂。将下面的离子方程式配平;
)有毒,必须处理达标后才能排放。工业上常用绿矾(FeSO4·7H2O) 做处理剂。将下面的离子方程式配平; + 口_______= 口Fe3++口Cr3++ 口。
+ 口_______= 口Fe3++口Cr3++ 口。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】某化工厂生产的漂白粉,产品说明书如下:
回答下列问题:
(1)请你为漂白粉写一份保存、使用的注意事项(不超过35字)_____ 。
(2)用化学方程式表示:
①漂白粉的生产原理:______________ ;
②一般情况下,漂白粉失效的主要原因:__________
| 漂白粉使用说明书 主要成分:次氯酸钙、氯化钙 用法用量:每次取漂白粉2 g,水1 000 mL,配成0.2%~0.3%的浊液。 将病人用具浸泡其中5~10分钟,如需要,浓度可提高,时间可延长。 注意事项:…… |
回答下列问题:
(1)请你为漂白粉写一份保存、使用的注意事项(不超过35字)
(2)用化学方程式表示:
①漂白粉的生产原理:
②一般情况下,漂白粉失效的主要原因:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】按要求完成下列填空:
(1)质量数为35,中子数为18的原子__ (微粒符号),其阴离子的结构示意图__ 。
(2)写出下列反应的化学方程式:
①氯气与水反应:___ 。
②漂白粉失效的原理:___ 。
(3)现有下列物质:①铜 ②液态氯化氢 ③稀硫酸 ④二氧化碳 ⑤氯化钠晶体 ⑥熔融的烧碱 ⑦葡萄糖
上述物质中能导电的物质是(填写序号,下同)__ 。属于非电解质的物质为__ 。
(1)质量数为35,中子数为18的原子
(2)写出下列反应的化学方程式:
①氯气与水反应:
②漂白粉失效的原理:
(3)现有下列物质:①铜 ②液态氯化氢 ③稀硫酸 ④二氧化碳 ⑤氯化钠晶体 ⑥熔融的烧碱 ⑦葡萄糖
上述物质中能导电的物质是(填写序号,下同)
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】氯气是一种重要的化工原料。
(1)氯气和石灰乳反应可以制得漂白粉,漂白粉暴露在空气中因吸收了空气中的CO2和H2O而失效,漂白粉失效过程的化学反应方程式为:______ 。
(2)氯水中含有多种成分,因而具有多种性质,根据新制氯水分别与如图四种物质发生的反应填空(a、b、c、d中重合部分代表物质间反应,且氯水足量)。
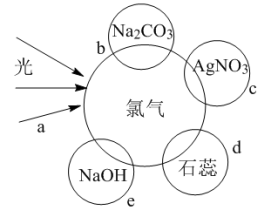
①c过程的反应的离子方程式______ ,e过程中的离子方程式为 _______ 。
②d过程所观察到的现象为:____ ,原因: ____ ,b过程的离子方程式: ______ 。
(1)氯气和石灰乳反应可以制得漂白粉,漂白粉暴露在空气中因吸收了空气中的CO2和H2O而失效,漂白粉失效过程的化学反应方程式为:
(2)氯水中含有多种成分,因而具有多种性质,根据新制氯水分别与如图四种物质发生的反应填空(a、b、c、d中重合部分代表物质间反应,且氯水足量)。

①c过程的反应的离子方程式
②d过程所观察到的现象为:
您最近一年使用:0次



