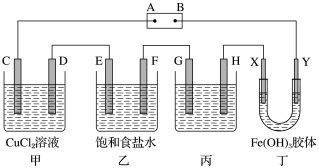
课题式研究性学习是培养学生创造思维的良好方法,某研究性学习小组将下列装置如图连接,C、D、E、F、X、Y 都是惰性电极。将电源接通后,向乙中滴入酚酞试液,在F极附近显红色。试回答下列问题:
(1)电源A 极的名称是________ 。
(2)甲装置中电解反应的总化学方程式是__________________ 。
(3)如果收集乙装置中产生的气体,两种气体的体积比是________ 。
(4)欲用丙装置精炼铜,G应该是____ (填“纯铜”或“粗铜”),电解液的成分是______ 。
(5)已知氢氧化铁胶体中含有带正电荷的红褐色的粒子,那么装置丁中的现象是________________ 。
(6)在实验室电解500 mL 0.03 mol/L的NaCl溶液,通电一段时间后溶液中c(OH-)为1×10-2 mol/L(设电解时溶液的体积变化忽略不计),阴极产生___ mL(标况)气体,溶液中NaCl的浓度为_______ mol/L。

(1)电源A 极的名称是
(2)甲装置中电解反应的总化学方程式是
(3)如果收集乙装置中产生的气体,两种气体的体积比是
(4)欲用丙装置精炼铜,G应该是
(5)已知氢氧化铁胶体中含有带正电荷的红褐色的粒子,那么装置丁中的现象是
(6)在实验室电解500 mL 0.03 mol/L的NaCl溶液,通电一段时间后溶液中c(OH-)为1×10-2 mol/L(设电解时溶液的体积变化忽略不计),阴极产生
更新时间:2020-05-11 10:48:24
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】某学习小组将有关“电解饱和食盐水”的相关内容进行梳理,形成如下问题(显示的电极均为石墨)。
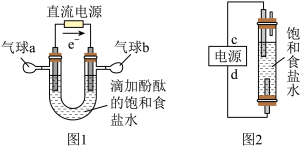
(1)图 1 中,电解一段时间后,气球 b 中的气体是___ (填化学式),U 形管___ (填“左”或“右”)边的溶液变红。
(2)利用图 2 制作一种环保型消毒液发生器,电解可制备“84”消毒液的有效成分,则 c 为电源的_____ 极;该发生器中反应的总离子方程式为_____ 。
(3)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能 30%以上。该工艺的相关物质运输与转化关系如图 3 所示(其中的电极未标出,所用的离子膜都只允许阳离子通过)。
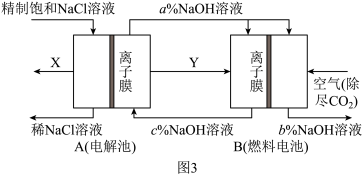
燃料电池 B 中的电极反应式分别为负极_____ , 正极____ 。

(1)图 1 中,电解一段时间后,气球 b 中的气体是
(2)利用图 2 制作一种环保型消毒液发生器,电解可制备“84”消毒液的有效成分,则 c 为电源的
(3)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能 30%以上。该工艺的相关物质运输与转化关系如图 3 所示(其中的电极未标出,所用的离子膜都只允许阳离子通过)。

燃料电池 B 中的电极反应式分别为负极
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】利用电解法转化 可实现
可实现 资源化利用。
资源化利用。
(1)以过渡金属为催化剂电解 制
制 的原理示意图如图所示。
的原理示意图如图所示。
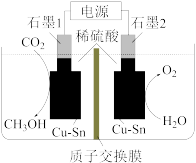
①石墨电极1上发生反应的电极反应式为___________ 。
②石墨电极2上发生反应的电极反应式为___________ 。
③电解的总反应方程式为___________ 。
(2)电解 制
制 的原理示意图如图所示。
的原理示意图如图所示。

①阴极上 与
与 反应时,
反应时, 还原为
还原为 的电极反应式为
的电极反应式为___________ 。
②阳极室排出的气体的化学式为___________ 。
③电解一段时间后,阳极区的 溶液浓度降低,其原因是
溶液浓度降低,其原因是___________ 。
 可实现
可实现 资源化利用。
资源化利用。(1)以过渡金属为催化剂电解
 制
制 的原理示意图如图所示。
的原理示意图如图所示。
①石墨电极1上发生反应的电极反应式为
②石墨电极2上发生反应的电极反应式为
③电解的总反应方程式为
(2)电解
 制
制 的原理示意图如图所示。
的原理示意图如图所示。
①阴极上
 与
与 反应时,
反应时, 还原为
还原为 的电极反应式为
的电极反应式为②阳极室排出的气体的化学式为
③电解一段时间后,阳极区的
 溶液浓度降低,其原因是
溶液浓度降低,其原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】I.装置如图所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极。将直流电源接通后,F极附近呈红色。氢氧化铁胶体的胶粒带正电荷。请回答:

(1)B极是电源的_________ 极,C极的电极反应式为_________ ,甲中溶液的pH_________ (填“变大“变小”或“不变”)。一段时间后丁中X极附近的颜色逐渐_________ (填“变深”或“变浅”)。
(2)现用丙装置给铜件镀银,则H应该是_________ (填“铜”或“银”)。常温下,当乙中溶液的OH-浓度为0.1mol/L(此时乙溶液体积为500mL),丙中镀件上析出银的质量为_________ g。
(3)若甲、乙装置中的C、D、E、F电极均只有一种单质生成时,对应单质的物质的量之比为_________ 。
(4)若工作一段时间后停止通电,此时,甲中C、D两极上都产生2.24L气体(标准状况),欲使溶液恢复到起始状态,可向溶液中加入_________(填序号)。
(5)若将C电极换为铁,其他装置都不变,则甲中发生的总反应的离子方程式为_________ 。
II.以Fe、Ni为电极制取Na2FeO4的原理如图所示。通电后,在铁电极附近生成紫红色的FeO ,若pH过高,铁电极区会产生红褐色物质。
,若pH过高,铁电极区会产生红褐色物质。
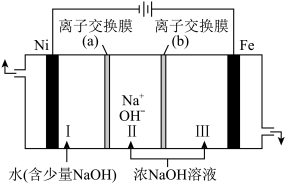
(6)电解时阳极的电极反应式为_________ ,离子交换膜(b)为_________ ,(填“阴”或“阳”)离子交换膜。

(1)B极是电源的
(2)现用丙装置给铜件镀银,则H应该是
(3)若甲、乙装置中的C、D、E、F电极均只有一种单质生成时,对应单质的物质的量之比为
(4)若工作一段时间后停止通电,此时,甲中C、D两极上都产生2.24L气体(标准状况),欲使溶液恢复到起始状态,可向溶液中加入_________(填序号)。
| A.CuO | B.Cu2(OH)2CO3 | C.Cu(OH)2 | D.CuCO3 |
II.以Fe、Ni为电极制取Na2FeO4的原理如图所示。通电后,在铁电极附近生成紫红色的FeO
 ,若pH过高,铁电极区会产生红褐色物质。
,若pH过高,铁电极区会产生红褐色物质。
(6)电解时阳极的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】高锰酸钾是一种常用的消毒剂和氧化剂。回答下列问题:
实验(一):电解法制备 。
。
以石墨、铜为电极,电解 溶液制备
溶液制备 溶液,装置如图所示。
溶液,装置如图所示。

(1)电解过程中,Cu极附近电解质溶液的pH___________ (填“升高”“降低”或“不变”)。阳极的电极反应式为___________ 。
(2)铜极、石墨极能否互换并简述理由:___________ 。
实验(二):探究 和
和 氧化性强弱。装置如图所示。
氧化性强弱。装置如图所示。
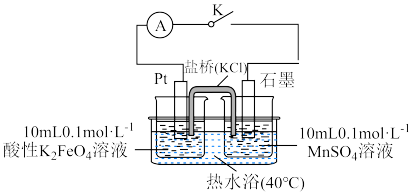
关闭开关K,观察到左烧杯中紫红色溶液变为浅黄色,右烧杯中无色溶液变为紫红色。
(3)关闭K,盐桥中___________ 向左烧杯迁移。盐桥的主要作用是___________ 。
(4)正极反应式为___________ ,实验结论是氧化性:
___________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
实验(三):探究影响草酸和酸性 溶液反应的因素(
溶液反应的因素( ,
,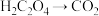 )。
)。
为了探究外界条件改变对反应速率的影响,设计如下实验方案:
(5)通过实验①、②可探究___________ 的改变对反应速率的影响。
(6)在一定 溶液中加入适量硫酸,再加入一定量草酸溶液,产生
溶液中加入适量硫酸,再加入一定量草酸溶液,产生 体积(同温同压)与反应时间的关系如图所示(水浴温度保持35℃)。
体积(同温同压)与反应时间的关系如图所示(水浴温度保持35℃)。
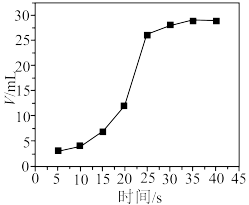
 时间段反应速率突增,其原因可能是
时间段反应速率突增,其原因可能是___________ 。
实验(一):电解法制备
 。
。以石墨、铜为电极,电解
 溶液制备
溶液制备 溶液,装置如图所示。
溶液,装置如图所示。
(1)电解过程中,Cu极附近电解质溶液的pH
(2)铜极、石墨极能否互换并简述理由:
实验(二):探究
 和
和 氧化性强弱。装置如图所示。
氧化性强弱。装置如图所示。
关闭开关K,观察到左烧杯中紫红色溶液变为浅黄色,右烧杯中无色溶液变为紫红色。
(3)关闭K,盐桥中
(4)正极反应式为

 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。实验(三):探究影响草酸和酸性
 溶液反应的因素(
溶液反应的因素( ,
,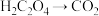 )。
)。为了探究外界条件改变对反应速率的影响,设计如下实验方案:
| 实验 序号 | 实验温度/℃ |  溶液(含硫酸) 溶液(含硫酸) |  溶液 溶液 |  | 溶液颜色褪至无色时所需时间/s | ||
 |  |  |  |  | |||
| ① | 20 | 2 | 0.02 | 5 | 0.1 | 5 |  |
| ② | 20 | 2 | 0.02 | 4 | 0.1 | 6 | 10 |
| ③ | 40 | 2 | 0.02 | 4 | 0.1 | 6 |  |
(5)通过实验①、②可探究
(6)在一定
 溶液中加入适量硫酸,再加入一定量草酸溶液,产生
溶液中加入适量硫酸,再加入一定量草酸溶液,产生 体积(同温同压)与反应时间的关系如图所示(水浴温度保持35℃)。
体积(同温同压)与反应时间的关系如图所示(水浴温度保持35℃)。
 时间段反应速率突增,其原因可能是
时间段反应速率突增,其原因可能是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】甲醇(CH3OH)燃料电池的工作原理如图甲所示,回答下列问题:

(1)该电池工作时,b口通入的物质为________ (填化学式,下同),c口通入的物质为________ 。
(2)该电池负极的电极反应式为________ 。
(3)精炼铜时,粗铜应与甲醇燃料电池的________ (填“正”或“负”)极相连,阴极的电极反应式为________ ,电解质溶液为________ 。
(4)以该燃料电池作电源,在实验室中模拟铝制品表面“钝化”处理的过程中,发现溶液逐渐变浑浊(如图乙),原因是:________ (用相关的电极反应式表示)。

(1)该电池工作时,b口通入的物质为
(2)该电池负极的电极反应式为
(3)精炼铜时,粗铜应与甲醇燃料电池的
(4)以该燃料电池作电源,在实验室中模拟铝制品表面“钝化”处理的过程中,发现溶液逐渐变浑浊(如图乙),原因是:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】电解原理在化学工业中有广泛的应用。如图表示一个电解池,装有电解液a,X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:
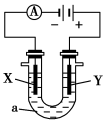
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则:
①电解池中X极上的电极反应式为_______ ,在X极附近观察到的现象是_______ 。电解液中向X极方向移动的离子是_______ 。
②Y电极上的电极反应式为_______ 。
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则:
①X电极的材料是_______ ,电极反应式为_______ 。
②Y电极的材料是_______ ,电极反应式为_______ 。
(2)某新型可充电电池,能长时间保持稳定的放电电压,该电池的总反应3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH。
3Zn(OH)2+2Fe(OH)3+4KOH。
①放电时负极反应式为_______ ;
②充电时Fe(OH)3发生_______ 反应;(填“氧化”或“还原”)
③放电时1 mol K2FeO4发生反应,转移电子数是_______ 。

(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则:
①电解池中X极上的电极反应式为
②Y电极上的电极反应式为
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则:
①X电极的材料是
②Y电极的材料是
(2)某新型可充电电池,能长时间保持稳定的放电电压,该电池的总反应3Zn+2K2FeO4+8H2O
 3Zn(OH)2+2Fe(OH)3+4KOH。
3Zn(OH)2+2Fe(OH)3+4KOH。①放电时负极反应式为
②充电时Fe(OH)3发生
③放电时1 mol K2FeO4发生反应,转移电子数是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】Ⅰ某兴趣小组的同学用下图所示装置研究有关电化学的问题 甲、乙、丙三池中溶质足量
甲、乙、丙三池中溶质足量 ,当闭合该装置的开关K时,观察到电流计的指针发生了偏转。请回答下列问题:
,当闭合该装置的开关K时,观察到电流计的指针发生了偏转。请回答下列问题:
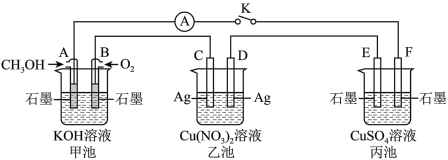
(1)甲、乙、丙三池中为原电池的是______ (填“甲池”、“乙池”或“丙池”)。
(2)写出甲池中A电极的电极反应式____________ 。
(3)丙池中F电极为______ (填“正极”、“负极”、“阴极”或“阳极”),该池的总反应化学方程式为_________ 。
(4)当乙池中C电极质量减轻 时,甲池中B电极理论上消耗
时,甲池中B电极理论上消耗 的体积为
的体积为____ mL(标况)。
(5)一段时间后,断开开关K。下列物质能使丙池恢复到反应前浓度的是____ (填选项字母)。
A.Cu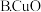
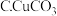

Ⅱ控制适合的条件,将反应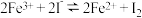 ,设计成如上图所示装置。请回答下列问题:
,设计成如上图所示装置。请回答下列问题:
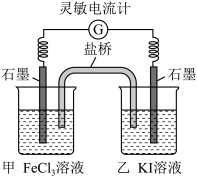
(6)反应开始时,乙中石墨电极上发生___ (填“氧化”或“还原”)反应,电极反应式为_______ 。盐桥中的__ (填“阳”或“阴”)离子向甲溶液方向移动。
(7)电流计读数为0时,反应达到平衡状态,此时在甲中加入 固体,则甲中的石墨作
固体,则甲中的石墨作______  填“正”或“负”
填“正”或“负” 极,该电极的电极反应式为
极,该电极的电极反应式为_______________ 。
(Ⅲ)高铁电池是一种新型可充电电池,与普通高能电池相比,该电池长时间保持稳定的放电电压。高铁电池的总反应为: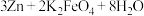

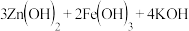 。
。
(8)放电时负极反应为______ , 充电时阳极反应为_______ ,放电时正极附近溶液的碱性___  选填“增强”“减弱”或“不变”
选填“增强”“减弱”或“不变” 。
。
 甲、乙、丙三池中溶质足量
甲、乙、丙三池中溶质足量 ,当闭合该装置的开关K时,观察到电流计的指针发生了偏转。请回答下列问题:
,当闭合该装置的开关K时,观察到电流计的指针发生了偏转。请回答下列问题:
(1)甲、乙、丙三池中为原电池的是
(2)写出甲池中A电极的电极反应式
(3)丙池中F电极为
(4)当乙池中C电极质量减轻
 时,甲池中B电极理论上消耗
时,甲池中B电极理论上消耗 的体积为
的体积为(5)一段时间后,断开开关K。下列物质能使丙池恢复到反应前浓度的是
A.Cu
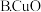
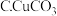

Ⅱ控制适合的条件,将反应
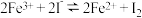 ,设计成如上图所示装置。请回答下列问题:
,设计成如上图所示装置。请回答下列问题:
(6)反应开始时,乙中石墨电极上发生
(7)电流计读数为0时,反应达到平衡状态,此时在甲中加入
 固体,则甲中的石墨作
固体,则甲中的石墨作 填“正”或“负”
填“正”或“负” 极,该电极的电极反应式为
极,该电极的电极反应式为(Ⅲ)高铁电池是一种新型可充电电池,与普通高能电池相比,该电池长时间保持稳定的放电电压。高铁电池的总反应为:
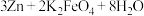

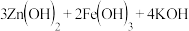 。
。(8)放电时负极反应为
 选填“增强”“减弱”或“不变”
选填“增强”“减弱”或“不变” 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】I.载人航天工程对科学研究及太空资源开发具有重要意义,中国正逐步建立自己的载人空间站“天宫”,神舟十三号载人飞船在北京时间10月16日0时23分点火发射,又一次踏上飞向浩渺星辰的征途。
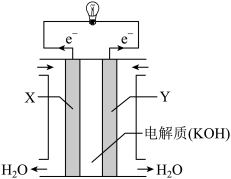
(1)氢氧燃料电池(构造如图)单位质量输出电能较高,反应生成的水可作为航天员的饮用水,氧气可以作为备用氧源供给航天员呼吸。由此判断Y极为电池的_______ 极,OH-向_______ (填“正”或“负”)极作定向移动,Y极的电极反应式为_________________ 。
(2)“神舟”飞船的电源系统共有3种,分别是太阳能电池帆板、镉镍蓄电池和应急电池。
①飞船在光照区运行时,太阳能电池帆板将_______ 能转化为电能,除供给飞船使用外,多余部分用镉镍蓄电池储存起来。其工作原理为:Cd+2NiOOH+2H2O Cd(OH)2+2Ni(OH)2,充电时,阳极的电极反应式为
Cd(OH)2+2Ni(OH)2,充电时,阳极的电极反应式为_________________ 。
②紧急状况下,应急电池会自动启动,工作原理为Zn+Ag2O+H2O 2Ag+Zn(OH)2,其负极溶液的碱性
2Ag+Zn(OH)2,其负极溶液的碱性____ (填“增大”“减小”或“不变”)。
Ⅱ.如图所示,某研究性学习小组利用上述燃烧原理设计一个肼(N2H4)─空气燃料电池(如图甲,已知肼反应生成N2)并探究某些工业原理,其中乙装置中X为阳离子交换膜(即只允许阳离子通过)。根据要求回答相关问题:
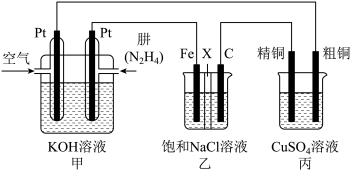
(3)甲装置中通入______ 的一极为正极;乙装置中电解一段时间后溶液呈_____ 性,此时若将乙池中石墨(C)电极换成Mg电极,电极反应变为:__________________ 。
(4)图中用丙装置模拟工业中的粗铜的精炼原理,如果电解后丙装置精铜质量增加3.2g,则理论上甲装置中肼消耗质量为______ g。
(1)氢氧燃料电池(构造如图)单位质量输出电能较高,反应生成的水可作为航天员的饮用水,氧气可以作为备用氧源供给航天员呼吸。由此判断Y极为电池的

(2)“神舟”飞船的电源系统共有3种,分别是太阳能电池帆板、镉镍蓄电池和应急电池。
①飞船在光照区运行时,太阳能电池帆板将
 Cd(OH)2+2Ni(OH)2,充电时,阳极的电极反应式为
Cd(OH)2+2Ni(OH)2,充电时,阳极的电极反应式为②紧急状况下,应急电池会自动启动,工作原理为Zn+Ag2O+H2O
 2Ag+Zn(OH)2,其负极溶液的碱性
2Ag+Zn(OH)2,其负极溶液的碱性Ⅱ.如图所示,某研究性学习小组利用上述燃烧原理设计一个肼(N2H4)─空气燃料电池(如图甲,已知肼反应生成N2)并探究某些工业原理,其中乙装置中X为阳离子交换膜(即只允许阳离子通过)。根据要求回答相关问题:

(3)甲装置中通入
(4)图中用丙装置模拟工业中的粗铜的精炼原理,如果电解后丙装置精铜质量增加3.2g,则理论上甲装置中肼消耗质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】相同金属在其不同浓度盐溶液中可形成浓差电池,当两个电极区的浓度相等时停止放电。如图所示装置是利用浓差电池电解 溶液(a、b电极均为石墨电极),可以制得
溶液(a、b电极均为石墨电极),可以制得 、
、 、
、 和NaOH,实验前Cu(I)电极和Cu(II)电极质量相等。
和NaOH,实验前Cu(I)电极和Cu(II)电极质量相等。
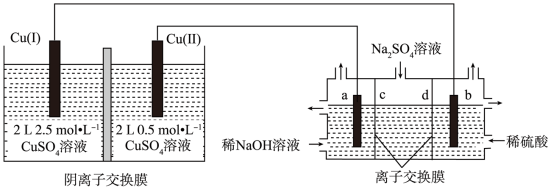
(1)Cu(I)电极为_______ 极,a电极的电极反应为_______ 。
(2)c膜为_______ (填“阳离子交换膜”或“阴离子交换膜”)。
(3)电池从开始工作到停止放电,Cu(I)电极和Cu(II)电极质量差为_______ g,电解池理论上可制得_______ gNaOH。
 溶液(a、b电极均为石墨电极),可以制得
溶液(a、b电极均为石墨电极),可以制得 、
、 、
、 和NaOH,实验前Cu(I)电极和Cu(II)电极质量相等。
和NaOH,实验前Cu(I)电极和Cu(II)电极质量相等。
(1)Cu(I)电极为
(2)c膜为
(3)电池从开始工作到停止放电,Cu(I)电极和Cu(II)电极质量差为
您最近一年使用:0次



