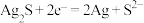一种镁-过氧化氢燃料电池的原理为Mg + H2O2 + H2SO4=MgSO4+ 2H2O ,其装置如图所示。下列说法错误的是
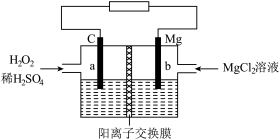

| A.a极发生还原反应 | B.电子由b极经电解质溶液流向a极 |
| C.Mg2+由右侧经过阳离子交换膜移向左侧 | D.b极电极反应式为Mg-2e-=Mg2+ |
更新时间:2020/05/14 09:44:25
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】一种水性电解液Al- PbO2离子选择隔膜电池如图所示{ KOH溶液中,Al3+以[Al(OH)4]-的形式存在)。电池放电时,下列叙述正确的是
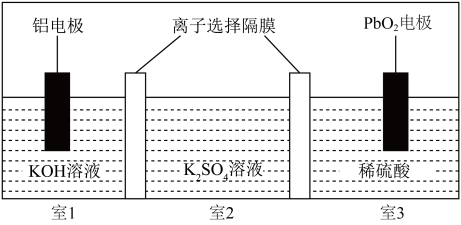

A.27 g Al参与反应,有1 mol  从室2向室1迁移。 从室2向室1迁移。 |
| B.负极的电极反应式为2Al- 6e-+8OH-=2[ Al(OH)4]- |
| C.一段时间后,室2溶液浓度一定会减小 |
| D.电路上转移1mol电子时,理论上PbO2电极质量净减32g |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】目前科学家已开发出一种新型燃料电池—固体氧化物电池,该电池用辛烷(C8H18)作燃料,电池中间部分的固体氧化物陶瓷可传递O2-,下列说法正确的是
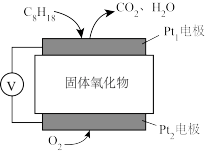

| A.电池工作时,氧气发生氧化反应 |
| B.电池正极的电极反应式:O2+2H2O+4e-=4OH- |
| C.电子由Pt2电极经外电路流向Pt1电极 |
| D.电池的总反应为2C8H18+25O2=16CO2+18H2O |
您最近一年使用:0次

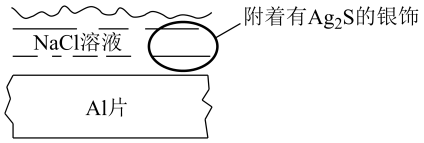
 而发黑,将银饰与
而发黑,将银饰与 片接触并加入
片接触并加入 溶液,发生原电池反应可以除去银饰表面的
溶液,发生原电池反应可以除去银饰表面的