FeCl2是中学化学常用试剂。请根据题意填空:
往FeCl2溶液中加入KSCN溶液,溶液___ (填“变”或“不变”)色,再往其中通入氯气,溶液呈___ (填“红”或“蓝”)色。除去FeCl2溶液中少量的FeCl3应加(通)入的试剂为___ (填“Fe”或“Cl2”)。
往FeCl2溶液中加入KSCN溶液,溶液
更新时间:2020-05-26 02:24:20
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】物质检验、分离、提纯和制备是化学实验中的常见操作。
(1)除去FeCl3溶液中混有的FeCl2可采取的方法是_______ (用离子方程式表示)。
(2)检验食盐中所含阳离子的实验操作名称是_______ 。
(3)检验Fe2(SO4)3溶液中是否含有FeSO4所用试剂是_______ 。
(4)除去Cl2中混有的HCl气体所用的试剂是_______ 。
(5)实验室制备氯气的化学反应方程式为_______ 请在方程式中标出电子转移的方向和数目。
(1)除去FeCl3溶液中混有的FeCl2可采取的方法是
(2)检验食盐中所含阳离子的实验操作名称是
(3)检验Fe2(SO4)3溶液中是否含有FeSO4所用试剂是
(4)除去Cl2中混有的HCl气体所用的试剂是
(5)实验室制备氯气的化学反应方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】铁及其化合物在日常生产生活中应用广泛,研究铁及其化合物的应用意义重大。
(1)所含铁元素只有还原性的物质是___________。
(2)当人体缺铁时,往往需要吃补铁保健品。人体能够吸收的是+2价的铁,但是+2价的铁很容易被氧化。
①如何检验某固体补铁剂中铁元素已被氧化?写出操作过程、现象及结论。
答:研细后用盐酸溶解,___________ 。
②服用维生素C,可使食物中的三价铁离子转化为二价铁离子。由此可推知,维生素C具有___________ (填化学性质)。
(3)高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂。湿法制备高铁酸钾(K2FeO4)的反应体系中有六种微粒:Fe(OH)3、C1O-、OH-、FeO 、Cl-、H2O。写出并配平湿法制高铁酸钾的离子反应方程式:
、Cl-、H2O。写出并配平湿法制高铁酸钾的离子反应方程式:___________
______Fe(OH)3+_______ClO-+_______=_______FeO +_______Cl-+_______
+_______Cl-+_______
(4)工业上用氯化铁腐蚀铜箔、制造电路板。某工程师为了从使用过的腐蚀废液中回收铜,并获得氯化铁晶体,准备采用下列步骤:

回答下列问题:
①试剂a是___________ ,操作I用到的玻璃仪器有烧杯、玻璃棒和___________ 。
②滤液X、Z中都有同一种溶质,它们转化为溶液W的离子方程式为___________ 。
③上述流程中操作Ⅲ包括:蒸发浓缩、___________ 、过滤、洗涤。
(1)所含铁元素只有还原性的物质是___________。
| A.Fe | B.FeCl2 | C.FeCl3 | D.Fe2O3 |
(2)当人体缺铁时,往往需要吃补铁保健品。人体能够吸收的是+2价的铁,但是+2价的铁很容易被氧化。
①如何检验某固体补铁剂中铁元素已被氧化?写出操作过程、现象及结论。
答:研细后用盐酸溶解,
②服用维生素C,可使食物中的三价铁离子转化为二价铁离子。由此可推知,维生素C具有
(3)高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂。湿法制备高铁酸钾(K2FeO4)的反应体系中有六种微粒:Fe(OH)3、C1O-、OH-、FeO
 、Cl-、H2O。写出并配平湿法制高铁酸钾的离子反应方程式:
、Cl-、H2O。写出并配平湿法制高铁酸钾的离子反应方程式:______Fe(OH)3+_______ClO-+_______=_______FeO
 +_______Cl-+_______
+_______Cl-+_______(4)工业上用氯化铁腐蚀铜箔、制造电路板。某工程师为了从使用过的腐蚀废液中回收铜,并获得氯化铁晶体,准备采用下列步骤:

回答下列问题:
①试剂a是
②滤液X、Z中都有同一种溶质,它们转化为溶液W的离子方程式为
③上述流程中操作Ⅲ包括:蒸发浓缩、
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】“纳米零价铁—H2O2”体系可将烟气中难溶的NO氧化为可溶的 。
。
(1)制备纳米零价铁:将FeSO4溶液与碱性NaBH4溶液混合可生成纳米零价铁、H2和NaBO2等,该反应的离子方程式为_______ (NaBH4、NaBO2中B元素均为+3价)。
(2)NO的氧化:在一定温度下,将H2O2溶液和HCl溶液雾化后与烟气按一定比例混合,以一定流速通过装有纳米零价铁的反应装置,可将烟气中的NO氧化。
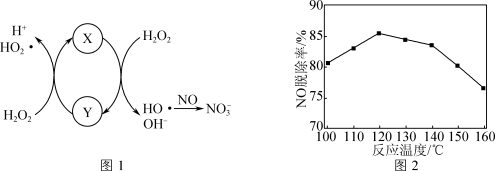
①Fe2+催化H2O2分解产生HO·,HO·将NO氧化为 的机理如图1所示,Y的化学式为
的机理如图1所示,Y的化学式为_______ 。
②NO与H2O2反应生成HNO3的化学方程式为_______ 。
③NO脱除率随温度的变化如图2所示。温度高于120℃时,NO脱除率随温度升高呈现下降趋势的主要原因是_______ 。
 。
。(1)制备纳米零价铁:将FeSO4溶液与碱性NaBH4溶液混合可生成纳米零价铁、H2和NaBO2等,该反应的离子方程式为
(2)NO的氧化:在一定温度下,将H2O2溶液和HCl溶液雾化后与烟气按一定比例混合,以一定流速通过装有纳米零价铁的反应装置,可将烟气中的NO氧化。
①Fe2+催化H2O2分解产生HO·,HO·将NO氧化为
 的机理如图1所示,Y的化学式为
的机理如图1所示,Y的化学式为②NO与H2O2反应生成HNO3的化学方程式为
③NO脱除率随温度的变化如图2所示。温度高于120℃时,NO脱除率随温度升高呈现下降趋势的主要原因是

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】铁及其重要化合物的“价类二维图”如下图所示。
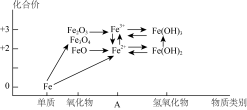
(1)该“价类二维图”中缺失的类别A应为_______ 。
(2)生活中的钢铁制品如废旧铁锅,使用时间长久后若要丢弃,应归为_______。
(3)某实验小组在探究实验后,想要检验废液中是否存在Fe3+,该怎么做?_______ 。
(4)将足量铁粉投入溴化铁溶液中充分反应,写出该反应的化学方程式_______ 。
(5)在上述反应液中继续加入足量氯水,此时溶液中发生反应的离子方程式为_______ 。
(6)工业上曾经通过反应“3Fe+4NaOH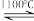 Fe3O4+2H2↑+4Na↑”生产金属钠,下列说法正确的是_______。
Fe3O4+2H2↑+4Na↑”生产金属钠,下列说法正确的是_______。

(1)该“价类二维图”中缺失的类别A应为
(2)生活中的钢铁制品如废旧铁锅,使用时间长久后若要丢弃,应归为_______。
| A.干垃圾 | B.湿垃圾 | C.有毒有害垃圾 | D.可回收垃圾 |
(4)将足量铁粉投入溴化铁溶液中充分反应,写出该反应的化学方程式
(5)在上述反应液中继续加入足量氯水,此时溶液中发生反应的离子方程式为
(6)工业上曾经通过反应“3Fe+4NaOH
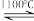 Fe3O4+2H2↑+4Na↑”生产金属钠,下列说法正确的是_______。
Fe3O4+2H2↑+4Na↑”生产金属钠,下列说法正确的是_______。| A.用磁铁可以将Fe与Fe3O4分离 | B.该反应条件下铁的氧化性比钠强 |
| C.每生成1 mol H2,转移的电子为4 mol | D.将生成的气体在空气中冷却可获得钠 |
您最近一年使用:0次
【推荐2】某兴趣小组研究亚硝酸钠,查阅下列资料,试根据信息回答下列问题。
(1)已知NaNO2能发生如下反应: 2NaNO2+4HI=2NO↑+I2+2NaI+2H2O。请用双线桥表示电子转移的方向和数目。________________ ;该反应中氧化剂是_____ ;若有0.75mol电子转移,则被还原的氧化剂粒子数为_______ 。(用NA表示)
(2)误食NaNO2会导致血红蛋白中的Fe2+转化为Fe3+而中毒,可服用维生素C解毒。下列分析错误的是______ (填序号)。
A.NaNO2被还原 B.维生素C具有还原性
C.还原性: 维生素C > Fe2+ D.NaNO2是还原剂
(3)下列方法中,可用来区分NaNO2和NaCl的是______ (填序号)。
A. 焰色反应 B.分别滴加酸化FeSO4溶液和KSCN溶液
C.在酸性条件下加入KI 淀粉溶液 D.分别滴加AgNO3溶液
(4)某同学把新制的氯水加到NaNO2溶液中,观察到氯水褪色,同时生成NaNO3和HCl,请写出反应的离子方程式:_______________ 。
| 药品 | NaNO2 (亚硝酸钠) |
| 性质 | 1.在酸性溶液中有较强氧化性,能将Fe2+ 氧化成Fe3+ ; 2.AgNO2是一种难溶于水、易溶于酸的盐。 |
(1)已知NaNO2能发生如下反应: 2NaNO2+4HI=2NO↑+I2+2NaI+2H2O。请用双线桥表示电子转移的方向和数目。
(2)误食NaNO2会导致血红蛋白中的Fe2+转化为Fe3+而中毒,可服用维生素C解毒。下列分析错误的是
A.NaNO2被还原 B.维生素C具有还原性
C.还原性: 维生素C > Fe2+ D.NaNO2是还原剂
(3)下列方法中,可用来区分NaNO2和NaCl的是
A. 焰色反应 B.分别滴加酸化FeSO4溶液和KSCN溶液
C.在酸性条件下加入KI 淀粉溶液 D.分别滴加AgNO3溶液
(4)某同学把新制的氯水加到NaNO2溶液中,观察到氯水褪色,同时生成NaNO3和HCl,请写出反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】H2S是一种无色、有毒的可燃性气体,其水溶液叫氢硫酸(二元弱酸)。
(1)实验室可用硫化亚铁固体与稀硫酸反应来制备H2S气体。
①该反应的化学方程式为____________________________ 。
②多余的H2S气体可用_____________ 溶液来吸收,不能用燃烧的方法处理H2S气体的理由是___________ 。
(2)用30% FeCl3溶液作吸收液也能吸收H2S气体,反应方程式为:2FeCl3+H2S = S↓+2FeCl2+2HCl,废吸收液经电解可循环使用。
①该反应中H2S显__________ (填字母)。
a、不稳定性 b、弱酸性 c、氧化性 d、还原性
②检验废吸收液中是否含有Fe3+的适宜试剂是___________ 。
③强酸性的废吸收液电解可生成FeCl3和一种分子量最小的气体,则化学方程式为____________ 。
(3)已知:H2S在高温下分解生成硫蒸气和H2。现测得某温度下,H2S分解过程中各物质的物质的量随时间变化关系如图所示。
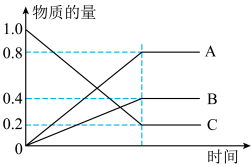
①表示H2的曲线是__________ (填“A”、“B”或“C”)。
②生成硫蒸气的分子式为__________ 。
(1)实验室可用硫化亚铁固体与稀硫酸反应来制备H2S气体。
①该反应的化学方程式为
②多余的H2S气体可用
(2)用30% FeCl3溶液作吸收液也能吸收H2S气体,反应方程式为:2FeCl3+H2S = S↓+2FeCl2+2HCl,废吸收液经电解可循环使用。
①该反应中H2S显
a、不稳定性 b、弱酸性 c、氧化性 d、还原性
②检验废吸收液中是否含有Fe3+的适宜试剂是
③强酸性的废吸收液电解可生成FeCl3和一种分子量最小的气体,则化学方程式为
(3)已知:H2S在高温下分解生成硫蒸气和H2。现测得某温度下,H2S分解过程中各物质的物质的量随时间变化关系如图所示。

①表示H2的曲线是
②生成硫蒸气的分子式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】Ⅰ、运用铁及其化合物的知识,完成下列各题。
(1)下列物质跟铁反应后的生成物,能跟KSCN溶液作用生成红色溶液的是________ 。
A.盐酸 B.氯气 C.CuSO4溶液 D.稀硫酸
(2)把过量的铁粉加入稀硝酸中,其结果是________ 。
A.不反应 B.生成硝酸铁 C.生成硝酸亚铁
(3)要除去FeCl2溶液中的少量FeCl3,可行的办法是________ 。
A.滴入KSCN溶液 B.通入氯气 C.加入铜粉 D.加入铁粉
Ⅱ、工业上硝酸的制备和自然界中硝酸的生成既有相同的地方,又有区别。线路①、②、③是工业生产硝酸的主要途径,线路Ⅰ、Ⅱ、Ⅲ是雷电高能固氮过程中硝酸的生成途径。
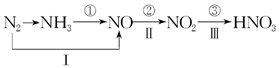
(1)写出①步反应的化学方程式:____________________________________________________ 。
(2)下列环境问题与NO2的排放有关的是________ (填字母序号)。
A.赤潮 B.光化学烟雾 C.臭氧空洞 D.温室效应 E.酸雨
(3)若将12.8 g铜跟一定量的浓硝酸反应,铜消耗完时,共产生气体5.6 L(标准状况),则所消耗的硝酸的物质的量是________ 。
(1)下列物质跟铁反应后的生成物,能跟KSCN溶液作用生成红色溶液的是
A.盐酸 B.氯气 C.CuSO4溶液 D.稀硫酸
(2)把过量的铁粉加入稀硝酸中,其结果是
A.不反应 B.生成硝酸铁 C.生成硝酸亚铁
(3)要除去FeCl2溶液中的少量FeCl3,可行的办法是
A.滴入KSCN溶液 B.通入氯气 C.加入铜粉 D.加入铁粉
Ⅱ、工业上硝酸的制备和自然界中硝酸的生成既有相同的地方,又有区别。线路①、②、③是工业生产硝酸的主要途径,线路Ⅰ、Ⅱ、Ⅲ是雷电高能固氮过程中硝酸的生成途径。

(1)写出①步反应的化学方程式:
(2)下列环境问题与NO2的排放有关的是
A.赤潮 B.光化学烟雾 C.臭氧空洞 D.温室效应 E.酸雨
(3)若将12.8 g铜跟一定量的浓硝酸反应,铜消耗完时,共产生气体5.6 L(标准状况),则所消耗的硝酸的物质的量是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】除杂质:所选试剂都填化学式
(1) 除去混入NaCl溶液中少量NaHCO3杂质的试剂是_________ ,离子方程式为__________ 。
(2) 除去FeCl2溶液中混入的FeCl3溶液杂质用试剂是________ ,离子方程式为_______________ 。
(3)除去Mg粉中混有的少量Al杂质的试剂是_________ ,离子方程式为________________ 。
(4)除去NaHCO3溶液中混有的少量Na2CO3 杂质的试剂是_________ ,离子方程式为_________ 。
(1) 除去混入NaCl溶液中少量NaHCO3杂质的试剂是
(2) 除去FeCl2溶液中混入的FeCl3溶液杂质用试剂是
(3)除去Mg粉中混有的少量Al杂质的试剂是
(4)除去NaHCO3溶液中混有的少量Na2CO3 杂质的试剂是
您最近一年使用:0次



