A、B、D、E、F、G为短周期元素,且原子序数依次递增。A、F同主族,E、G同主族。A与其他非金属元素化合时易形成共价键,F与其他非金属元素化合时易形成离子键,且F+与E2-核外电子排布相同。由以上元素组成的物质BE和D2具有相同的电子数。
请回答下列问题:
(1)F位于第________ 周期第________ 族。
(2)G的离子结构示意图为_______________________________________________ 。
(3)用电子式表示D2的形成过程:________________________________________ 。
(4)由A、E、F三种元素形成的化合物的化学式为________ ,属于________ 化合物。
(5)B的最高价是________ ,由A、B组成的化合物中,含A的质量分数最高的物质的化学式是________ ;A、B组成的化合物中与D2相对分子质量相等的物质的化学式是________ ,有________ 对共用电子对。
请回答下列问题:
(1)F位于第
(2)G的离子结构示意图为
(3)用电子式表示D2的形成过程:
(4)由A、E、F三种元素形成的化合物的化学式为
(5)B的最高价是
2020高三·全国·专题练习 查看更多[1]
(已下线)第5章 原子结构 元素周期律 单元测试(测)——2020年高考化学一轮复习讲练测
更新时间:2020-05-28 15:04:15
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】填空。
(1)工业上采用向饱和食盐水中先后通入NH3和CO2的方式制取重要的化工原料纯碱。CO2的电子式是_______ ,分子中的键角为_______ ;NH3的结构式是_______ ,其分子构型为_______ 。两者中属于非极性分子的是_______ ,其所含化学键为_______ (填“极性”或“非极性”)键。
(2)氢化锂(LiH)是_______ (填“离子”或“共价”)化合物,写出其电子式_______ ,其构成微粒的半径大小关系为_______ (用微粒符号表示)。与同类型的NaH相比,_______ 的熔点高,理由是_______ 。
(3)实验数据表明,氯化铝在2.02×105Pa时熔点为190℃,且在180℃时开始升华。
①推测氯化铝是_______ (填“离子”或“共价”)化合物,导电性实验发现熔化的氯化铝不导电,氯化铝属于_______ (填“电解质”、“非电解质”或“既不是电解质也不是非电解质”)。
②实验测得氯化铝蒸气的密度折算成标准状况下为11.92g·L-1,则氯化铝的化学式为_______ 。
(1)工业上采用向饱和食盐水中先后通入NH3和CO2的方式制取重要的化工原料纯碱。CO2的电子式是
(2)氢化锂(LiH)是
(3)实验数据表明,氯化铝在2.02×105Pa时熔点为190℃,且在180℃时开始升华。
①推测氯化铝是
②实验测得氯化铝蒸气的密度折算成标准状况下为11.92g·L-1,则氯化铝的化学式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】钼酸钠晶体( )可用于制造生物碱、油墨、化肥、钼红颜料等,也可用于制造阻燃剂和无公害型冷却水系统的金属缓蚀剂。如图所示是利用钼精矿(主要成分为
)可用于制造生物碱、油墨、化肥、钼红颜料等,也可用于制造阻燃剂和无公害型冷却水系统的金属缓蚀剂。如图所示是利用钼精矿(主要成分为 ,含少量PbS等)为原料生产钼酸钠晶体的工艺流程图。
,含少量PbS等)为原料生产钼酸钠晶体的工艺流程图。

请回答下列问题:
(1) 中Mo的化合价为
中Mo的化合价为___________
(2)“焙烧”时,有 生成,反应的化学方程式为
生成,反应的化学方程式为___________ ,氧化产物是___________
(3)“碱浸”生成 和另外一种物质,
和另外一种物质, 的电子式为
的电子式为___________ ,另外一种生成物的化学式为___________
(4)若“除重金属离子”时加入的沉淀剂为 ,则废渣的成分为
,则废渣的成分为___________  填化学式
填化学式
(5)测得“除重金属离子”中部分离子的浓度: “结晶”前应先除去
“结晶”前应先除去 ,方法是加入
,方法是加入 固体。假设加入
固体。假设加入 固体后溶液体积不变,当
固体后溶液体积不变,当 开始沉淀时,去除的
开始沉淀时,去除的 的质量分数为
的质量分数为___________  已知
已知
 )可用于制造生物碱、油墨、化肥、钼红颜料等,也可用于制造阻燃剂和无公害型冷却水系统的金属缓蚀剂。如图所示是利用钼精矿(主要成分为
)可用于制造生物碱、油墨、化肥、钼红颜料等,也可用于制造阻燃剂和无公害型冷却水系统的金属缓蚀剂。如图所示是利用钼精矿(主要成分为 ,含少量PbS等)为原料生产钼酸钠晶体的工艺流程图。
,含少量PbS等)为原料生产钼酸钠晶体的工艺流程图。
请回答下列问题:
(1)
 中Mo的化合价为
中Mo的化合价为(2)“焙烧”时,有
 生成,反应的化学方程式为
生成,反应的化学方程式为(3)“碱浸”生成
 和另外一种物质,
和另外一种物质, 的电子式为
的电子式为(4)若“除重金属离子”时加入的沉淀剂为
 ,则废渣的成分为
,则废渣的成分为 填化学式
填化学式
(5)测得“除重金属离子”中部分离子的浓度:
 “结晶”前应先除去
“结晶”前应先除去 ,方法是加入
,方法是加入 固体。假设加入
固体。假设加入 固体后溶液体积不变,当
固体后溶液体积不变,当 开始沉淀时,去除的
开始沉淀时,去除的 的质量分数为
的质量分数为 已知
已知
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】现有M、Q、R、T、W、X、Y、Z八种前四周期常见元素,原子序数依次递增。其中,M具有一种没有中子的同位素;Q是植物生长三要素之一;R是地壳中含量最多的元素,且W与R的最外层电子数相同;T、Y、Z是金属元素,其中T的原子半径是短周期中最大的,能与X形成离子化合物TX;Y既不是主族元素、也不是副族元素,其合金被称为“黑色金属”;Z的单质在空气中被锈蚀后会生成翠绿色的化合物。请回答下列问题:
(1)Y在周期表中的位置___________ ;
(2)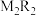 的电子式为
的电子式为___________ ;M、Q能形成一种阳离子,该阳离子能与W的简单离子能形成一种2:1的离子化合物,请写出该化合物的电子式___________ 。
(3)非金属性X___________ W(填“>”“=”或“<”),请用化学方程式说明该事实___________ ;
(4)写出Z的单质在浓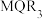 溶液中反应的离子方程式
溶液中反应的离子方程式___________ ,若Z的单质过量,则产物气体的成分可能是___________ 。
(1)Y在周期表中的位置
(2)
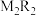 的电子式为
的电子式为(3)非金属性X
(4)写出Z的单质在浓
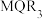 溶液中反应的离子方程式
溶液中反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】部分元素的原子结构特点如下表:
(1)画出W简单离子的结构示意图:_________ 。
(2)Z在元素周期表中的位置是___________ 。
(3)元素X与元素Z相比,非金属性较强的是_______ (填元素名称),写出一个能表示X、Z非金属性强弱关系的化学方程式:__________ 。
(4)元素X和元素Y以原子个数比1:1形成化合物Q,Q的化学式为___ ,Q中含有的化学键为___ 。
| X | L层电子数是K层电子数的3倍 |
| Y | 核外电子层数等于原子序数 |
| Z | Z原子K层、L层、M层电子数分别为a、b、3/4b |
| W | W元素的单质是空气中含量最高的气体 |
(2)Z在元素周期表中的位置是
(3)元素X与元素Z相比,非金属性较强的是
(4)元素X和元素Y以原子个数比1:1形成化合物Q,Q的化学式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】A、B、C、D、E是核电荷数依次增大的五种短周期主族元素,A元素的原子核内只有1个质子;B元素的原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3;C元素原子的最外层电子数比次外层多4;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C;C、E同主族。
(1)B在周期表中的位置为第____ 周期第___ 族。
(2)E元素形成的氧化物对应的水化物的化学式为______ 。
(3)元素B、C、D、E形成的简单离子半径大小关系是___________ (用离子符号表示)。
(4)用电子式表示化合物D2C的形成过程:__________________________ 。
(5)由A、B、C三种元素形成的离子化合物的化学式为______ ,它与强碱溶液共热,发生反应的离子方程式是_________________ 。
(6)D2EC3一定条件下可以发生分解反应生成两种盐,其中一种产物为无氧酸盐,则此反应的化学方程式为____________ (化学式用具体的元素符号表示)。
(1)B在周期表中的位置为第
(2)E元素形成的氧化物对应的水化物的化学式为
(3)元素B、C、D、E形成的简单离子半径大小关系是
(4)用电子式表示化合物D2C的形成过程:
(5)由A、B、C三种元素形成的离子化合物的化学式为
(6)D2EC3一定条件下可以发生分解反应生成两种盐,其中一种产物为无氧酸盐,则此反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】Ⅰ.有4种化合物W(通常状况下是气态)、X(通常状况下是液态)、Y、Z(通常状况下是固态),它们共由5种短周期元素A、B、C、D、E组成。已知:①原子序数A<B<C<D<E,且A与D同族;C与E同族;B与C同周期。②W由A和B组成,且W分子中,A与B的原子个数比为4∶1;X由A和C组成,且X分子中A与C的原子个数比为1∶1;Y由C和D组成,属离子化合物,且测得Y固体中C与D的原子个数比为1∶1。③Z由D和E组成,属离子化合物,且其阳离子比阴离子少1个电子层,阳离子数与阴离子数之比为2∶1。试推断写出:
(1)W的化学式是________ ,W属于________ 化合物。
(2)X的电子式是________ ,X属于________ 化合物。
(3)1 mol Y在干燥的空气中质量会______ (填“增大”或“减小”),其变化量(Δm)为________ 。
(4)用电子式表示化合物Z的形成过程________ 。
Ⅱ.已知Si-Cl键、H-H键、H-Cl键、Si-Si键的键能分别为a kJ·mol-1、b kJ·mol-1、c kJ·mol-1、d kJ·mol-1,1 mol硅晶体含2 mol Si-Si键。
(5)工业上,提纯硅的化学方程式是SiCl4(g)+2H2(g)=Si(s)+4HCl(g) 则该反应的反应热是_______________ 。
(1)W的化学式是
(2)X的电子式是
(3)1 mol Y在干燥的空气中质量会
(4)用电子式表示化合物Z的形成过程
Ⅱ.已知Si-Cl键、H-H键、H-Cl键、Si-Si键的键能分别为a kJ·mol-1、b kJ·mol-1、c kJ·mol-1、d kJ·mol-1,1 mol硅晶体含2 mol Si-Si键。
(5)工业上,提纯硅的化学方程式是SiCl4(g)+2H2(g)=Si(s)+4HCl(g) 则该反应的反应热是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】短周期主族元素X、Y、Z、W原子序数依次增大,X的单质是空气中含量最高的气体,Y的焰色反应现象为黄色。Z为金属元素,由Z制得的容器常温下可盛装浓硫酸。W原子最外层比X原子最外层多2个电子。
(1)X在元素周期表中的位置为___________ ,X单质的结构式为___________ 。
(2)W的简单气态氢化物电子式是___________ ,该气态氢化物溶于水时,破坏的化学键是___________ 。
(3)Y、Z、W的原子半径从大到小的顺序是___________ (用元素符号表示)。Y的最高价氧化物的水化物和Z的最高价氧化物的水化物反应的离子方程式是___________ 。
(1)X在元素周期表中的位置为
(2)W的简单气态氢化物电子式是
(3)Y、Z、W的原子半径从大到小的顺序是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】A、B、C、D、E、F为短周期元素.A的焰色反应为黄色,B的氢氧化物具有两性,C的原子最外层电子数是次外层电子数的2倍.D的原子最外层电子数是次外层电子数的3倍.E与D同主族,F的单质是黄绿色气体。
(1)B、F的元素符号分别为______ 、____ ;
(2)A、E两种元素按原子半径由大到小的顺序为______ (用元素符号填写);
(3)D元素氢化物的化学式为______ ;
(4)C的氧化物中能产生温室效应的是__________ (填化学式)。
(1)B、F的元素符号分别为
(2)A、E两种元素按原子半径由大到小的顺序为
(3)D元素氢化物的化学式为
(4)C的氧化物中能产生温室效应的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】A、B、C、D、E是原子序数依次增大的五种短周期元素。A原子的电子层数与它的核外电子总数相同,A与C、B与D分别为同主族,B和C的最外层电子数之和与E的最外层电子数相同,A与E形成的化合物化学式为AE,其分子中含18个电子。请回答下列问题:
(1)B元素 在周期表中的位置___________ ,写出E最高价氧化物对应水化物的化学式___________ 。
(2)由B、C两种元素形成的含共价键的化合物的电子式为___________ ,写出其与CO2反应的化学方程式并用双线桥标出电子转移的方向和数目___________
(3)写出E单质与A、B、C三种元素形成的化合物反应的离子方程式___________ 。
(4)A、B、C、D、E常见离子半径由大到小的顺序为___________ (用离子符号表示)。
(1)B元素 在周期表中的位置
(2)由B、C两种元素形成的含共价键的化合物的电子式为
(3)写出E单质与A、B、C三种元素形成的化合物反应的离子方程式
(4)A、B、C、D、E常见离子半径由大到小的顺序为
您最近一年使用:0次



