Ⅰ.有4种化合物W(通常状况下是气态)、X(通常状况下是液态)、Y、Z(通常状况下是固态),它们共由5种短周期元素A、B、C、D、E组成。已知:①原子序数A<B<C<D<E,且A与D同族;C与E同族;B与C同周期。②W由A和B组成,且W分子中,A与B的原子个数比为4∶1;X由A和C组成,且X分子中A与C的原子个数比为1∶1;Y由C和D组成,属离子化合物,且测得Y固体中C与D的原子个数比为1∶1。③Z由D和E组成,属离子化合物,且其阳离子比阴离子少1个电子层,阳离子数与阴离子数之比为2∶1。试推断写出:
(1)W的化学式是________ ,W属于________ 化合物。
(2)X的电子式是________ ,X属于________ 化合物。
(3)1 mol Y在干燥的空气中质量会______ (填“增大”或“减小”),其变化量(Δm)为________ 。
(4)用电子式表示化合物Z的形成过程________ 。
Ⅱ.已知Si-Cl键、H-H键、H-Cl键、Si-Si键的键能分别为a kJ·mol-1、b kJ·mol-1、c kJ·mol-1、d kJ·mol-1,1 mol硅晶体含2 mol Si-Si键。
(5)工业上,提纯硅的化学方程式是SiCl4(g)+2H2(g)=Si(s)+4HCl(g) 则该反应的反应热是_______________ 。
(1)W的化学式是
(2)X的电子式是
(3)1 mol Y在干燥的空气中质量会
(4)用电子式表示化合物Z的形成过程
Ⅱ.已知Si-Cl键、H-H键、H-Cl键、Si-Si键的键能分别为a kJ·mol-1、b kJ·mol-1、c kJ·mol-1、d kJ·mol-1,1 mol硅晶体含2 mol Si-Si键。
(5)工业上,提纯硅的化学方程式是SiCl4(g)+2H2(g)=Si(s)+4HCl(g) 则该反应的反应热是
更新时间:2018-04-09 21:14:22
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】下表是元素周期表的一部分,针对编号①~⑫元素,回答下列有关问题:
(1)在这些元素中,非金属性最强的元素是_______ (填元素符号,下同),最不活泼的元素是_______ 。
(2)写出元素①对应气态氢化物的化学式和电子式:_______ 、_______ 。
(3)在元素③和④中,单质与水反应较剧烈的是_______ (填元素符号),它与水反应的化学方程式是_______ 。
(4)在元素③、④与⑤的最高价氧化物对应的水化物中,碱性最弱是_______ (填化学式)。
(5)能证明⑧和⑫单质氧化性强弱的实验事实 用离子方程式表示)是
用离子方程式表示)是_______ 。
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA |  |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 四 | ⑩ | ⑪ | ⑫ |
(2)写出元素①对应气态氢化物的化学式和电子式:
(3)在元素③和④中,单质与水反应较剧烈的是
(4)在元素③、④与⑤的最高价氧化物对应的水化物中,碱性最弱是
(5)能证明⑧和⑫单质氧化性强弱的实验事实
 用离子方程式表示)是
用离子方程式表示)是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】下表为元素周期表的一部分,请参照元素①~⑥在表中的位置,用化学用语 回答下列问题。

(1)元素①的原子结构示意图为_______ 。
(2)元素③和⑥可形成化合物,用电子式表示形成其过程_______ 。
(3)元素②、③形成简单离子的半径(填离子符号)_______ >_______ 。
(4)元素②、⑥形成的气态氢化物稳定性(填化学式,下同)_______ >_______ ;元素③、④形成的最高价氧化物水化物的碱性_______ >_______ 。
(5)元素④的最高价氧化物与元素⑤最高价氧化物的水化物稀溶液反应的离子方程式_______ 。
(6)元素①的最高价氧化物的水化物与元素③最高价氧化物的水化物稀溶液反应的离子方程式_______

(1)元素①的原子结构示意图为
(2)元素③和⑥可形成化合物,用电子式表示形成其过程
(3)元素②、③形成简单离子的半径(填离子符号)
(4)元素②、⑥形成的气态氢化物稳定性(填化学式,下同)
(5)元素④的最高价氧化物与元素⑤最高价氧化物的水化物稀溶液反应的离子方程式
(6)元素①的最高价氧化物的水化物与元素③最高价氧化物的水化物稀溶液反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】该表是元素周期表中的一部分:
回答下列问题:
(1)⑦是____________ ,原子半径最大的是____________ 。(填元素符号或化学式,下同)
(2)⑧⑨⑪⑫四种元素形成的简单离子,半径由大到小的顺序是________ 。
(3)上述元素中,最高价氧化物的水化物中,酸性最强的化合物的分子式是____________ ,碱性最强的化合物的电子式____________ 。
(4)用电子式表示⑤和⑨组成的化合物的形成过程____________ 。
(5)①和氢元素形成的化合物很多,其中C2H6可用于形成燃料电池,若用NaOH作电解质溶液,写出该燃料电池的负极反应方程式____________ 。
(6)CO2与CH4经催化重整制得合成气:CH4(g)+CO2(g)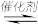 2CO(g)+2H2(g)。已知上述反应中相关的化学键键能数据如表:
2CO(g)+2H2(g)。已知上述反应中相关的化学键键能数据如表:
则该反应产生2molH2(g)时____________ (填“放出”或“吸收”)热量为____________ kJ。
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | |
| 4 | ⑪ | ⑫ | ⑬ |
(1)⑦是
(2)⑧⑨⑪⑫四种元素形成的简单离子,半径由大到小的顺序是
(3)上述元素中,最高价氧化物的水化物中,酸性最强的化合物的分子式是
(4)用电子式表示⑤和⑨组成的化合物的形成过程
(5)①和氢元素形成的化合物很多,其中C2H6可用于形成燃料电池,若用NaOH作电解质溶液,写出该燃料电池的负极反应方程式
(6)CO2与CH4经催化重整制得合成气:CH4(g)+CO2(g)
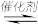 2CO(g)+2H2(g)。已知上述反应中相关的化学键键能数据如表:
2CO(g)+2H2(g)。已知上述反应中相关的化学键键能数据如表:| 化学键 | C-H | C=O | H-H | C O(CO) O(CO) |
| 键能/kJ·mol−1 | 413 | 745 | 436 | 1075 |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】Ⅰ、化学实验中,通常需要使用到硫酸
(1)向Na2S2O3溶液滴加稀硫酸,产生淡黄色沉淀,写出反应的离子方程式_____ 。
(2)向硫酸酸化的KMnO4溶液中滴加草酸溶液,紫红色褪去。写出反应的化学方程式_____ 。
Ⅱ、氢气作为一种清洁能源,一直是能源研究的热点,工业上制取氢气有多种方法:
①C(s)+H2O(g)=CO(g)+H2(g) △H1=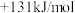
②CH4(g)+CO2(g)=2CO(g)+2H2(g) △H2=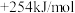
③CH4(g)+H2O(g)=CO(g)+3H2(g) △H3=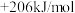
④CH3OH(1)=CO(g)+2H2(g) △H4=
(3)根据以上数据,请写出CH4(g)分解生成C(s)和H2(g)的热化学方程式_____ 。反应②需要在_____ (高温、低温)下才能自发进行
(4)几种化学键的键能如下表所示:
根据以上有关反应的△H,计算x=_____ 。
(5)我国科学家通过计算机模拟,研究了在某催化剂表面上发生反应④的反应历程(吸附在催化剂表面的物质,用"*"标注)。甲醇(CH3OH)脱氢反应的第一步历程,有两种可能方式:
方式Ⅰ: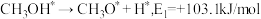
方式Ⅱ:
活化能E值推测,甲醇脱氢过程中主要历程的方式为_____ (填"Ⅰ"或"Ⅱ")。计算机模拟的各步反应的能量变化示意图如下。

写出该历程中有最大能垒(活化能)的基元反应的化学方程式_____ 。
(1)向Na2S2O3溶液滴加稀硫酸,产生淡黄色沉淀,写出反应的离子方程式
(2)向硫酸酸化的KMnO4溶液中滴加草酸溶液,紫红色褪去。写出反应的化学方程式
Ⅱ、氢气作为一种清洁能源,一直是能源研究的热点,工业上制取氢气有多种方法:
①C(s)+H2O(g)=CO(g)+H2(g) △H1=
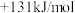
②CH4(g)+CO2(g)=2CO(g)+2H2(g) △H2=
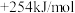
③CH4(g)+H2O(g)=CO(g)+3H2(g) △H3=
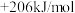
④CH3OH(1)=CO(g)+2H2(g) △H4=

(3)根据以上数据,请写出CH4(g)分解生成C(s)和H2(g)的热化学方程式
(4)几种化学键的键能如下表所示:
| 化学键 | C=O | H—H | 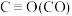 | C—H | O—H |
| 键能/kJ·mol-1 | 803 | 436 | x | 414 | 463 |
(5)我国科学家通过计算机模拟,研究了在某催化剂表面上发生反应④的反应历程(吸附在催化剂表面的物质,用"*"标注)。甲醇(CH3OH)脱氢反应的第一步历程,有两种可能方式:
方式Ⅰ:
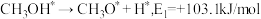
方式Ⅱ:

活化能E值推测,甲醇脱氢过程中主要历程的方式为

写出该历程中有最大能垒(活化能)的基元反应的化学方程式
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】 是一种廉价的碳资源,其综合利用具有重要意义。回答下列问题:
是一种廉价的碳资源,其综合利用具有重要意义。回答下列问题:
(1) 可以被
可以被 溶液捕获。若所得溶液
溶液捕获。若所得溶液 ,
, 主要转化为
主要转化为_______ (写离子符号);若所得溶液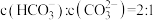 ,溶液
,溶液
_______ 。(室温下, 的
的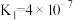 ;
;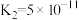 )
)
(2) 与
与 经催化重整,制得合成气:
经催化重整,制得合成气:
①已知上述反应中相关的化学键键能数据如表:
则该反应的
_______ 。
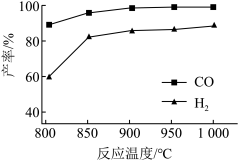
②按一定体积比加入 和
和 ,在恒压下发生反应,温度对
,在恒压下发生反应,温度对 和
和 产率的影响如图所示。此反应优选温度为900℃的原因是
产率的影响如图所示。此反应优选温度为900℃的原因是_______ 。
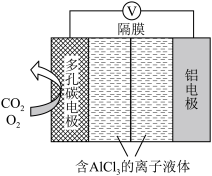
(3) 辅助的
辅助的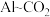 电池工作原理如图所示。该电池电容量大,能有效利用
电池工作原理如图所示。该电池电容量大,能有效利用 ,电池反应产物
,电池反应产物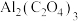 是重要的化工原料。电池的负极反应式:
是重要的化工原料。电池的负极反应式:_______ 。
 是一种廉价的碳资源,其综合利用具有重要意义。回答下列问题:
是一种廉价的碳资源,其综合利用具有重要意义。回答下列问题:(1)
 可以被
可以被 溶液捕获。若所得溶液
溶液捕获。若所得溶液 ,
, 主要转化为
主要转化为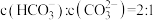 ,溶液
,溶液
 的
的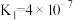 ;
;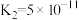 )
)(2)
 与
与 经催化重整,制得合成气:
经催化重整,制得合成气:
①已知上述反应中相关的化学键键能数据如表:
| 化学键 |  |  |  | 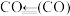 |
键能/ | 413 | 745 | 436 | 1075 |

②按一定体积比加入
 和
和 ,在恒压下发生反应,温度对
,在恒压下发生反应,温度对 和
和 产率的影响如图所示。此反应优选温度为900℃的原因是
产率的影响如图所示。此反应优选温度为900℃的原因是
(3)
 辅助的
辅助的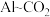 电池工作原理如图所示。该电池电容量大,能有效利用
电池工作原理如图所示。该电池电容量大,能有效利用 ,电池反应产物
,电池反应产物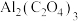 是重要的化工原料。电池的负极反应式:
是重要的化工原料。电池的负极反应式:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】回答下列问题:
(1)研究表明 和
和 在催化剂存在下可发生反应生成
在催化剂存在下可发生反应生成 。已知部分反应的热化学方程式如下:
。已知部分反应的热化学方程式如下:
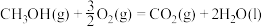

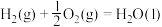


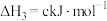
则

___________  。
。
(2)已知热化学方程式:
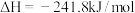 ,该反应的活化能为167.2kJ/mol,则其逆反应的活化能为
,该反应的活化能为167.2kJ/mol,则其逆反应的活化能为___________  。
。
(3)如图是中和热的测定实验装置。
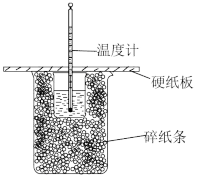
①从实验装置图看,图中尚缺少的一种玻璃用品是___________ 。
②该实验常用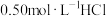 和
和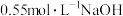 溶液各50mL。解释NaOH溶液的浓度稍大的原因
溶液各50mL。解释NaOH溶液的浓度稍大的原因___________ 。
(4)偏二甲肼是一种高比冲液体燃料,其燃烧值是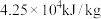 ,我国发射宇宙飞船的“神舟“系列火箭用偏二甲肼
,我国发射宇宙飞船的“神舟“系列火箭用偏二甲肼 作燃料,液态四氧化二氮作氧化剂,生成氮气和二氧化碳气体及水蒸气。写出反应的热化学反应方程式:
作燃料,液态四氧化二氮作氧化剂,生成氮气和二氧化碳气体及水蒸气。写出反应的热化学反应方程式:___________ 。
(1)研究表明
 和
和 在催化剂存在下可发生反应生成
在催化剂存在下可发生反应生成 。已知部分反应的热化学方程式如下:
。已知部分反应的热化学方程式如下: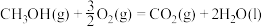

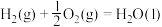


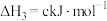
则


 。
。(2)已知热化学方程式:

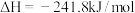 ,该反应的活化能为167.2kJ/mol,则其逆反应的活化能为
,该反应的活化能为167.2kJ/mol,则其逆反应的活化能为 。
。(3)如图是中和热的测定实验装置。

①从实验装置图看,图中尚缺少的一种玻璃用品是
②该实验常用
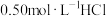 和
和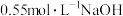 溶液各50mL。解释NaOH溶液的浓度稍大的原因
溶液各50mL。解释NaOH溶液的浓度稍大的原因(4)偏二甲肼是一种高比冲液体燃料,其燃烧值是
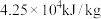 ,我国发射宇宙飞船的“神舟“系列火箭用偏二甲肼
,我国发射宇宙飞船的“神舟“系列火箭用偏二甲肼 作燃料,液态四氧化二氮作氧化剂,生成氮气和二氧化碳气体及水蒸气。写出反应的热化学反应方程式:
作燃料,液态四氧化二氮作氧化剂,生成氮气和二氧化碳气体及水蒸气。写出反应的热化学反应方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】现有表格中短周期元素的数据(已知Be的原子半径为0.089nm),回答下列问题(用对应的元素符号或化学式表示):
(1)写出下列元素符号②___________ ⑤___________ 。
(2)比较①、④、⑧形成的简单离子半径大小:___________ 。
(3)比较元素①和④金属性强弱:___________ ,判断依据是___________ 。
(4)碲(Te)的某化合物是常用的VCR光盘记录材料之一,可在激光照射下发生化学或物理的性能改变而记录、储存信号。上述元素中,和碲元素处于同一主族的元素是___________ ;推测碲元素及其化合物可能具有的性质为:___________ (不定项选择)。
A.单质碲在常温下是固体
B.Cl2通入H2Te溶液中不发生反应
C.Te很容易与H2化合生成H2Te
D.H2TeO4的酸性比H2SO4的弱
E.沸点:H2Te>H2S>H2O
| 元素代号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| 原子半径(nm) | 0.186 | 0.160 | 0.152 | 0.143 | 0.110 | 0.099 | 0.075 | 0.074 |
| 主要化合价 | +1 | +2 | +1 | +3 | +5、-3 | +7、-1 | +5、-3 | -2 |
(2)比较①、④、⑧形成的简单离子半径大小:
(3)比较元素①和④金属性强弱:
(4)碲(Te)的某化合物是常用的VCR光盘记录材料之一,可在激光照射下发生化学或物理的性能改变而记录、储存信号。上述元素中,和碲元素处于同一主族的元素是
A.单质碲在常温下是固体
B.Cl2通入H2Te溶液中不发生反应
C.Te很容易与H2化合生成H2Te
D.H2TeO4的酸性比H2SO4的弱
E.沸点:H2Te>H2S>H2O
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】已知X、Y、Z、W四种元素分别是元素周期表中三个连续短周期的元素,且原子序数依次增大。X、W同主族,Y、Z为同周期的相邻元素。W原子的质子数等于Y、Z原子的最外层电子数之和。Y与X形成的分子中有3个共价键。 原子的最外层电子数是次外层电子数的3倍,试推断:
原子的最外层电子数是次外层电子数的3倍,试推断:
(1)X、Z两种元素的元素符号: X__________ 、Z__________ 。
(2)由以上元素中两两形成的化合物中,溶于水显碱性的气态氢化物的电子式为__________ ;含有离子键和非极性共价键的化合物的电子式为__________ ;含有极性共价键和非极性共价键的化合物的电子式为_______ 。
(3)由X、Y、Z所形成的常见离子化合物是__________ (写化学式),该化合物与W的最高价氧化物对应的水化物的浓溶液加热时反应的离子方程式为__________ 。
 原子的最外层电子数是次外层电子数的3倍,试推断:
原子的最外层电子数是次外层电子数的3倍,试推断:(1)X、Z两种元素的元素符号: X
(2)由以上元素中两两形成的化合物中,溶于水显碱性的气态氢化物的电子式为
(3)由X、Y、Z所形成的常见离子化合物是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】A、B、C、D、E为短周期主族元素,且原子序数依次增大,质子数之和为39,B、C同周期,A、D同主族,A为短周期原子半径最小的元素,C原子最外层电子数为次外层的3倍,A、C常温下能形成两种液态化合物A2C和A2C2,E元素的周期数与主族序数相等。请用化学用语回答下列问题:
(1)C元素在周期表中的位置为________ ;由 A、C、D 三种元素组成的化合物中含有的化学键为___________ 。
(2)写出A2C的电子式_____ ,A2C2的结构式________ 。
(3)废印刷电路板上含有铜,以往的回收方法是将其灼烧使铜转化为氧化铜,再用硫酸溶解。现改用A2C2和稀硫酸浸泡废印刷电路板既达到上述目的,又保护了环境,试写出反应的离子方程式:_____________ 。
(4)元素D的单质在一定条件下,能与A 单质化合生成一种化合物DA,其电子式为________ ,DA能与水反应放出氢气,若将 0.1 molDA和 0.1 mol E 单质混合加入足量的水,充分反应后生成的气体在标准状况下的体积是______ L。
(1)C元素在周期表中的位置为
(2)写出A2C的电子式
(3)废印刷电路板上含有铜,以往的回收方法是将其灼烧使铜转化为氧化铜,再用硫酸溶解。现改用A2C2和稀硫酸浸泡废印刷电路板既达到上述目的,又保护了环境,试写出反应的离子方程式:
(4)元素D的单质在一定条件下,能与A 单质化合生成一种化合物DA,其电子式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】下图为相关物质之间的转化关系,其中甲、乙为生活中常见的金属单质,丙、丁在常温下为气态非金属单质,A~F为化合物(水均已略去)。
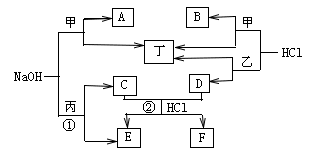
请回答:
(1)组成丙的元一素在元素周期表中的位置为____________ ;利用反应① ,工业上常制备__________ (填产品名称)。
(2)C的电子式为________________ ;反应②的离子方程式为________________ 。
(3)将A、B的水溶液混合,反应的离子方程式为________________ 。
(4)将B 的稀溶液加水稀释,在下图中画出溶液pH 随加水体积的变化曲线____ .
(5)工业上冶炼金属甲的化学方程式为________________ 。
(6)将等物质的量的A和NaOH混合溶于水,该溶液中各离子的物质的量浓度由大到小的顺序为________________ 。
(7)检验F中阳离子的方法为________________ 。

请回答:
(1)组成丙的元一素在元素周期表中的位置为
(2)C的电子式为
(3)将A、B的水溶液混合,反应的离子方程式为
(4)将B 的稀溶液加水稀释,在下图中画出溶液pH 随加水体积的变化曲线

(5)工业上冶炼金属甲的化学方程式为
(6)将等物质的量的A和NaOH混合溶于水,该溶液中各离子的物质的量浓度由大到小的顺序为
(7)检验F中阳离子的方法为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】结合元素周期表,完成下列问题。
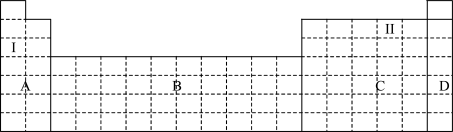
(1)在元素周期表中全部是金属元素的区域为____________ (填序号)。
a.A b.B c.C d.D
(2)Ⅰ和Ⅱ元素形成的化合物的化学式为__________________ ,写出其中含有非极性共价键的化合物的电子式_______________ 。
(3)现有甲、乙两种短周期元素,室温下,甲元素的单质在冷的浓硫酸或空气中表面都会生成致密的氧化膜,乙元素原子核外第三层与第一层上的电子数相等。
①写出甲元素周期表中对应的位置__________ 。
②甲、乙两元素中,金属性较强的是__________ (填元素名称),可以验证该结论的实验是_______________ (填序号)。
a.将在空气中放置已久的这两种元素的单质分别放入热水中
b.将这两种元素的单质粉末分别和相同浓度的盐酸反应
c.将这两种元素的单质粉末分别和热水作用,并滴入酚酞溶液
d.比较这两种元素的气态氢化物的稳定性

(1)在元素周期表中全部是金属元素的区域为
a.A b.B c.C d.D
(2)Ⅰ和Ⅱ元素形成的化合物的化学式为
(3)现有甲、乙两种短周期元素,室温下,甲元素的单质在冷的浓硫酸或空气中表面都会生成致密的氧化膜,乙元素原子核外第三层与第一层上的电子数相等。
①写出甲元素周期表中对应的位置
②甲、乙两元素中,金属性较强的是
a.将在空气中放置已久的这两种元素的单质分别放入热水中
b.将这两种元素的单质粉末分别和相同浓度的盐酸反应
c.将这两种元素的单质粉末分别和热水作用,并滴入酚酞溶液
d.比较这两种元素的气态氢化物的稳定性
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】已知A、B、C、D、E是原子序数依次增大的短周期元素。其中A的原子半径在短周期中最小;B的最外层电子数是内层电子总数的2倍;A与C形成的最简单化合物X在常温下是一种气体,其水溶液呈碱性;D常见有D2和D3两种不同形态的同素异形体;E单质常温下在浓硫酸中会钝化。请回答:(答题时,A、B、C、D、E用对应元素符号表示)
(1)A在元素周期表中的位置为________ 。
(2)写出化合物BD2的电子式:________ ,它是由________ (填“极性共价键”或“非极性共价键”)形成的非极性分子。
(3) 化合物X的结构式为________ ;E的原子结构示意图为________ 。
(4) D与E形成的化合物溶于氢氧化钠溶液的离子方程式为______________________ 。
(1)A在元素周期表中的位置为
(2)写出化合物BD2的电子式:
(3) 化合物X的结构式为
(4) D与E形成的化合物溶于氢氧化钠溶液的离子方程式为
您最近一年使用:0次



