 是一种廉价的碳资源,其综合利用具有重要意义。回答下列问题:
是一种廉价的碳资源,其综合利用具有重要意义。回答下列问题:(1)
 可以被
可以被 溶液捕获。若所得溶液
溶液捕获。若所得溶液 ,
, 主要转化为
主要转化为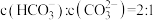 ,溶液
,溶液
 的
的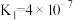 ;
;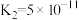 )
)(2)
 与
与 经催化重整,制得合成气:
经催化重整,制得合成气:
①已知上述反应中相关的化学键键能数据如表:
| 化学键 |  |  |  | 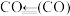 |
键能/ | 413 | 745 | 436 | 1075 |

②按一定体积比加入
 和
和 ,在恒压下发生反应,温度对
,在恒压下发生反应,温度对 和
和 产率的影响如图所示。此反应优选温度为900℃的原因是
产率的影响如图所示。此反应优选温度为900℃的原因是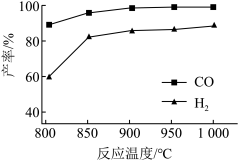
(3)
 辅助的
辅助的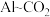 电池工作原理如图所示。该电池电容量大,能有效利用
电池工作原理如图所示。该电池电容量大,能有效利用 ,电池反应产物
,电池反应产物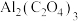 是重要的化工原料。电池的负极反应式:
是重要的化工原料。电池的负极反应式: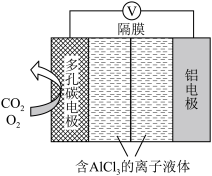
更新时间:2022-10-25 15:08:49
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】甲醇是重要的化工原料。利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,可能发生的反应如下:
①CO2(g)+3H2(g) CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
②CO2(g)+H2(g) CO(g)+H2O(g)
CO(g)+H2O(g)
③CH3OH(g) CO(g)+2H2(g)
CO(g)+2H2(g)
反应①为主反应(放热反应),②③为副反应。
回答下列问题:
(1)已知反应②中相关化学键键能数据如表:(注:C≡O表示CO中的化学键)
由此可知反应②是____ 反应。(填“放热”或“吸热”)
(2)一定比例的合成气在装有催化剂的反应器中反应12小时。体系中甲醇的产率和催化剂的催化活性与温度的关系如图1所示。
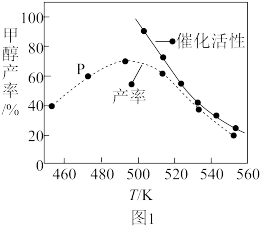
①温度为470K时,图中P点___ (填“是”或“不是”)处于平衡状态。490K之后,甲醇产率下降的原因是___ 。
②提高甲醇产率的措施是___ 。
A.增大压强 B.升高温度 C.选择合适催化剂 D.加入大量催化剂
(3)如图2为一定比例的CO2/H2,CO/H2、CO/CO2/H2条件下甲醇生成速率与温度的关系。当温度为490K时,根据曲线a、c,判断合成甲醇的反应机理是___ (填“A”或“B”)。

A:CO2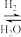 CO
CO CH3OH
CH3OH
B:CO CO2
CO2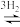 CH3OH+H2O
CH3OH+H2O
(4)490K时,曲线a与曲线b相比,CO的存在使甲醇生成速率增大,从平衡移动的角度分析原因___ 。
①CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)②CO2(g)+H2(g)
 CO(g)+H2O(g)
CO(g)+H2O(g)③CH3OH(g)
 CO(g)+2H2(g)
CO(g)+2H2(g)反应①为主反应(放热反应),②③为副反应。
回答下列问题:
(1)已知反应②中相关化学键键能数据如表:(注:C≡O表示CO中的化学键)
化学键 | H-H | C=O | C≡O | H-O |
E/(kJ∙mol-1) | 436 | 803 | 1076 | 465 |
(2)一定比例的合成气在装有催化剂的反应器中反应12小时。体系中甲醇的产率和催化剂的催化活性与温度的关系如图1所示。

①温度为470K时,图中P点
②提高甲醇产率的措施是
A.增大压强 B.升高温度 C.选择合适催化剂 D.加入大量催化剂
(3)如图2为一定比例的CO2/H2,CO/H2、CO/CO2/H2条件下甲醇生成速率与温度的关系。当温度为490K时,根据曲线a、c,判断合成甲醇的反应机理是

A:CO2
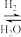 CO
CO CH3OH
CH3OHB:CO
 CO2
CO2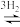 CH3OH+H2O
CH3OH+H2O(4)490K时,曲线a与曲线b相比,CO的存在使甲醇生成速率增大,从平衡移动的角度分析原因
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】氨气是中学化学中常见的气体,其用途广泛。
(1)工业上氨气可以由氢气和氮气合成。
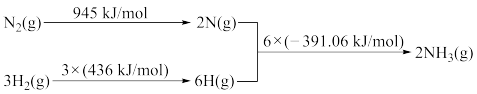
①该反应的热化学方程式是___ 。
②450℃,将5molN2和5molH2充入2L恒容密闭容器中发生反应,5min后达到平衡,N2的转化率为20%,则NH3的化学反应速率v(NH3)=___ ,该温度下如图所示反应的平衡常数的数值K=___ ,温度升高,平衡常数K将___ (填“增大”、“减小”或“不变”)。
(2)工业制硫酸的尾气中含较多的SO2,为防止污染空气,回收利用SO2,工业上常用氨水吸收法处理尾气。
①当氨水中所含氨的物质的量为3mol,吸收标准状况下44.8LSO2时,溶液中的溶质为___ 。
②已知NH4HSO3溶液显酸性。用氨水吸收SO2,当吸收液显中性时,溶液中离子浓度关系正确的是___ 。
A.c(NH4+)=2c(SO32-)+c(HSO3-)
B.c(NH4+)>c(SO32-)>c(H+)=c(OH-)
C.c(NH4+)+c(H+)=c(SO32-)+c(HSO3-)+c(OH-)
D.c(NH4+)+c(NH3·H2O)=c(SO32-)+c(HSO3-)+c(H2SO3)
(3)氨气是一种富氢燃料,可以直接用于燃料电池,如图是供氨水式燃料电池工作原理:
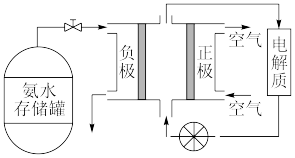
①氨气燃料电池的电解质溶液最好选择___ (填“酸性”、“碱性”或“中性”)溶液。
②氨气燃料电池的反应是氨气与氧气生成一种常见的无毒气体和水,该电池的总反应方程式为___ ,正极的电极反应式为___ 。
(1)工业上氨气可以由氢气和氮气合成。
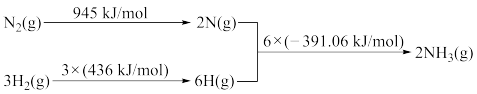
①该反应的热化学方程式是
②450℃,将5molN2和5molH2充入2L恒容密闭容器中发生反应,5min后达到平衡,N2的转化率为20%,则NH3的化学反应速率v(NH3)=
(2)工业制硫酸的尾气中含较多的SO2,为防止污染空气,回收利用SO2,工业上常用氨水吸收法处理尾气。
①当氨水中所含氨的物质的量为3mol,吸收标准状况下44.8LSO2时,溶液中的溶质为
②已知NH4HSO3溶液显酸性。用氨水吸收SO2,当吸收液显中性时,溶液中离子浓度关系正确的是
A.c(NH4+)=2c(SO32-)+c(HSO3-)
B.c(NH4+)>c(SO32-)>c(H+)=c(OH-)
C.c(NH4+)+c(H+)=c(SO32-)+c(HSO3-)+c(OH-)
D.c(NH4+)+c(NH3·H2O)=c(SO32-)+c(HSO3-)+c(H2SO3)
(3)氨气是一种富氢燃料,可以直接用于燃料电池,如图是供氨水式燃料电池工作原理:

①氨气燃料电池的电解质溶液最好选择
②氨气燃料电池的反应是氨气与氧气生成一种常见的无毒气体和水,该电池的总反应方程式为
您最近一年使用:0次
【推荐3】完成下列问题。
(1)已知:①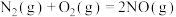
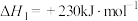
②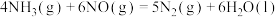
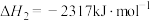
则表示氨气燃烧热的热化学方程式为___________ ,该反应可设计为碱性条件下的燃料电池,负极电极反应式为___________ 。
(2)已知几种化学键的键能和热化学方程式如下:

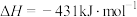 ,则
,则 =
=___________ 。
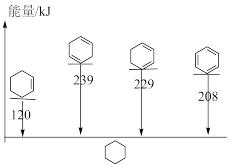
(3)4种不饱和烃分别与氢气发生加成反应生成1mol环己烷(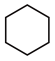 )的能量变化如图所示。根据图示计算反应
)的能量变化如图所示。根据图示计算反应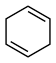 (l)=
(l)=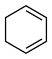 (l)的
(l)的 =
=___________ 。
(4)Fe和氨气在640℃可发生置换反应,产物之一的晶胞结构如图所示,写出该反应的化学方程式:___________ ,若两个最近的 原子间的距离为
原子间的距离为 ,则该晶体的密度是
,则该晶体的密度是___________  。
。

(1)已知:①
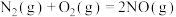
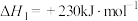
②
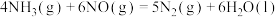
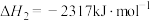
则表示氨气燃烧热的热化学方程式为
(2)已知几种化学键的键能和热化学方程式如下:
| 化学键 |  |  |  |  |  |
键能/( ) ) | 391 | 193 | 243 |  | 432 |

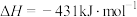 ,则
,则 =
=(3)4种不饱和烃分别与氢气发生加成反应生成1mol环己烷(
 )的能量变化如图所示。根据图示计算反应
)的能量变化如图所示。根据图示计算反应 (l)=
(l)= (l)的
(l)的 =
=
(4)Fe和氨气在640℃可发生置换反应,产物之一的晶胞结构如图所示,写出该反应的化学方程式:
 原子间的距离为
原子间的距离为 ,则该晶体的密度是
,则该晶体的密度是 。
。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】 是大气的主要污染物,工业上利用钠碱循环法可除去
是大气的主要污染物,工业上利用钠碱循环法可除去 。回答下列问题:
。回答下列问题:
(1)钠碱循环法中,吸收液为 溶液,其中各离子浓度由大到小的顺序为
溶液,其中各离子浓度由大到小的顺序为_______ 。
(2)可用 溶液吸收
溶液吸收 制备
制备 ,该反应的离子方程式是
,该反应的离子方程式是_______ 。
(3)已知 的电离常数为
的电离常数为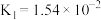 ,
,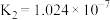 ;
; 的电离常数为
的电离常数为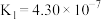 ,
,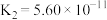 ,则下列各组微粒可以大量共存的是_______。(填字母)
,则下列各组微粒可以大量共存的是_______。(填字母)
(4)①写出 的水解常数表达式
的水解常数表达式_______ 。
②根据测定 溶液呈酸性,试用所学知识解释:
溶液呈酸性,试用所学知识解释:_______
则0.1mol/L 溶液中粒子浓度关系不正确的是
溶液中粒子浓度关系不正确的是_______ 。(填字母)
A.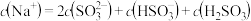
B.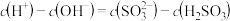
C.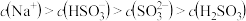
D.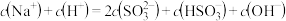
(5)当吸收液的pH降至约为6时,需送至电解槽再生回收液。再生示意图如下:
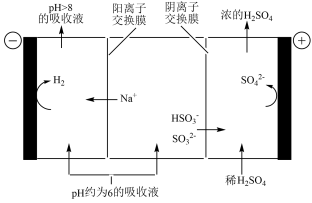
 在阳极放电的电极反应式是
在阳极放电的电极反应式是_______ 。
 是大气的主要污染物,工业上利用钠碱循环法可除去
是大气的主要污染物,工业上利用钠碱循环法可除去 。回答下列问题:
。回答下列问题:(1)钠碱循环法中,吸收液为
 溶液,其中各离子浓度由大到小的顺序为
溶液,其中各离子浓度由大到小的顺序为(2)可用
 溶液吸收
溶液吸收 制备
制备 ,该反应的离子方程式是
,该反应的离子方程式是(3)已知
 的电离常数为
的电离常数为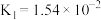 ,
,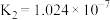 ;
; 的电离常数为
的电离常数为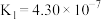 ,
,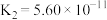 ,则下列各组微粒可以大量共存的是_______。(填字母)
,则下列各组微粒可以大量共存的是_______。(填字母)A. 和 和 | B. 和 和 | C. 和 和 | D. 和 和 |
 的水解常数表达式
的水解常数表达式②根据测定
 溶液呈酸性,试用所学知识解释:
溶液呈酸性,试用所学知识解释:则0.1mol/L
 溶液中粒子浓度关系不正确的是
溶液中粒子浓度关系不正确的是A.
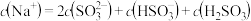
B.
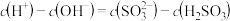
C.
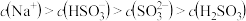
D.
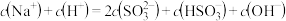
(5)当吸收液的pH降至约为6时,需送至电解槽再生回收液。再生示意图如下:

 在阳极放电的电极反应式是
在阳极放电的电极反应式是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】常温下向20.00 mL 0.10 mol/L Na2CO3溶液中逐滴加入0.10 mol/L盐酸40.00 mL,所得溶液的pH与加入盐酸体积的关系如表所示:
回答下列问题:
(1)20.00 mL 0.10 mol/L Na2CO3溶液中所有阳离子和阴离子的浓度有何关系?______ (用等式表示)。
(2)当V(HCl)=20.00 mL时,溶液呈碱性的原因是________ (用离子方程式和必要的文字说明)此时溶液中c(H2CO3)____ (填“>”、“<”或“=”)c(CO32—)。
(3)V(HCl)=40.00 mL时,得到H2CO3饱和溶液,且c(H2CO3)=4.0×10-5mol/L。若忽略水的电离及H2CO3的第二级电离,则H2CO3 HCO3—+H+的电离常数K1=
HCO3—+H+的电离常数K1=_____ 。此时保持其他条件不变,继续加入0.1 mol/L盐酸10.00 mL,K1将_____ (填“变大”、“变小”或“不变”)。
(4)若向20 mL 0.10 mol/L Na2CO3溶液中加入BaCl2粉末3.94×10-7 g时开始产生沉淀BaCO3,则Ksp(Ba2CO3)= 。
| 溶液的pH | 加入盐酸的总体积 |
| 12 | V(HCl)=0 |
| 8 | V(HCl)=20.00 mL |
| 5 | V(HCl)=40.00 mL |
回答下列问题:
(1)20.00 mL 0.10 mol/L Na2CO3溶液中所有阳离子和阴离子的浓度有何关系?
(2)当V(HCl)=20.00 mL时,溶液呈碱性的原因是
(3)V(HCl)=40.00 mL时,得到H2CO3饱和溶液,且c(H2CO3)=4.0×10-5mol/L。若忽略水的电离及H2CO3的第二级电离,则H2CO3
 HCO3—+H+的电离常数K1=
HCO3—+H+的电离常数K1=(4)若向20 mL 0.10 mol/L Na2CO3溶液中加入BaCl2粉末3.94×10-7 g时开始产生沉淀BaCO3,则Ksp(Ba2CO3)= 。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】一定条件下, 在某密闭容器中发生的反应有:
在某密闭容器中发生的反应有:
反应I.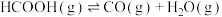


反应Ⅱ.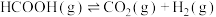

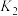
回答下列问题:
(1)对于反应

 ,
,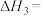
___________ (用含 、
、 的式子表示),
的式子表示),
___________ (用含 、
、 的式子表示)。
的式子表示)。
(2)常温下,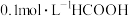 (甲酸)溶液中[已知:
(甲酸)溶液中[已知: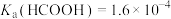 ]:
]:
①HCOOH的电离方程式为___________ 。
②该溶液中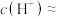
___________  。
。
③此温度下,若将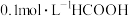 溶液加水稀释至
溶液加水稀释至 ,此时
,此时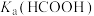
___________ (填“变大”、“变小”或“不变”,下同),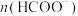
___________ 。
(3)某温度下,往某一恒容密闭容器中通入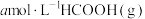 ,仅发生反应I和反应Ⅱ,
,仅发生反应I和反应Ⅱ, 后反应达到平衡,此时测得CO、HCOOH的浓度分别为
后反应达到平衡,此时测得CO、HCOOH的浓度分别为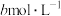 、
、 (不考虑碳元素的其他存在形式,
(不考虑碳元素的其他存在形式,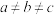 )。则
)。则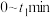 内
内
___________  (用含a、b、c的式子表示,下同),
(用含a、b、c的式子表示,下同), 的物质的量分数为
的物质的量分数为___________ ,反应Ⅱ的平衡常数为___________ 。
 在某密闭容器中发生的反应有:
在某密闭容器中发生的反应有:反应I.
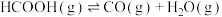


反应Ⅱ.
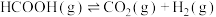

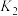
回答下列问题:
(1)对于反应


 ,
,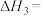
 、
、 的式子表示),
的式子表示),
 、
、 的式子表示)。
的式子表示)。(2)常温下,
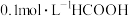 (甲酸)溶液中[已知:
(甲酸)溶液中[已知: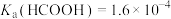 ]:
]:①HCOOH的电离方程式为
②该溶液中
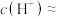
 。
。③此温度下,若将
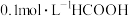 溶液加水稀释至
溶液加水稀释至 ,此时
,此时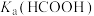
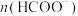
(3)某温度下,往某一恒容密闭容器中通入
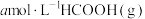 ,仅发生反应I和反应Ⅱ,
,仅发生反应I和反应Ⅱ, 后反应达到平衡,此时测得CO、HCOOH的浓度分别为
后反应达到平衡,此时测得CO、HCOOH的浓度分别为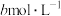 、
、 (不考虑碳元素的其他存在形式,
(不考虑碳元素的其他存在形式,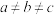 )。则
)。则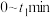 内
内
 (用含a、b、c的式子表示,下同),
(用含a、b、c的式子表示,下同), 的物质的量分数为
的物质的量分数为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】含氮化合物是重要的化工原料。存在如下转化关系:
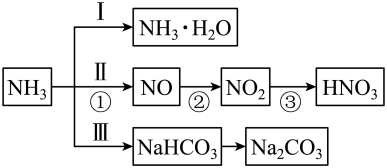
(1)转化Ⅱ中发生的系列反应,在工业上可以用来制备硝酸,写出①中反应的化学方程式为___________ 。
(2)①工业上常用浓氨水检验氯气管道是否泄漏,若泄露可看到白烟,用方程式解释检验原理___________ 。
②向固体氧化钙中滴加浓氨水,可用于实验室制取少量氨气,请结合化学用语简述原理___________ 。
(3)现代工业常以氯化钠、二氧化碳和氨气为原料制备纯碱。
①向一水合氨中通入过量的 CO2,该反应的离子方程式为___________ 。
②某工业纯碱样品中含少量 NaCl 和 NaHCO3,为测定该样品中 NaHCO3的质量分数, 某同学设计方案如下:准确称取 100.00 g 样品,反复加热、冷却、称量,直至所称量的固体质量几乎不变为止, 此时所得固体的质量为 99.38 g 。样品中 NaHCO3的质量分数为___________ 。
(4)以氨作为燃料的固体氧化物(含有O2-)燃料电池,具有全固态结构、能量效率高、无污染等特点。工作原理如图所示:

①固体氧化物电池工作的电解质,O2-移向___________ (填字母)。
A.电极a B.电极b
②该电池工作时, 电极a上发生的电极反应为___________ 。

(1)转化Ⅱ中发生的系列反应,在工业上可以用来制备硝酸,写出①中反应的化学方程式为
(2)①工业上常用浓氨水检验氯气管道是否泄漏,若泄露可看到白烟,用方程式解释检验原理
②向固体氧化钙中滴加浓氨水,可用于实验室制取少量氨气,请结合化学用语简述原理
(3)现代工业常以氯化钠、二氧化碳和氨气为原料制备纯碱。
①向一水合氨中通入过量的 CO2,该反应的离子方程式为
②某工业纯碱样品中含少量 NaCl 和 NaHCO3,为测定该样品中 NaHCO3的质量分数, 某同学设计方案如下:准确称取 100.00 g 样品,反复加热、冷却、称量,直至所称量的固体质量几乎不变为止, 此时所得固体的质量为 99.38 g 。样品中 NaHCO3的质量分数为
(4)以氨作为燃料的固体氧化物(含有O2-)燃料电池,具有全固态结构、能量效率高、无污染等特点。工作原理如图所示:

①固体氧化物电池工作的电解质,O2-移向
A.电极a B.电极b
②该电池工作时, 电极a上发生的电极反应为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】接触法制硫酸生产中的关键工序是 的催化氧化(
的催化氧化(
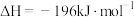 )。回答下列问题:
)。回答下列问题:
(1)补写完成 在催化剂
在催化剂 表面反应生成
表面反应生成 的历程:
的历程:
①
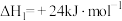
②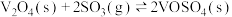
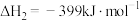
③___________ 。
(2)下列关于工业上用 和
和 反应合成
反应合成 的理解错误的是___________(填标号)。
的理解错误的是___________(填标号)。
(3) 的平衡转化率与反应温度和压强的关系如图所示。
的平衡转化率与反应温度和压强的关系如图所示。

①实际生产选择图中A点的反应条件,不选择B、C点的理由分别是___________ 。
②在温度T℃下,向某恒容密闭容器中充入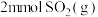 、
、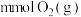 和
和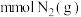 ,起始时压强为p,进行反应
,起始时压强为p,进行反应 。平衡时,
。平衡时, 转化率为80%,则平衡时
转化率为80%,则平衡时 分压为
分压为___________ (用含p的代数式表示,下同),平衡常数
___________ (以分压代替浓度计算,分压=总压×物质的量分数)。
(4)利用电化学原理可将 直接转化为
直接转化为 ,其工作原理如图所示,
,其工作原理如图所示,
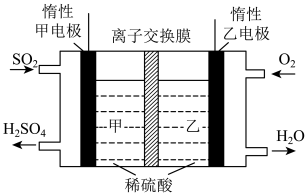
①为使电池持续工作,电解质溶液中的___________ (填离子符号)从___________ (填“甲”或“乙”,下同)室通过离子交换膜移向___________ 室。
②起始时,稀硫酸中含 和
和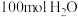 ,当甲电极消耗
,当甲电极消耗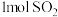 时,甲、乙两室中
时,甲、乙两室中 与
与 的总物质的量之比为
的总物质的量之比为___________ 。(两电极的产物均留在溶液中,忽略水的电离)
 的催化氧化(
的催化氧化(
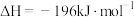 )。回答下列问题:
)。回答下列问题:(1)补写完成
 在催化剂
在催化剂 表面反应生成
表面反应生成 的历程:
的历程:①

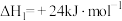
②
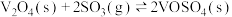
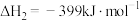
③
(2)下列关于工业上用
 和
和 反应合成
反应合成 的理解错误的是___________(填标号)。
的理解错误的是___________(填标号)。| A.该反应的实际工业生产条件是高温、常压和合适的催化剂 |
B.当温度、压强一定时,混合气组分中 和 和 分压比不变,可作为反应达到化学平衡状态的判据 分压比不变,可作为反应达到化学平衡状态的判据 |
C.反应过程中可将 液化移去,有利于提高正反应速率 液化移去,有利于提高正反应速率 |
| D.可以把该反应设计成原电池,实现能量的转化 |
 的平衡转化率与反应温度和压强的关系如图所示。
的平衡转化率与反应温度和压强的关系如图所示。
①实际生产选择图中A点的反应条件,不选择B、C点的理由分别是
②在温度T℃下,向某恒容密闭容器中充入
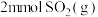 、
、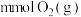 和
和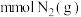 ,起始时压强为p,进行反应
,起始时压强为p,进行反应 。平衡时,
。平衡时, 转化率为80%,则平衡时
转化率为80%,则平衡时 分压为
分压为
(4)利用电化学原理可将
 直接转化为
直接转化为 ,其工作原理如图所示,
,其工作原理如图所示,
①为使电池持续工作,电解质溶液中的
②起始时,稀硫酸中含
 和
和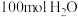 ,当甲电极消耗
,当甲电极消耗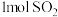 时,甲、乙两室中
时,甲、乙两室中 与
与 的总物质的量之比为
的总物质的量之比为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】化学电源广泛地应用于现代社会的生产和生活。请回答下列问题:
(1)原电池是一种化学能转变为电能的装置,所以原电池的设计原理与某类化学反应有关。你认为下列化学反应,可以设计成原电池的是___________(填字母)。
(2)化学反应均涉及相应的能量变化,为探究这些能量变化,某同学设计了如图两个实验,已知两个实验除了是否有导线连接两个金属棒外,其余均相同。

①该同学设计这两个实验的目的是___________ 。
②有关反应一段时间后的实验现象,下列说法正确的是___________ ( 填字母)。
A.图1中温度计的示数高于图2的示数
B.图1和图2中温度计的示数相等,且均高于室温。
C.图1和图2的气泡均产生于锌棒表面
D.图2中产生气体的速率比1慢
(3)若将用导线相连在一起,总质量为80.00 g的锌片和银片同时浸入稀硫酸中,工作一段时间后,取出金属片,进行洗涤、干燥、称量,得金属片的总质量为63.75 g,则装置工作时锌片上的电极反应式为___________ ,工作时间内装置所产生氢气的体积为 ___________ L(标准状况)。
(1)原电池是一种化学能转变为电能的装置,所以原电池的设计原理与某类化学反应有关。你认为下列化学反应,可以设计成原电池的是___________(填字母)。
| A.CaO+H2O=Ca(OH)2 |
B.C+CO2 2CO 2CO |
| C.NaOH+HCl=NaCl+H2O |
| D.2FeCl3+Cu=2FeCl2+CuCl2 |

①该同学设计这两个实验的目的是
②有关反应一段时间后的实验现象,下列说法正确的是
A.图1中温度计的示数高于图2的示数
B.图1和图2中温度计的示数相等,且均高于室温。
C.图1和图2的气泡均产生于锌棒表面
D.图2中产生气体的速率比1慢
(3)若将用导线相连在一起,总质量为80.00 g的锌片和银片同时浸入稀硫酸中,工作一段时间后,取出金属片,进行洗涤、干燥、称量,得金属片的总质量为63.75 g,则装置工作时锌片上的电极反应式为
您最近一年使用:0次



