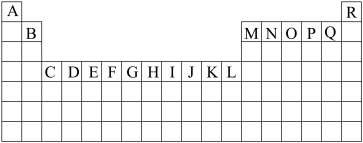
下表为元素周期表的一部分,请参照元素①~⑥在表中的位置,用化学用语 回答下列问题。

(1)元素①的原子结构示意图为_______ 。
(2)元素③和⑥可形成化合物,用电子式表示形成其过程_______ 。
(3)元素②、③形成简单离子的半径(填离子符号)_______ >_______ 。
(4)元素②、⑥形成的气态氢化物稳定性(填化学式,下同)_______ >_______ ;元素③、④形成的最高价氧化物水化物的碱性_______ >_______ 。
(5)元素④的最高价氧化物与元素⑤最高价氧化物的水化物稀溶液反应的离子方程式_______ 。
(6)元素①的最高价氧化物的水化物与元素③最高价氧化物的水化物稀溶液反应的离子方程式_______

(1)元素①的原子结构示意图为
(2)元素③和⑥可形成化合物,用电子式表示形成其过程
(3)元素②、③形成简单离子的半径(填离子符号)
(4)元素②、⑥形成的气态氢化物稳定性(填化学式,下同)
(5)元素④的最高价氧化物与元素⑤最高价氧化物的水化物稀溶液反应的离子方程式
(6)元素①的最高价氧化物的水化物与元素③最高价氧化物的水化物稀溶液反应的离子方程式
更新时间:2021-09-08 09:38:44
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】现有七种元素,其中A、B、C、D、E为短周期主族元素,F、G、H为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
(1)写出BA3的电子式:_________ 。
(2)B元素基态原子中能量最高的电子,其电子云在空间有_____ 个取向,原子轨道呈___ 形。
(3)某同学根据上述信息,推断C基态原子的核外电子排布图为 ,该同学所画的电子排布图违背了
,该同学所画的电子排布图违背了_____ 。
(4)比较B和D的电负性_________ >_________ (填元素符号)。
(5)G的价电子轨道排布式为_________ 。
(6)H位于_________ 族,__________ 区,该元素的核外电子排布式为__________ 。
| A元素的核外电子数和电子层数相等 |
| B元素原子的核外p电子数比s电子数少1 |
| C原子的第一至第四电离能如下:I1=738kJ/mol、I2=1451kJ/mol、I3=7733kJ/mol、I4=10540kJ/mol |
| D原子价电子层的p轨道半满 |
| E元素的主族序数与周期数的差为4 |
| F是前四周期中电负性最小的元素 |
| G是所在周期中未成对电子最多的元素 |
| H在周期表的第七列 |
(1)写出BA3的电子式:
(2)B元素基态原子中能量最高的电子,其电子云在空间有
(3)某同学根据上述信息,推断C基态原子的核外电子排布图为
 ,该同学所画的电子排布图违背了
,该同学所画的电子排布图违背了(4)比较B和D的电负性
(5)G的价电子轨道排布式为
(6)H位于
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】黑火药是中华民族对人类文明的重大贡献。“它”由 、硫磺(S)、木炭(C)按一定比例混合而成,爆炸时主要反应为:
、硫磺(S)、木炭(C)按一定比例混合而成,爆炸时主要反应为: 。结合反应中的物质和组成元素回答下列问题:
。结合反应中的物质和组成元素回答下列问题:
(1)如图显示元素周期表中钾元素的部分信息,

钾元素在周期表中的位置为______ 。“39.10”表示______ 。
A.钾原子的相对原子质量 B.钾元素的相对原子质量 C.钾元素的原子序数
(2)上述非金属元素中,原子半径最大的是______ ,非金属性最强______ ,能证明O元素的非金属性强于S元素的依据是______ 。
A.热稳定性:
B.
C.沸点: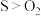
(3)氧元素有三种核素: 、
、 、
、 ,对这三种核素的描述不正确的是______。
,对这三种核素的描述不正确的是______。
(4) 、
、 、
、 三种物质中,属于共价化合物的是
三种物质中,属于共价化合物的是______ ,写出 的电子式
的电子式______ 。
(5)写出 结构示意图
结构示意图______ ,氮元素最高价氧化物对应水化物的分子式______ ,碳元素气态氢化物分子空间构型是______ 。
A.平面正四边形 B.正四面体 C.四棱锥
(6)黑火药爆炸时伴随了化学键的断裂和形成,涉及到的化学键类型是______ 。
A.离子键 B.共价键 C.离子键和共价键
(7)证明 是离子化合物的依据是______。
是离子化合物的依据是______。
 、硫磺(S)、木炭(C)按一定比例混合而成,爆炸时主要反应为:
、硫磺(S)、木炭(C)按一定比例混合而成,爆炸时主要反应为: 。结合反应中的物质和组成元素回答下列问题:
。结合反应中的物质和组成元素回答下列问题:(1)如图显示元素周期表中钾元素的部分信息,

钾元素在周期表中的位置为
A.钾原子的相对原子质量 B.钾元素的相对原子质量 C.钾元素的原子序数
(2)上述非金属元素中,原子半径最大的是
A.热稳定性:

B.

C.沸点:
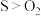
(3)氧元素有三种核素:
 、
、 、
、 ,对这三种核素的描述不正确的是______。
,对这三种核素的描述不正确的是______。| A.质子数相同 | B.质量相同 | C.化学性质相同 | D.位置相同(周期表中) |
(4)
 、
、 、
、 三种物质中,属于共价化合物的是
三种物质中,属于共价化合物的是 的电子式
的电子式(5)写出
 结构示意图
结构示意图A.平面正四边形 B.正四面体 C.四棱锥
(6)黑火药爆炸时伴随了化学键的断裂和形成,涉及到的化学键类型是
A.离子键 B.共价键 C.离子键和共价键
(7)证明
 是离子化合物的依据是______。
是离子化合物的依据是______。A. 易溶于水 易溶于水 | B. 溶液能导电 溶液能导电 |
C.熔融 能导电 能导电 | D. 熔点:334℃ 熔点:334℃ |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】短周期主族元素 、
、 、
、 、
、 、
、 在元素周期表中的位置如图所示,其中
在元素周期表中的位置如图所示,其中 为能壳中含量最高的金属元素。
为能壳中含量最高的金属元素。

请用化学用语回答下列问题:
(1) 元素在周期表中的位置:
元素在周期表中的位置:________ ,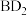 的空间结构为
的空间结构为_____ 形,上述非金属元素形成的简单氢化物中沸点最高的为________ (用化学式表示)。
(2) 、
、 、
、 对应的最高价含氧酸酸性由强到弱的顺序是
对应的最高价含氧酸酸性由强到弱的顺序是_______ (用化学式表示)。
(3) 与
与 同主族且相邻,
同主族且相邻, 、
、 、
、 可形成一个三原子分子,且每个原子均达到8电子稳定结构,则该分子的结构式为
可形成一个三原子分子,且每个原子均达到8电子稳定结构,则该分子的结构式为________ ;元素氢与元素 、元素氢与元素
、元素氢与元素 均可形成18电子分子,这两种分子在水溶液中反应有黄色沉淀生成,请写出该反应的化学方程式:
均可形成18电子分子,这两种分子在水溶液中反应有黄色沉淀生成,请写出该反应的化学方程式:________ 。
(4)由元素 、
、 形成的物质
形成的物质 与由元素
与由元素 和元素氢形成的化合物
和元素氢形成的化合物 可发生以下反应:
可发生以下反应:

①写出 的电子式
的电子式_________ ,含有的化学键类型为_______ 。
②写出 溶液与
溶液与 溶液反应的离子方程式
溶液反应的离子方程式_________ 。
 、
、 、
、 、
、 、
、 在元素周期表中的位置如图所示,其中
在元素周期表中的位置如图所示,其中 为能壳中含量最高的金属元素。
为能壳中含量最高的金属元素。
请用化学用语回答下列问题:
(1)
 元素在周期表中的位置:
元素在周期表中的位置: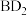 的空间结构为
的空间结构为(2)
 、
、 、
、 对应的最高价含氧酸酸性由强到弱的顺序是
对应的最高价含氧酸酸性由强到弱的顺序是(3)
 与
与 同主族且相邻,
同主族且相邻, 、
、 、
、 可形成一个三原子分子,且每个原子均达到8电子稳定结构,则该分子的结构式为
可形成一个三原子分子,且每个原子均达到8电子稳定结构,则该分子的结构式为 、元素氢与元素
、元素氢与元素 均可形成18电子分子,这两种分子在水溶液中反应有黄色沉淀生成,请写出该反应的化学方程式:
均可形成18电子分子,这两种分子在水溶液中反应有黄色沉淀生成,请写出该反应的化学方程式:(4)由元素
 、
、 形成的物质
形成的物质 与由元素
与由元素 和元素氢形成的化合物
和元素氢形成的化合物 可发生以下反应:
可发生以下反应:
①写出
 的电子式
的电子式②写出
 溶液与
溶液与 溶液反应的离子方程式
溶液反应的离子方程式
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】钠单质性质活泼,钠有多种化合物。请回答下列问题:
(1)钠与水反应的离子方程式为____________ 。
(2) 能够与人体呼出的
能够与人体呼出的 反应,用作呼吸面具中的供氧剂,请用化学方程式表示原因
反应,用作呼吸面具中的供氧剂,请用化学方程式表示原因________ 。
(3)除去碳酸钠固体中混有的碳酸氢钠的方法为__________________ (用化学方程式表示)。
(4)写出碳酸氢钠的一种用途_____________ 。
(5)某碳酸钠溶液中含有NaCl,验证该溶液中含有 的实验操作和现象是
的实验操作和现象是________________ 。
(6)已知碳酸钠可用于从海水提取溴,涉及的反应如下: ,该反应的离子方程式为
,该反应的离子方程式为__________________ 。
(7)工业盐的主要成分是 ,曾多次发生过因误食
,曾多次发生过因误食 而中毒的事件,其原因是
而中毒的事件,其原因是 把人体内的
把人体内的 转化为
转化为 而失去与
而失去与 结合的能力,这说明
结合的能力,这说明 具有
具有_________ 性。为了防止钢铁零件生锈,常用 进行化学处理方法使钢铁零件表面生成
进行化学处理方法使钢铁零件表面生成 的致密保护层—“发蓝”。化学处理过程中其中一步的反应为
的致密保护层—“发蓝”。化学处理过程中其中一步的反应为 (未配平),上述反应中氧化剂与还原剂的化学计量系数之比为
(未配平),上述反应中氧化剂与还原剂的化学计量系数之比为___________ 。
(1)钠与水反应的离子方程式为
(2)
 能够与人体呼出的
能够与人体呼出的 反应,用作呼吸面具中的供氧剂,请用化学方程式表示原因
反应,用作呼吸面具中的供氧剂,请用化学方程式表示原因(3)除去碳酸钠固体中混有的碳酸氢钠的方法为
(4)写出碳酸氢钠的一种用途
(5)某碳酸钠溶液中含有NaCl,验证该溶液中含有
 的实验操作和现象是
的实验操作和现象是(6)已知碳酸钠可用于从海水提取溴,涉及的反应如下:
 ,该反应的离子方程式为
,该反应的离子方程式为(7)工业盐的主要成分是
 ,曾多次发生过因误食
,曾多次发生过因误食 而中毒的事件,其原因是
而中毒的事件,其原因是 把人体内的
把人体内的 转化为
转化为 而失去与
而失去与 结合的能力,这说明
结合的能力,这说明 具有
具有 进行化学处理方法使钢铁零件表面生成
进行化学处理方法使钢铁零件表面生成 的致密保护层—“发蓝”。化学处理过程中其中一步的反应为
的致密保护层—“发蓝”。化学处理过程中其中一步的反应为 (未配平),上述反应中氧化剂与还原剂的化学计量系数之比为
(未配平),上述反应中氧化剂与还原剂的化学计量系数之比为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】氯化镁(MgCl2)可用作部分食品的添加剂、小麦粉处理剂、融雪剂等。某MgCO3样品中含有Fe2O3、FeO杂质,以该样品制取MgCl2溶液的流程如图:

已知: Fe3+在pH=6时可完全生成Fe (OH)3沉淀,Fe2+在pH=7.6时可完全生成Fe (OH) 2沉淀。
请回答下列问题:
(1)Fe2O3属于_____ (填“酸”或“碱”)性氧化物,写出一条基于其物理性质的用途________________ 。
(2)“酸溶”所得气体的电子式为__________________ 。
(3)加入氯水的作用是__________________ ,该反应的离子方程式为_____________________ 。
(4)滤渣的化学式为______________ 。
(5)请设计实验方案,检验过滤后所得氯化镁溶液中铁元素是否已被除尽:_________________ 。

已知: Fe3+在pH=6时可完全生成Fe (OH)3沉淀,Fe2+在pH=7.6时可完全生成Fe (OH) 2沉淀。
请回答下列问题:
(1)Fe2O3属于
(2)“酸溶”所得气体的电子式为
(3)加入氯水的作用是
(4)滤渣的化学式为
(5)请设计实验方案,检验过滤后所得氯化镁溶液中铁元素是否已被除尽:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】氨氮废水中的氮多以 和NH3∙H2O形式存在。某工厂处理氨氮废水流程如下:
和NH3∙H2O形式存在。某工厂处理氨氮废水流程如下:
(1)过程I的目的是将 转化为NH3,其离子方程式为
转化为NH3,其离子方程式为___________ ,鼓入热空气能将氨吹出的原因是___________ 。
(2)过程II加入NaClO溶液可将废水中残留的NH3∙H2O转化为无污染气体,该反应的化学方程式为___________ 。
(3)含余氯废水的主要成分是NaClO以及HClO,X可选用以下哪种溶液以达到将余氯转化为无毒物质的目的___________ (填字母)。
a.KOH b.Na2SO3 c.KMnO4 d.NaCl
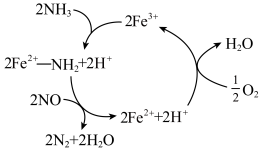
(4)有氧条件下,NH3催化还原NO是主要的烟气脱硝技术。在以Fe2O3为主的催化剂上可能发生的反应过程如图。写出总反应的化学方程式:___________ 。
 和NH3∙H2O形式存在。某工厂处理氨氮废水流程如下:
和NH3∙H2O形式存在。某工厂处理氨氮废水流程如下:
(1)过程I的目的是将
 转化为NH3,其离子方程式为
转化为NH3,其离子方程式为(2)过程II加入NaClO溶液可将废水中残留的NH3∙H2O转化为无污染气体,该反应的化学方程式为
(3)含余氯废水的主要成分是NaClO以及HClO,X可选用以下哪种溶液以达到将余氯转化为无毒物质的目的
a.KOH b.Na2SO3 c.KMnO4 d.NaCl
(4)有氧条件下,NH3催化还原NO是主要的烟气脱硝技术。在以Fe2O3为主的催化剂上可能发生的反应过程如图。写出总反应的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】如图是元素周期表的一部分,填写下列空格:
(1)比较④⑤⑧的原子半径由大到小依次___________ 。(填元素符号,下同)
(2)元素②与④形成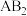 型化合物的电子式为
型化合物的电子式为___________ ,属于___________ 晶体。
(3)③的气态氢化物与⑨的气态氢化物反应的化学反应方程式:___________ ,所得产物中含有的化学键类型有___________ 。
(4)⑥、⑦最高价氧化物对应的水化物碱性较强的是___________ 。(填化学式)
| ① | |||||||||||||||||
| ② | ③ | ④ | ⑤ | ||||||||||||||
| ⑥ | ⑦ | ⑧ | ⑨ | ||||||||||||||
(2)元素②与④形成
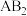 型化合物的电子式为
型化合物的电子式为(3)③的气态氢化物与⑨的气态氢化物反应的化学反应方程式:
(4)⑥、⑦最高价氧化物对应的水化物碱性较强的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】下表是周期表中的一部分,根据A~I在周期表中的位置,用元素符号或化学式回答下列问题:

(1)表中元素,化学性质最不活泼的是_________ ,只有负价而无正价的是_________ , 可用于制半导体材料的元素是_______ 。
(2)最高价氧化物的水化物碱性最强的是_________ ,酸性最强的是_________ ,呈两性的是________ ;
(3)A分别与D、E、F、G、H形成的化合物中,最稳定的_________ ;
(4)在B、C、D、J、 E、F、G、H中,原子半径最大的是_________ .

(1)表中元素,化学性质最不活泼的是
(2)最高价氧化物的水化物碱性最强的是
(3)A分别与D、E、F、G、H形成的化合物中,最稳定的
(4)在B、C、D、J、 E、F、G、H中,原子半径最大的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】表为四种短周期元素的相关信息
回答下列问题(注:涉及元素的均要用对应元素的元素符号书写作答)
(1)Y元素的最简单氢化物的空间构型是_______ 。
(2)写出R与Z元素组成最高价氧化物的杂化方式_______ ,其VSEPR模型为_______ 。
(3)Z、Q、R相比,其原子半径由大到小的顺序是_______ 。
(4)Y与R相比,非金属性较强的是_______ ,能证明这一结论的事实是_______ 。(用化学方程式表示)
(5)Q单质在过量Y的最高价氧化物中燃烧,生成黑色颗粒并产生大量白烟,写出该反应的化学方程式_______ 。
| 元素 | 元素的相关信息 |
| Y | 原子最外层电子数是次外层电子数的2倍 |
| Z | 地壳中含量最多的元素 |
| Q | 短周期中金属性最强 |
| R | 常温下,R的单质是淡黄色固体,常在火山喷口附近沉积 |
(1)Y元素的最简单氢化物的空间构型是
(2)写出R与Z元素组成最高价氧化物的杂化方式
(3)Z、Q、R相比,其原子半径由大到小的顺序是
(4)Y与R相比,非金属性较强的是
(5)Q单质在过量Y的最高价氧化物中燃烧,生成黑色颗粒并产生大量白烟,写出该反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】下表列出了①~⑩十种元素在元素周期表中的位置。

根据表中元素①~⑩,回答下列问题:
(1)①元素有三种质子数相同,中子数不同的核素,互称为_______ 。
(2)③、⑤的最高价氧化物对应的水化物的碱性:③_______ ⑤(选填“>”或“<”)。
(3)⑧的固态氢化物 与
与 反应生成
反应生成 和一种可燃性气体单质
和一种可燃性气体单质_______ (填化学式)。
(4)某小组同学设计实验比较VIIA族元素的非金属性: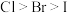
甲同学设计实验如下:打开分液漏斗的活塞,烧瓶中产生黄绿色气体,蘸有 溶液的棉球变为橙黄色,湿润的淀粉
溶液的棉球变为橙黄色,湿润的淀粉 试纸变蓝,已知:常温下浓盐酸与高锰酸钾反应生成氯气。
试纸变蓝,已知:常温下浓盐酸与高锰酸钾反应生成氯气。

乙同学设计实验如下:向A中通入少量 充分反应后,静置A中液体为橙黄色,将A中液体滴入试管内,取下试管,充分振荡,试管中的
充分反应后,静置A中液体为橙黄色,将A中液体滴入试管内,取下试管,充分振荡,试管中的 ;层变为紫红色。
;层变为紫红色。

①以上两位同学的实验,_______ (填“甲”或“乙)同学的实验能证明非金属性: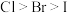 。
。
②除了利用卤素单质间的置换反应,下列可作为卤族元素非金属性递变规律的判断依据有_______ 。(填字母)
A. 、
、 、
、 的熔点逐渐升高 B.
的熔点逐渐升高 B. 、
、 、
、 的稳定性逐渐减弱
的稳定性逐渐减弱
C. 、
、 、
、 水溶液的酸性逐渐增强 D.
水溶液的酸性逐渐增强 D. 、
、 、
、 的还原性逐渐增强
的还原性逐渐增强

根据表中元素①~⑩,回答下列问题:
(1)①元素有三种质子数相同,中子数不同的核素,互称为
(2)③、⑤的最高价氧化物对应的水化物的碱性:③
(3)⑧的固态氢化物
 与
与 反应生成
反应生成 和一种可燃性气体单质
和一种可燃性气体单质(4)某小组同学设计实验比较VIIA族元素的非金属性:
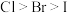
甲同学设计实验如下:打开分液漏斗的活塞,烧瓶中产生黄绿色气体,蘸有
 溶液的棉球变为橙黄色,湿润的淀粉
溶液的棉球变为橙黄色,湿润的淀粉 试纸变蓝,已知:常温下浓盐酸与高锰酸钾反应生成氯气。
试纸变蓝,已知:常温下浓盐酸与高锰酸钾反应生成氯气。
乙同学设计实验如下:向A中通入少量
 充分反应后,静置A中液体为橙黄色,将A中液体滴入试管内,取下试管,充分振荡,试管中的
充分反应后,静置A中液体为橙黄色,将A中液体滴入试管内,取下试管,充分振荡,试管中的 ;层变为紫红色。
;层变为紫红色。
①以上两位同学的实验,
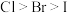 。
。②除了利用卤素单质间的置换反应,下列可作为卤族元素非金属性递变规律的判断依据有
A.
 、
、 、
、 的熔点逐渐升高 B.
的熔点逐渐升高 B. 、
、 、
、 的稳定性逐渐减弱
的稳定性逐渐减弱C.
 、
、 、
、 水溶液的酸性逐渐增强 D.
水溶液的酸性逐渐增强 D. 、
、 、
、 的还原性逐渐增强
的还原性逐渐增强
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】X、Y、Z、W是原子序数依次增大的短周期元素,且互不同族;其中只有两种为金属,X原子的最外层电子数与次外层电子数相等;X与W、Y与Z这两对原子的最外层电子数之和均为9,单质Y和W都可与浓的NaOH溶液反应。请回答下列问题:
(1)R与W同主族,且半径小于W,则R与水反应的化学方程式___________ ;
(2)X与Y化学性质相似,则单质X与浓的NaOH溶液反应的化学方程式是___________ ;
(3)Z的单质与NaOH溶液反应的离子方程式是___________ ;
(4)0.1 mol的单质W与50 mL 1.5 mol/L的FeBr2溶液反应,则被氧化的Fe2+和Br-的物质的量之比是___________ 。
(1)R与W同主族,且半径小于W,则R与水反应的化学方程式
(2)X与Y化学性质相似,则单质X与浓的NaOH溶液反应的化学方程式是
(3)Z的单质与NaOH溶液反应的离子方程式是
(4)0.1 mol的单质W与50 mL 1.5 mol/L的FeBr2溶液反应,则被氧化的Fe2+和Br-的物质的量之比是
您最近一年使用:0次