在半导体工业中有这样一句话:“从沙滩到用户”,其中由粗硅制纯硅的常用方法为:Si(粗)+2Cl2=SiCl4SiCl4+2H2=Si(纯)+4HCl。
若在25℃、101kPa条件下反应生成HCl气体49L,(注:25℃、101kPa条件下气体摩尔体积为24.5L•mol-1)则:
(1)反应生成HCl气体的质量为__ ,转移电子的总数为___ 。
(2)反应生成的HCl气体溶于127mL水中,得到密度为1.20g•mL-1的盐酸,此盐酸的物质的量浓度为___ 。
(3)“从沙滩到用户”涉及多个反应,其中制取粗硅的反应方程式为___ 。纯净的石英与烧碱反应可以制得水玻璃,反应的离子方程式为__ 。
(4)普通玻璃若以氧化物形式表示其组成为(质量分数):Na2O13%,CaO11.7%,SiO275.3%。现以石灰石、纯碱和石英为原料生产这种玻璃10t,石灰石的利用率为80%,纯碱和石英的利用率为95%,至少需要上述原料的质量是___ t。(保留两位小数)
若在25℃、101kPa条件下反应生成HCl气体49L,(注:25℃、101kPa条件下气体摩尔体积为24.5L•mol-1)则:
(1)反应生成HCl气体的质量为
(2)反应生成的HCl气体溶于127mL水中,得到密度为1.20g•mL-1的盐酸,此盐酸的物质的量浓度为
(3)“从沙滩到用户”涉及多个反应,其中制取粗硅的反应方程式为
(4)普通玻璃若以氧化物形式表示其组成为(质量分数):Na2O13%,CaO11.7%,SiO275.3%。现以石灰石、纯碱和石英为原料生产这种玻璃10t,石灰石的利用率为80%,纯碱和石英的利用率为95%,至少需要上述原料的质量是
更新时间:2020-06-04 09:42:58
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】某工厂用m1 kg铬铁矿粉(含Cr2O3 40%)制备K2Cr2O7,最终得到产品m2 kg,产率为_______ 。
您最近半年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)12.4 g Na2X含有0.4 mol Na+,Na2X的摩尔质量为____________
(2)标准状况下,18gCO和CO2的混合气体的物质的量为0.5mol,则此混合气体中CO和CO2的物质的量之比是_________ 。
(3)混合气体由N2和CH4组成,测得混合气体在标准状况下的密度为1.071g/L,则混合气体中N2和CH4的体积比为_______ 。
(4)某固态化合物X受热分解的反应为:X=A↑+B↑+C↑,在一定的温度和压强下测得反应生成的混合气体对氢气的相对密度为15,则X的摩尔质量是_________ 。
(2)标准状况下,18gCO和CO2的混合气体的物质的量为0.5mol,则此混合气体中CO和CO2的物质的量之比是
(3)混合气体由N2和CH4组成,测得混合气体在标准状况下的密度为1.071g/L,则混合气体中N2和CH4的体积比为
(4)某固态化合物X受热分解的反应为:X=A↑+B↑+C↑,在一定的温度和压强下测得反应生成的混合气体对氢气的相对密度为15,则X的摩尔质量是
您最近半年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】已知SiO2+2C Si+2CO↑;Si+C
Si+2CO↑;Si+C SiC。
SiC。
现有石英砂和炭粉的混合物1mol,于高温下在电炉里充分反应后,得残留固体;若石英砂与混和物的物质的量之比n(0<n<1),试讨论n取何值时,残留物的成分及其物质的量。
___________ 。
 Si+2CO↑;Si+C
Si+2CO↑;Si+C SiC。
SiC。现有石英砂和炭粉的混合物1mol,于高温下在电炉里充分反应后,得残留固体;若石英砂与混和物的物质的量之比n(0<n<1),试讨论n取何值时,残留物的成分及其物质的量。
| n | 例︰n= | __ | __ | __ | __ |
| 残留固体及物质的量(摩) | Si  | __ | __ | __ | __ |
您最近半年使用:0次
计算题
|
适中
(0.65)
【推荐2】工业生产粗硅的反应有:
SiO2+2C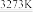 Si(粗)+2CO↑;SiO2+3C
Si(粗)+2CO↑;SiO2+3C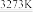 SiC+2CO↑。
SiC+2CO↑。
(1)若产品中粗硅与碳化硅的物质的量之比为1∶1,则参加反应的C 和SiO2的质量比为_____________ 。
(2)粗硅进一步制备纯硅的原理如下:
Si(粗)+2Cl2(g) SiCl4(l); SiCl4+2H2
SiCl4(l); SiCl4+2H2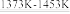 Si(纯)+4HCl。
Si(纯)+4HCl。
若上述反应中Si(粗)和SiCl4的利用率均为80%,制粗硅时有10%的SiO2转化为SiC,则生产25.2吨纯硅需纯度为75%石英砂_______________ 吨。
(3)工业上还可以通过如下图所示的流程制取纯硅:
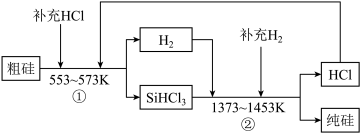
若反应①为:Si(粗)+3HCl(g)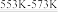 SiHCl3(l)+H2(g);
SiHCl3(l)+H2(g);
则反应②的化学方程式为____________________________ 。
假设每一轮次生产过程中,硅元素没有损失,反应①中HCl的利用率为α1,反应②中H2的利用率为α2,,若制备1mol纯硅,在第二轮次的生产中,现补充投入HCl和H2的物质的量之比是5∶1。则α1与α2的代数关系式为____________________ 。
SiO2+2C
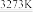 Si(粗)+2CO↑;SiO2+3C
Si(粗)+2CO↑;SiO2+3C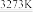 SiC+2CO↑。
SiC+2CO↑。(1)若产品中粗硅与碳化硅的物质的量之比为1∶1,则参加反应的C 和SiO2的质量比为
(2)粗硅进一步制备纯硅的原理如下:
Si(粗)+2Cl2(g)
 SiCl4(l); SiCl4+2H2
SiCl4(l); SiCl4+2H2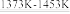 Si(纯)+4HCl。
Si(纯)+4HCl。若上述反应中Si(粗)和SiCl4的利用率均为80%,制粗硅时有10%的SiO2转化为SiC,则生产25.2吨纯硅需纯度为75%石英砂
(3)工业上还可以通过如下图所示的流程制取纯硅:

若反应①为:Si(粗)+3HCl(g)
 SiHCl3(l)+H2(g);
SiHCl3(l)+H2(g);则反应②的化学方程式为
假设每一轮次生产过程中,硅元素没有损失,反应①中HCl的利用率为α1,反应②中H2的利用率为α2,,若制备1mol纯硅,在第二轮次的生产中,现补充投入HCl和H2的物质的量之比是5∶1。则α1与α2的代数关系式为
您最近半年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】工业生产粗硅的主要原理为:SiO2+2C Si(粗)+2CO↑
Si(粗)+2CO↑
(1)若在制粗硅的过程中同时生成了碳化硅,请写出该反应的方程式:___________ 。
(2)若在制粗硅的过程中同时生成了碳化硅,且生成的硅和碳化硅的物质的量之比为5∶1,则参加反应的C和SiO2的质量比为__________ 。
(3)工业上可通过如下流程由粗硅制取纯硅:
Si(粗) SiCl4(l)
SiCl4(l) Si(纯)
Si(纯)
若上述反应中Si(粗)和SiCl4的利用率均为80%,制粗硅时有10%的SiO2转化为SiC,则生产100.8t纯硅,需纯度为75%的石英砂(主要成分为SiO2)多少吨?_____________
(4)工业上还可以通过下图所示的流程来制取纯硅:

反应①:Si(粗)+3HCl(g)=SiHCl3(l)+H2(g)
反应②:SiHCl3+H2=Si(纯)+3HCl
假设在每一轮次的投料生产中,硅元素没有损失,反应①中HCl的利用率为75%,反应②中H2的利用率为80%,则在下轮次的生产中,需补充投入HCl和H2的体积比为多少?_____________
 Si(粗)+2CO↑
Si(粗)+2CO↑(1)若在制粗硅的过程中同时生成了碳化硅,请写出该反应的方程式:
(2)若在制粗硅的过程中同时生成了碳化硅,且生成的硅和碳化硅的物质的量之比为5∶1,则参加反应的C和SiO2的质量比为
(3)工业上可通过如下流程由粗硅制取纯硅:
Si(粗)
 SiCl4(l)
SiCl4(l) Si(纯)
Si(纯)若上述反应中Si(粗)和SiCl4的利用率均为80%,制粗硅时有10%的SiO2转化为SiC,则生产100.8t纯硅,需纯度为75%的石英砂(主要成分为SiO2)多少吨?
(4)工业上还可以通过下图所示的流程来制取纯硅:

反应①:Si(粗)+3HCl(g)=SiHCl3(l)+H2(g)
反应②:SiHCl3+H2=Si(纯)+3HCl
假设在每一轮次的投料生产中,硅元素没有损失,反应①中HCl的利用率为75%,反应②中H2的利用率为80%,则在下轮次的生产中,需补充投入HCl和H2的体积比为多少?
您最近半年使用:0次

 溶液的浓度,取
溶液的浓度,取 待测液,向其中加入过量
待测液,向其中加入过量 溶液。充分反应后过滤、洗涤并干燥,得到
溶液。充分反应后过滤、洗涤并干燥,得到 沉淀的质量为
沉淀的质量为 ,反应的化学方程式为
,反应的化学方程式为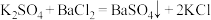 。求该溶液中
。求该溶液中

