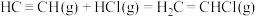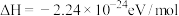下列说法不正确的是
| A.1g氢气在氧气中完全燃烧生成气态水,放出的热量为120.9kJ,氢气的燃烧热大于241.8kJ•mol-1 |
| B.500℃、30MPa下,将0.5molN2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放出的热量为19.3kJ,其热化学方程式为N2(g)+3H2(g)=2NH3(g)ΔH=﹣38.6kJ·mol-1 |
| C.常温下,若反应C(s)+CO2(g)=2CO(g)不能自发进行,则该反应的ΔH>0 |
| D.已知中和热为57.3kJ·mol-1,若将含0.5molH2SO4的浓溶液与含1molNaOH的溶液混合,放出的热量要大于57.3kJ |
19-20高二下·新疆昌吉·期中 查看更多[8]
更新时间:2020-06-05 12:51:07
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】已知: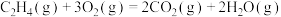
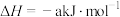


其他数据如下表:
下列说法正确的是
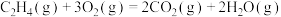
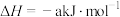


其他数据如下表:
| 化学键 | C=O | O=O | C-H | O-H | C=C |
键能/( ) ) | 798 | x | 413 | 463 | 615 |
A.乙烯的燃烧热为 |
B.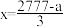 |
C.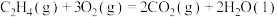 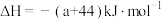 |
| D.当生成4molO-H键时,该反应放出热量一定为akJ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】CH4-CO2催化重整反应为:CH4(g)+ CO2(g)=2CO(g)+2H2(g)。已知:①C(s)+2H2(g)=CH4(g) ΔH=-75 kJ·mol−1②C(s)+O2(g)=CO2(g) ΔH=-394 kJ·mol−1③C(s)+1/2O2(g)=CO(g) ΔH=-111 kJ·mol−1则该催化重整反应的ΔH等于
| A.-580 kJ·mol−1 | B.+247 kJ·mol−1 | C.+208 kJ·mol−1 | D.-430kJ·mol−1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列热化学方程式,正确的是( )
| A.4g固体硫完全燃烧生成SO2,放出37 kJ热量:S(s)+O2(g)=SO2(g) ΔH= -296kJ/mol |
B.1molN2与3molH2在某密闭容器中反应放出73kJ热量,则反应的热化学方程式为:N2(g)+3H2(g) 2NH3(g) △H= -73kJ/mol 2NH3(g) △H= -73kJ/mol |
| C.甲烷的标准燃烧热为-890.3kJ·mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g) ==CO2(g)+ 2H2O(g) ΔH=-890.3kJ·mol-1 |
| D.强酸强碱的中和热为- 57.3 kJ/mol:Ba(OH) 2(aq)+H2SO4(aq)=BaSO4(S)+2H2O(l) ΔH=-114.6kJ/mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下对说法中,正确的是
| A.经加热而发生的化学反应都是吸热反应 |
B. 的反应均是自发进行的反应 的反应均是自发进行的反应 |
| C.水蒸气变为液态水时放出的能量就是该变化的反应热 |
D.可逆反应的 表示完全反应时的热量变化,与反应进行的程度无关 表示完全反应时的热量变化,与反应进行的程度无关 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】如图所示实验,探究反应中的能量变化。下列判断正确的是
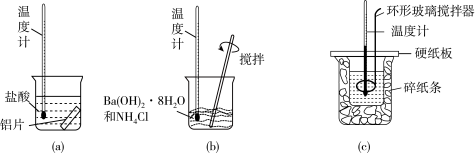

| A.实验可知,(a)、(b)、(c)所涉及的反应都是放热反应 |
| B.实验(c)中和热的测定应用同一支温度计,重复实验,取三次实验的平均数据 |
| C.实验(c)中选用浓的强酸溶液与强碱溶液反应,对实验结果没有影响 |
| D.将实验(a)中的铝片更换为等质量的铝粉后释放出的热量有所增加 |
您最近一年使用:0次
【推荐2】下列依据热化学方程式得出的结论正确的是
选项 | 热化学方程式 | 结论 |
A | H2(g)+Cl2(g) 2HCl(g) ΔH=-a kJ·mol-1 2HCl(g) ΔH=-a kJ·mol-1 | H2的燃烧热ΔH=-a kJ·mol-1 |
B | OH-(aq)+H+(aq)==H2O(l) ΔH=-57.3 kJ·mol-1 | 溶质物质的量为0.5 mol的Ba(OH)2稀溶液与足量稀H2SO4完全中和,放出的热量等于57.3 kJ |
C | C(s)+O2(g)=CO2(g) ΔH=-a kJ·mol-1; C(s)+  O2(g)=CO(g) ΔH=-b kJ·mol-1 O2(g)=CO(g) ΔH=-b kJ·mol-1 | b<a |
D | P4(s,白磷)=4P(s,红磷) ΔH=-29.2 kJ·mol-1 | P4(s,白磷)比P(s,红磷)稳定 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列热化学方程式书写正确的是
| A.2SO2 + O2 = 2SO3 △H=-196.6 kJ/mol |
| B.2H2O (g) =2H2(g)+O2(g) △H=-483.6kJ/mol |
| C.2H2(g)+O2(g) = 2H2O(l) △H=-571.6kJ/mol |
| D.C(s) + O2(g) = CO2(g) △H= +393.5kJ/mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】已知:氢气的燃烧热为 ,碳的燃烧热为
,碳的燃烧热为 。下列说法正确的是
。下列说法正确的是
 ,碳的燃烧热为
,碳的燃烧热为 。下列说法正确的是
。下列说法正确的是A.氢气燃烧热的热化学方程式为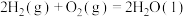 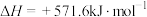 |
| B.标准状况下,22.4L氢气完全燃烧生成液态水放出热量285.8kJ |
C.反应 的 的 |
D.2.4g碳完全燃烧放出的热量为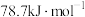 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列说法或表示方法正确的是
| A.等量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 |
| B.在稀溶液中: H++OH-=H2O;△H=-57.3kJ/mol,若将含0.5molH2SO4的浓硫酸与含1molNaOH的溶液混合,放出的热量大于57.3kJ; |
| C.由C(石墨)→C(金刚石);△H=+1.19 kJ/mol 可知,金刚石比石墨稳定 |
| D.在101kPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)=2H2O(l);△H=+285.8kJ/mol |
您最近一年使用:0次

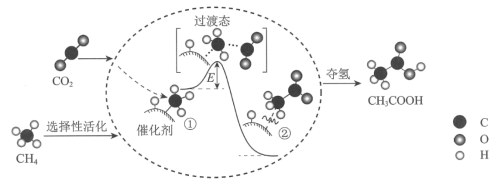
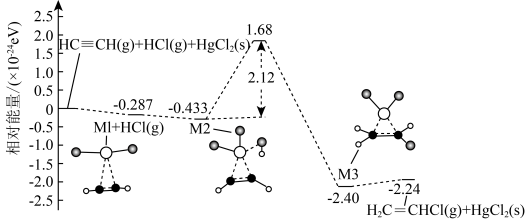
 与
与 形成的中间体
形成的中间体