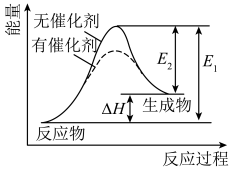
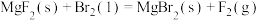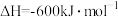在下列各说法中,正确的是( )
| A.同温同压下,反应H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的ΔH不同 |
B.雪是冬之精灵,在雪 水 水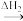 冰的转化中能量变化。ΔH1>0,ΔH2<0 冰的转化中能量变化。ΔH1>0,ΔH2<0 |
| C.1 mol H2SO4与1 mol Ba(OH)2反应生成BaSO4沉淀时放出的热量叫做中和热 |
| D.1 mol H2与0.5 mol O2反应放出的热量就是H2的燃烧热 |
更新时间:2020-06-10 19:28:39
|
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】已知反应:①101 kPa时,2C(s)+O2(g)=2CO(g) ΔH=-221 kJ/mol
②稀溶液中,H+(aq)+OH-(aq)=H2O(l)
ΔH=-57.3 kJ/mol下列结论正确的是( )
②稀溶液中,H+(aq)+OH-(aq)=H2O(l)
ΔH=-57.3 kJ/mol下列结论正确的是( )
| A.碳的燃烧热的数值大于110.5 kJ/mol |
| B.①的反应热ΔH为221 kJ/mol |
| C.浓硫酸与稀NaOH溶液反应的中和热为-57.3 kJ/mol |
| D.稀醋酸与稀NaOH溶液反应生成1 mol水,放出57.3 kJ热量 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】中和热测定实验中,下列操作一定会降低实验准确性的是
| A.用滴定管量取所用药品 |
| B.用环状不锈钢搅拌棒代替环状玻璃搅拌棒 |
| C.大、小烧杯体积相差较大,夹层间放的碎泡沫塑料较多 |
| D.测量HCl溶液的温度计用水洗净后再测NaOH溶液的温度 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐3】下列热化学方程式书写正确的是(ΔH的绝对值均正确)
| A.C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(g) ΔH=-1 322.8 kJ·mol-1(燃烧热) |
| B.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) ΔH=+57.3 kJ·mol-1(中和热) |
| C.S(s)+O2(g)=SO2(g) ΔH=-296.8 kJ·mol-1(反应热) |
| D.2NO2=O2+2NO ΔH=+116.2 kJ·mol-1(反应热) |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】25℃、101kPa时,强酸与强碱的稀溶液发生中和反应的中和热为57.3kJ·mol-1,辛烷的燃烧热为5518kJ·mol-1。下列热化学方程式书写正确的是
A.C8H18(l)+ O2(g)=8CO2(g)+9H2O(g) ΔH=-5518kJ·mol-1 O2(g)=8CO2(g)+9H2O(g) ΔH=-5518kJ·mol-1 |
| B.2C8H18(g)+25O2(g)=16CO2(g)+18H2O(l) ΔH=-5518kJ·mol-1 |
C.2H+(aq)+SO (aq)+Ba2+(aq)+2OH-(aq)=BaSO4(s)+2H2O(l) ΔH=-57.3kJ·mol-1 (aq)+Ba2+(aq)+2OH-(aq)=BaSO4(s)+2H2O(l) ΔH=-57.3kJ·mol-1 |
D.KOH(aq)+ H2SO4(aq)= H2SO4(aq)= K2SO4(aq)+H2O(l) ΔH=-57.3kJ·mol-1 K2SO4(aq)+H2O(l) ΔH=-57.3kJ·mol-1 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】含NaOH 20.0g的稀溶液与足量稀盐酸反应,放出28.7 kJ的热量,表示该反应的热化学方程式正确的是( )
| A.NaOH(aq)+HCl(aq)==NaCl(aq)+H2O(l)△H= +28.7 kJ·mol-1 |
| B.NaOH(aq)+HCl(aq)==NaCl(aq)+H2O(l)△H= _28.7 kJ·mol-1 |
| C.NaOH(aq)+HCl(aq)==NaCl(aq)+H2O(l)△H=+57.4 kJ·mol-1 |
| D.NaOH(aq)+HCl(aq)==NaCl(aq)+H2O(l)△H= _57.4 kJ·mol-1 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】下列说法正确的是
A.甲烷的标准燃烧热为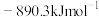 ,则甲烷燃烧的热化学方程式可表示为 ,则甲烷燃烧的热化学方程式可表示为 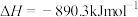 |
B.分别向等浓度等体积的 溶液中加入足量的稀醋酸和稀盐酸,反应的热效应分别为 溶液中加入足量的稀醋酸和稀盐酸,反应的热效应分别为 、 、 ,则 ,则 |
C.500℃、30MPa下,将0.5mol 和1.5mol 和1.5mol 置于密闭容器中充分反应生成 置于密闭容器中充分反应生成 ,放热19.3kJ,其热化学方程式为 ,放热19.3kJ,其热化学方程式为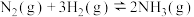 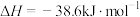 |
D.25℃,101kPa时,强酸与强碱的稀溶液发生中和反应的中和热 为 为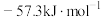 ,硫酸与氢氧化钾溶液反应的热化学方程式为 ,硫酸与氢氧化钾溶液反应的热化学方程式为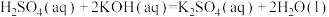 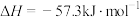 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】关于热化学方程式,下列说法正确 的是
A.标准状况下,  完全燃烧生成液态水,放出 完全燃烧生成液态水,放出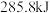 热量,则 热量,则 燃烧热的热化学方程式为: 燃烧热的热化学方程式为:  |
B.  ,则金刚石比石墨稳定 ,则金刚石比石墨稳定 |
C.  和 和  反应的中和热, 反应的中和热, |
D.500℃、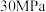 下, 下,  和 和  充分反应生成 充分反应生成 并放热 并放热 ,则热化学方程式为: ,则热化学方程式为: 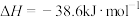 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐3】已知充分燃烧ag乙炔(C2H2)气体时生成1mol二氧化碳气体和液态水,并放出热量bkJ(b>0),则下列表示乙炔燃烧热的热化学方程式的是
| A.2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l)ΔH=-4bkJ·mol-1 |
| B.C2H2(g)+5/2O2(g)=2CO2(g)+H2O(l)ΔH=-2bkJ·mol-1 |
| C.2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l)ΔH=+4bkJ·mol-1 |
| D.C2H2(g)+5/2O2(g)=2CO2(g)+H2O(g)ΔH=-2bkJ·mol-1 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】下列说法正确的是
| A.热化学方程式中化学计量数不能为分数 |
| B.燃烧热是指101KPa时,1mol纯物质完全燃烧放出的热量 |
| C.化学反应的反应热只与反应体系的始态和终态有关,与反应途径无关 |
| D.所有碰撞都是有效碰撞 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列与化学反应能量变化相关的叙述中,正确的是
| A.热化学方程式的ΔH大小与化学计量数无关 |
| B.利用盖斯定律,可计算某些难以直接测量的反应焓变 |
| C.H2(g)的燃烧热ΔH=-285.8kJ·mol-1,则反应2H2O(g)=2H2(g)+O2(g)的反应热ΔH=+571.6kJ·mol-1 |
| D.测定中和反应反应热的时候,测量盐酸和NaOH混合溶液刚开始的温度,记为反应前体系的温度 |
您最近一年使用:0次

 2HCl(g)在光照和点燃条件下的△H不同
2HCl(g)在光照和点燃条件下的△H不同