如图中A、B、C、D是同周期或同主族的相邻元素:
(1)已知:A元素的最低价为-3价,它的最高价氧化物含氧56.34%,原子核内中子数比质子数多1个,则A元素原子的质量数为_____ 。
(2)写出元素符号:A_____ ,C_____ ,D____ 。
(3)A、B、C三种元素最高价氧化物的水化物中酸性最强的是____ (填化学式)。
(4)B、D两种元素和氢组成的气态氢化物中稳定性最强的是___ ,还原性最强的____ (填化学式)。
| D | ||
| A | B | C |
(1)已知:A元素的最低价为-3价,它的最高价氧化物含氧56.34%,原子核内中子数比质子数多1个,则A元素原子的质量数为
(2)写出元素符号:A
(3)A、B、C三种元素最高价氧化物的水化物中酸性最强的是
(4)B、D两种元素和氢组成的气态氢化物中稳定性最强的是
更新时间:2020-06-27 00:47:46
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】现有部分短周期元素的性质或原子结构如下表:
(1)四种元素原子半径由大到小的顺序是(写元素符号)_________________________ 。
(2)元素Y与氢元素形成的一种离子YH4+,写出该微粒的电子式________ (用元素符号表示)。
(3)T元素的简单阴离子的结构示意图是______________________ ,
(4)证明该粒子的还原性比Z-强的离子方程式是____________________ .
(5)元素Z的单质与氢氧化钠溶液反应的化学方程式为_______________________ 。
(6)将9g单质X在足量氧气中燃烧,所得气体通入1L 1mol·L-1NaOH溶液中,完全吸收后,将溶液在减压低温条件下蒸干,得到不含结晶水的固体质量为____________ g。
| 元素编号 | 元素性质或原子结构 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| T | 最外层电子数是电子层数的2倍 |
| Z | 元素最高正价是+7价 |
(1)四种元素原子半径由大到小的顺序是(写元素符号)
(2)元素Y与氢元素形成的一种离子YH4+,写出该微粒的电子式
(3)T元素的简单阴离子的结构示意图是
(4)证明该粒子的还原性比Z-强的离子方程式是
(5)元素Z的单质与氢氧化钠溶液反应的化学方程式为
(6)将9g单质X在足量氧气中燃烧,所得气体通入1L 1mol·L-1NaOH溶液中,完全吸收后,将溶液在减压低温条件下蒸干,得到不含结晶水的固体质量为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】元素周期表是学习物质结构和性质的重要工具。下图列出8种元素在周期表中的位置。请用化学符号回答下列问题:
(1)a可与另一种元素组成含18个电子的双原子分子,其电子式是_______ 。b、c,f、g简单离子半径由大到小的顺序是_______ (用离子符号表示)。
(2)用电子式表示h、f形成化合物的过程_______ 。
(3)b、c两种元素形成的淡黄色固体可在潜艇中作为氧气来源,其存在的化学键类型有_______ ,写出该固体在潜艇中供氧时发生的任意一个化学方程式_______ 。
(4)我国航天事业蓬勃发展,空间站“天和”核心舱的太阳翼电池采用了自主研发的砷化镓器件,能量转化效率大大提高。
①镓(Ga)的原子结构示意图为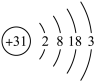 ,镓元素在元素周期表中的位置是
,镓元素在元素周期表中的位置是_______ 。b、d、g三种元素与镓元素化学性质相似的是_______ (填元素符号)。
②下列关于镓及其化合物的说法正确的是_______ 。
A.碱性:氢氧化镓>氢氧化铝 B.Ga可做半导体材料 C.元素的金属性:Ga>K
③类比氢氧化铝的性质,写出氢氧化镓与NaOH溶液反应的化学方程式_______ 。
| a | |||||||||||||||||
| b | |||||||||||||||||
| c | d | e | f | ||||||||||||||
| g | h | ||||||||||||||||
(2)用电子式表示h、f形成化合物的过程
(3)b、c两种元素形成的淡黄色固体可在潜艇中作为氧气来源,其存在的化学键类型有
(4)我国航天事业蓬勃发展,空间站“天和”核心舱的太阳翼电池采用了自主研发的砷化镓器件,能量转化效率大大提高。
①镓(Ga)的原子结构示意图为
 ,镓元素在元素周期表中的位置是
,镓元素在元素周期表中的位置是②下列关于镓及其化合物的说法正确的是
A.碱性:氢氧化镓>氢氧化铝 B.Ga可做半导体材料 C.元素的金属性:Ga>K
③类比氢氧化铝的性质,写出氢氧化镓与NaOH溶液反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】下表列出了①~⑨九种元素在周期表中的位置:
请按要求回答下列问题:

(1)元素④的名称是______ ,元素④在周期表中所处位置______ ,从元素原子得失电子的角度看,元素④形成的单质具有______ 性(填“氧化性”或“还原性”).
(2)元素⑦的原子结构示意图是______ .
(3)按气态氢化物的稳定性由弱到强的顺序排列,⑥④⑦的氢化物稳定性:______ (写氢化物的化学式).
(4)写出元素⑤形成的单质与水反应的化学方程式_____________________ .
(5)①与⑦能形成一种化合物,用电子式表示该化合物的形成过程______ .
请按要求回答下列问题:

(1)元素④的名称是
(2)元素⑦的原子结构示意图是
(3)按气态氢化物的稳定性由弱到强的顺序排列,⑥④⑦的氢化物稳定性:
(4)写出元素⑤形成的单质与水反应的化学方程式
(5)①与⑦能形成一种化合物,用电子式表示该化合物的形成过程
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】原子序数由小到大排列的四种短周期元素X、Y、Z、W,其中X、Z、W与氢元素可形成XH3、H2Z和HW三种分子:Y与氧元素可形成Y2O和Y2O2两种离子化合物。
(1)Y与Z形成的化合物电子式为_______ ,含有的化学键是_______ 。
(2)用电子式表示Y2O的形成过程:_______ 。
(3)X、Z、W三种元素的最高价氧化物对应的水化物中,酸性最强的是_______ (填化学式)。
(4)XH3与W2发生置换反应,生成的化合物属于离子化合物,该离子化合物是_______ (填化学式)。
(5)W2与NaOH溶液反应生成的三种物质中,属于离子化合物的是_______ 。
(1)Y与Z形成的化合物电子式为
(2)用电子式表示Y2O的形成过程:
(3)X、Z、W三种元素的最高价氧化物对应的水化物中,酸性最强的是
(4)XH3与W2发生置换反应,生成的化合物属于离子化合物,该离子化合物是
(5)W2与NaOH溶液反应生成的三种物质中,属于离子化合物的是
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
【推荐2】现有原子序数依次增大的A、B、C、D、E五种短周期元素。已知A、C、D三原子的最外电子层中共有10个电子,这三种元素的最高价氧化物的水化物之间,两两皆能反应。请回答下列问题:
(1)B元素的名称是_____ 。
(2)D、E两元素的最高价氧化物的水化物中,酸性较强的是_____ (填化学式)。
(3)写出A、C两元素的最高价氧化物的水化物之间反应的离子方程式:________ 。
(4)将A元素的过氧化物15.6g与足量二氧化碳完全反应,有____ mol 电子发生转移。
(1)B元素的名称是
(2)D、E两元素的最高价氧化物的水化物中,酸性较强的是
(3)写出A、C两元素的最高价氧化物的水化物之间反应的离子方程式:
(4)将A元素的过氧化物15.6g与足量二氧化碳完全反应,有
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】已知A、Y、Z、B四种元素分别是元素周期表中连续三个短周期的主族元素,且原子序数依次增大。Y的最外层电子数是其电子层数的3倍,且Y、Z同主族。
(1)A、B两种元素的元素符号:A_____________ 、B_____________ 。
(2)由A、Z所形成的化合物A2Z的电子式是_____________ ,化合物类型是__________ (填“离子化合物”或“共价化合物”)。
(3)由A、Y两元素形成的四核18电子的化合物的电子式为________ ,结构式为_________ ,由A、Y、B所形成的化合物AYB的电子式是__________ , 存在的化学键____________ 。
(4)化学反应A2+B2=2AB的能量变化如图所示,则下列说法正确的是___________ 。

A.该反应是放热反应
B.断裂1 mol A—A键和1 mol B—B键能放出x kJ能量
C.断裂2 mol A—B键需要吸收y kJ的能量
D.2 mol AB的总能量高于1 mol A2和1 mol B2的总能量
(1)A、B两种元素的元素符号:A
(2)由A、Z所形成的化合物A2Z的电子式是
(3)由A、Y两元素形成的四核18电子的化合物的电子式为
(4)化学反应A2+B2=2AB的能量变化如图所示,则下列说法正确的是

A.该反应是放热反应
B.断裂1 mol A—A键和1 mol B—B键能放出x kJ能量
C.断裂2 mol A—B键需要吸收y kJ的能量
D.2 mol AB的总能量高于1 mol A2和1 mol B2的总能量
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】某种食品添加剂由四种元素组成(结构如图),已知X、Y、Z、W为短周期主族元素,且原子序数依次增大,X与Z同主族,W与X原子的最外层电子数之和等于Y原子的最外层电子数,Y是地壳中含量最多的元素。
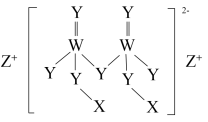
请回答下列问题:
(1)基态Z原子的核外电子排布式为______ ,W元素最高价氧化物的水化物的化学式为______ 。
(2)X、Y、Z、W原子半径由小到大的顺序为______ (用元素符号表示)。
(3)W元素以及同族相邻元素所形成的氢化物中,沸点由低到高的顺序是_____ (填化学式),原因是:______ 。
(4)元素Y可分别与元素X和Z形成原子个数比为1∶1的两种晶体,这两种晶体类型分别是_____ 晶体、_____ 晶体。

请回答下列问题:
(1)基态Z原子的核外电子排布式为
(2)X、Y、Z、W原子半径由小到大的顺序为
(3)W元素以及同族相邻元素所形成的氢化物中,沸点由低到高的顺序是
(4)元素Y可分别与元素X和Z形成原子个数比为1∶1的两种晶体,这两种晶体类型分别是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】W、X、Y、Z是周期表前36号元素中的四种常见元素,其原子序数依次增大。W、Y的氧化物是导致酸雨的主要物质,X的基态原子的核外有7个原子轨道填充了电子,Z能形成红色(或砖红色)的Z2O和黑色的ZO两种氧化物。
(1)W位于元素周期表第_____ 周期第____ 族。W的气态氢化物稳定性比H2O(g)_______ (填“强”或“弱”)。
(2)Y的基态原子的核外电子排布式是______ , Y的第一电离能比X的________ (填“大”或“小”)。
(3)Y的最高价氧化物对应水化物的浓溶液与Z的单质反应的化学方程式是_________ 。
(1)W位于元素周期表第
(2)Y的基态原子的核外电子排布式是
(3)Y的最高价氧化物对应水化物的浓溶液与Z的单质反应的化学方程式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】有A、B、C、D四种短周期元素,它们的原子序数由A到D依次增大,已知A和B原子有相同的电子层数,且A的L层电子数是K层电子数的两倍,C在空气中燃烧时呈现黄色火焰,C的单质在加热下与B的单质充分反应,可以得到与D单质颜色相同的淡黄色固态化合物,E的核电荷数为C、D两种元素原子序数之和。试根据以上叙述回答:
(1)元素名称:A_____ ;B_____ ;C_____ 。
(2)E元素在周期表中的位置_____ 。
(3)写出AB2与C2B2反应的化学方程式并用单线桥表示电子转移的方向:_____ 。
(4)电子式表示化合物C2D的形成过程:______ 。
(1)元素名称:A
(2)E元素在周期表中的位置
(3)写出AB2与C2B2反应的化学方程式并用单线桥表示电子转移的方向:
(4)电子式表示化合物C2D的形成过程:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】X、Y、Z、M是四种常见的短周期元素,其中Y、Z、M属于同一周期,X和M属于同一主族,Y元素最外层电子数为1,Z元素核内有14个质子。M和X元素可形成共价化合物MX2,它能使品红溶液褪色。请用化学式或化学用语回答下列问题:
(1)写出X、Y、Z的元素符号:X_______ ;Y_______ ;Z_________ 。
(2)M在周期表的位置是__________________________ 。
(3)用电子式表示Y2M的形成过程_________________ 。
(4)原子半径由小到大的顺序是____________________ 。
(5)四种元素中最高价氧化物对应水化物酸性最强的是__________ 。把锌片和铜片用导线连接浸入其稀溶液中(如图所示),则_______ 是正极,该极发生_______ 反应,电极反应式为________________ 。
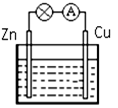
(6)X、Z、M三种元素的简单氢化物稳定性最强的是_________ ,其电子式是_______ 。
(1)写出X、Y、Z的元素符号:X
(2)M在周期表的位置是
(3)用电子式表示Y2M的形成过程
(4)原子半径由小到大的顺序是
(5)四种元素中最高价氧化物对应水化物酸性最强的是

(6)X、Z、M三种元素的简单氢化物稳定性最强的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】A、B、W、D、E,Y为短周期元素,且原子序数依次增大,A是周期表中原子半径最小的,B的最外层电子数比次外层多3,B、W同周期,A、D同主族,A、W能形成两种液态化合物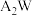 和
和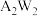 ,E元素的周期序数与主族序数相等。Y是短周期中原子序数最大的主族元素。
,E元素的周期序数与主族序数相等。Y是短周期中原子序数最大的主族元素。
(1)W2-离子的结构示意图为_______ ,E元素在周期表中的位置为_______ ,
(2)A2W2的电子式为_______ ,在酸性条件下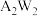 可以将
可以将 氧化成
氧化成 ,写出该反应的离子方程式
,写出该反应的离子方程式_______ 。当消耗2mol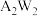 时,转移的电子数为
时,转移的电子数为_______ 。
(3)下列事实能说明Y元素的非金属性比硫(S)元素的非金属性强的是_______ ;
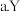 单质与
单质与 溶液反应,溶液变浑浊
溶液反应,溶液变浑浊
 在氧化还原反应中,1molY单质比1molS得电子多
在氧化还原反应中,1molY单质比1molS得电子多
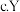 和S两元素的简单氢化物受热分解,前者的分解温度高
和S两元素的简单氢化物受热分解,前者的分解温度高
(4)用电子式表示B的最简单氢化物的形成过程_______ 。
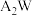 和
和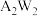 ,E元素的周期序数与主族序数相等。Y是短周期中原子序数最大的主族元素。
,E元素的周期序数与主族序数相等。Y是短周期中原子序数最大的主族元素。(1)W2-离子的结构示意图为
(2)A2W2的电子式为
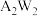 可以将
可以将 氧化成
氧化成 ,写出该反应的离子方程式
,写出该反应的离子方程式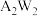 时,转移的电子数为
时,转移的电子数为(3)下列事实能说明Y元素的非金属性比硫(S)元素的非金属性强的是
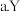 单质与
单质与 溶液反应,溶液变浑浊
溶液反应,溶液变浑浊 在氧化还原反应中,1molY单质比1molS得电子多
在氧化还原反应中,1molY单质比1molS得电子多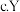 和S两元素的简单氢化物受热分解,前者的分解温度高
和S两元素的简单氢化物受热分解,前者的分解温度高(4)用电子式表示B的最简单氢化物的形成过程
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】有A、B、C、D、E五种短周期主族元素,原子序数由A到E逐渐增大。①A元素最外层电子数是次外层电子数的2倍。②B的阴离子和C的阳离子与氖原子的电子层结构相同。③在通常状况下,B的单质是气体,0.1 mol B的气体与足量的氢气完全反应共有0.4 mol电子转移。④C的单质在点燃时与B的单质充分反应,生成淡黄色的固体,此淡黄色固体能与AB2反应可生成B的单质。⑤D的气态氢化物与其最高价含氧酸间能发生氧化还原反应。请写出:
(1)A元素的最高价氧化物的结构式___________ ;B元素在周期表中的位置________________ 。
(2)C单质在B单质中燃烧的生成物中所含化学键类型有_______________________________ ;C与D 能形成化合物的电子式______________________ 。
(3)D元素的低价氧化物与E的单质的水溶液反应的化学方程式为_______________________ 。
(4)元素D与元素E相比,非金属性较强的是_______ (用元素符号表示),下列表述中能证明这一事实的是________ (填选项序号)。
a.常温下D的单质和E的单质状态不同 b.E的氢化物比D的氢化物稳定
c.一定条件下D和E的单质都能与钠反应 d.D的最高价含氧酸酸性弱于E的最高价含氧酸
e.D的单质能与E的氢化物反应生成E单质
(1)A元素的最高价氧化物的结构式
(2)C单质在B单质中燃烧的生成物中所含化学键类型有
(3)D元素的低价氧化物与E的单质的水溶液反应的化学方程式为
(4)元素D与元素E相比,非金属性较强的是
a.常温下D的单质和E的单质状态不同 b.E的氢化物比D的氢化物稳定
c.一定条件下D和E的单质都能与钠反应 d.D的最高价含氧酸酸性弱于E的最高价含氧酸
e.D的单质能与E的氢化物反应生成E单质
您最近一年使用:0次



