下列说法正确的是
| A.MgF2晶体中的化学键是只有离子键 |
| B.某物质在熔融态能导电,则该物质中一定含有离子键 |
| C.N2和BCl3两种分子中,每个原子的最外层都具有8电子稳定结构 |
| D.干冰是分子晶体,其溶于水生成碳酸的过程只需克服分子间作用力 |
更新时间:2020-06-30 16:41:21
|
相似题推荐
单选题
|
较易
(0.85)
【推荐1】下列关于范德华力影响物质性质的叙述中,正确的是。
| A.范德华力是决定由分子构成物质的熔点、沸点高低的惟一因素 |
| B.范德华力与物质的性质没有必然的联系 |
| C.范德华力能够影响物质的化学性质和物理性质 |
| D.范德华力仅是影响物质部分物理性质的一种因素 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】下列说法正确的是( )
| A.分子间作用力与化学键的大小相当 |
| B.分子间作用力比化学键强得多 |
| C.分子间作用力主要影响物质的化学性质 |
| D.化学键存在于分子内部,分子间作用力存在于分子之间 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下表所列数据是对应晶体的熔点,据此判断下列选项正确的是
| 晶体 |  | Na |  |  |  |  |  |  |
| 熔点 | 920℃ | 97.8℃ | 1291℃ | 190℃ | 2073℃ | -107℃ | -57℃ | 1723℃ |
| A.含有金属阳离子的晶体一定是离子晶体 |
B. 和 和 晶体熔化时,克服的微粒间作用力类型相同 晶体熔化时,克服的微粒间作用力类型相同 |
| C.同族元素的最高价氧化物不可能形成不同类型的晶体 |
| D.金属晶体的熔点不一定比分子晶体的高 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列各项中,符合分子晶体特征的是
A.熔点为 ,易溶于水,水溶液能导电 ,易溶于水,水溶液能导电 |
B.无色晶体,熔点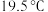 ,易溶于乙醇、氯仿、丙酮等 ,易溶于乙醇、氯仿、丙酮等 |
C.黄色晶体,熔点 ,熔融态不导电 ,熔融态不导电 |
D.熔点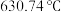 ,沸点 ,沸点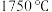 ,导电 ,导电 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列叙述中正确的是
| A.干冰升华时碳氧键发生断裂 |
| B.CaO和SiO2晶体中都不存在单个小分子 |
| C.Na2O与Na2O2所含的化学键类型完全相同 |
| D.Br2蒸气被木炭吸附时共价键被破坏 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列说法正确的是( )
| A.HF、HCl、HBr、HI的热稳定性依次减弱,沸点却依次升高 |
| B.熔融状态下能导电的化合物一定含离子键 |
| C.HCl气体溶于水的过程中,既有化学键的断裂,也有化学键的形成,所以是化学变化 |
| D.NaHSO4晶体中阴阳离子的个数比是1:2且熔化时破坏的是离子键和共价键 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐3】化学键是高中化学中非常重要的一个概念,它与物质变化过程中的能量变化息息相关,下列说法正确的有个
①化学键是相邻原子间强烈的相互吸引力
② 是一种非常稳定的化合物,这是因为分子间存在氢键
是一种非常稳定的化合物,这是因为分子间存在氢键
③ 中既存在离子键又存在共价键
中既存在离子键又存在共价键
④速滑馆“冰丝带”用干冰作为制冷剂,干冰升华过程中破坏了共价键
⑤物理变化也可以有化学键的破坏
⑥化学变化中一定有化学键的断裂和形成,所以一定伴随能量的变化
⑦ 、
、 熔点后者高,是因为前者克服分子间作用力而后者熔化破坏共价键
熔点后者高,是因为前者克服分子间作用力而后者熔化破坏共价键
①化学键是相邻原子间强烈的相互吸引力
②
 是一种非常稳定的化合物,这是因为分子间存在氢键
是一种非常稳定的化合物,这是因为分子间存在氢键③
 中既存在离子键又存在共价键
中既存在离子键又存在共价键④速滑馆“冰丝带”用干冰作为制冷剂,干冰升华过程中破坏了共价键
⑤物理变化也可以有化学键的破坏
⑥化学变化中一定有化学键的断裂和形成,所以一定伴随能量的变化
⑦
 、
、 熔点后者高,是因为前者克服分子间作用力而后者熔化破坏共价键
熔点后者高,是因为前者克服分子间作用力而后者熔化破坏共价键| A.2个 | B.3个 | C.4个 | D.5个 |
您最近一年使用:0次



