下表是元素周期表的一部分,针对表中的①~⑩种元素,填写下列空白:
(1)在这些元素中,化学性质最活泼的是___ ;化学性质最不活泼的是___ (填元素符号)。
(2)在最高价氧化物对应的水化物中,酸性最强的化合物的分子___ ,④和⑧结合的化合物的电子式是___ ,该化合物属于___ 化合物(填“共价”或“离子”)。
(3)③、⑥、⑦三种元素的原子半径由大到小的顺序是___ (用化学式表示),⑥、⑦、⑧三种元素的非金属性逐渐___ ,①、④、⑩三种元素原子还原性逐渐___ (填“增强”或“减弱”)。
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0族 | |
| 第二周期 | ① | ② | ③ | |||||
| 第三周期 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ||
| 第四周期 | ⑩ |
(2)在最高价氧化物对应的水化物中,酸性最强的化合物的分子
(3)③、⑥、⑦三种元素的原子半径由大到小的顺序是
更新时间:2020-07-03 21:59:39
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】我国科研团队成功研发“硅—石墨烯—锗晶体管”,代表着我国在这一尖端科技领域走在了世界的前列。
(1)碳元素在元素周期表中的位置是第___ 周期、第IVA族。
(2)硅元素最高价氧化物的化学式为___ 。
(3)Si的非金属性弱于S的,用原子结构解释原因:Si和S在同一周期,原子核外电子层数相同,___ ,原子半径Si大于S,得电子能力Si弱于S。
(4)在元素周期表中,锗(Ge)位于第4周期,与Si同主族。Ge—Si与Ge—Te作温差发电,可用于宇航、卫星与空间站的启动电源。下列关于Ge的推断中,正确的是__ (填字母)。
a.原子的最外层电子数为4
b.原子半径:Ge>Si
c.最高价氧化物对应的水化物酸性强于H2SiO3
(1)碳元素在元素周期表中的位置是第
(2)硅元素最高价氧化物的化学式为
(3)Si的非金属性弱于S的,用原子结构解释原因:Si和S在同一周期,原子核外电子层数相同,
(4)在元素周期表中,锗(Ge)位于第4周期,与Si同主族。Ge—Si与Ge—Te作温差发电,可用于宇航、卫星与空间站的启动电源。下列关于Ge的推断中,正确的是
a.原子的最外层电子数为4
b.原子半径:Ge>Si
c.最高价氧化物对应的水化物酸性强于H2SiO3
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】短周期元素在周期表中的位置如表所示。请按要求回答下列问题:
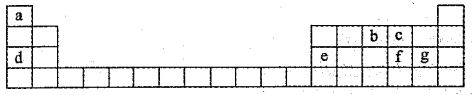
(1)元素f在周期表中的位置是___ 。
(2)上表中七种元素分别形成的单核离子中离子半径最大的是___ (填离子符号)。
(3)由a、b、g形成的常见化合物的电子式为___ ,该化合物属于___ 化合物(填“离”或“共价”)。
(4)写出e、g形成的化合物与过量d元素形成的最高价氧化物对应的水化物相互反应的离子方程式:___ 。
(5)下列事实能说明g元素的非金属性比f元素的非金属性强的是___ 。
A.将g的单质与f的气态氢化物的水溶液反应,生成淡黄色沉淀‘
B.g元素形成的简单氢化物的酸性比f元素形成的简单氢化物的酸性强
C.f与Fe化合时产物中Fe为+2价,g与Fe化合时产物中Fe为+3价
D.g与氢气化合比f与氢气化合更容易
(6)a分别与b、c形成的二元化合物中,所含电子数为18的两种分子之间可发生氧化还原反应生成b元素的单质,其反应的化学方程式为___ 。

(1)元素f在周期表中的位置是
(2)上表中七种元素分别形成的单核离子中离子半径最大的是
(3)由a、b、g形成的常见化合物的电子式为
(4)写出e、g形成的化合物与过量d元素形成的最高价氧化物对应的水化物相互反应的离子方程式:
(5)下列事实能说明g元素的非金属性比f元素的非金属性强的是
A.将g的单质与f的气态氢化物的水溶液反应,生成淡黄色沉淀‘
B.g元素形成的简单氢化物的酸性比f元素形成的简单氢化物的酸性强
C.f与Fe化合时产物中Fe为+2价,g与Fe化合时产物中Fe为+3价
D.g与氢气化合比f与氢气化合更容易
(6)a分别与b、c形成的二元化合物中,所含电子数为18的两种分子之间可发生氧化还原反应生成b元素的单质,其反应的化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】下图是元素周期表的一部分。按要求填写下列空白:

(1)元素①~⑧中原子半径最大的元素在周期表中的位置为_______ ;
(2)①~⑧元素的最高价氧化物对应的水化物中,酸性最强的是_______ (填化学式);
(3)④⑦两种元素形成的气态氢化物稳定性由大到小的顺序是_______ ;(用化学式表示);
(4)⑤和⑥两种元素的最高价氧化物对应的水化物反应的离子方程式_______ ;
(5)为了证明⑤和⑥两种元素的金属性强弱,下列说法或实验能提供证据的是________ 。
A.比较两种元素的单质的熔点、沸点高低
B.将两种元素的单质分别与冷水反应,观察反应的剧烈程度
C.比较两种元素的最高价氧化物对应的水化物的碱性强弱

(1)元素①~⑧中原子半径最大的元素在周期表中的位置为
(2)①~⑧元素的最高价氧化物对应的水化物中,酸性最强的是
(3)④⑦两种元素形成的气态氢化物稳定性由大到小的顺序是
(4)⑤和⑥两种元素的最高价氧化物对应的水化物反应的离子方程式
(5)为了证明⑤和⑥两种元素的金属性强弱,下列说法或实验能提供证据的是
A.比较两种元素的单质的熔点、沸点高低
B.将两种元素的单质分别与冷水反应,观察反应的剧烈程度
C.比较两种元素的最高价氧化物对应的水化物的碱性强弱
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】下表是元素周期律的一部分用元素符号或化学式、化学用语填空。
(1)在写出元素⑦的气态氢化物的电子式___ ;元素⑨的核外电子排布式为___ ;
(2)元素③的原子核外有___ 种能量不同的电子,有___ 种运动状态电子。
(3)元素⑧与⑥形成的晶体是___ 晶体:元素⑤和⑩形成的分子属于___ 分子(极性、非极性):
(4)写出元素②与④的最高价氧化物对应水化物之间反应的方程式___ ;
(5)元素⑨和⑩的非金属性比较更强___ (元素符号),用一个方程式说明这一结论___ 。
(6)关于氟、钠、镁、氯四种元素的性质递变规律,描述正确的是___ (写编号)。
a.原子半径:Na<Cl b.离子半径:F-<Mg2+
c.热稳定性:HF>HCl d.碱性:NaOH>Mg(OH)2
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ⑤ | ⑦ | ⑧ | ||||
| 3 | ② | ③ | ④ | ⑥ | ⑨ | ⑩ |
(1)在写出元素⑦的气态氢化物的电子式
(2)元素③的原子核外有
(3)元素⑧与⑥形成的晶体是
(4)写出元素②与④的最高价氧化物对应水化物之间反应的方程式
(5)元素⑨和⑩的非金属性比较更强
(6)关于氟、钠、镁、氯四种元素的性质递变规律,描述正确的是
a.原子半径:Na<Cl b.离子半径:F-<Mg2+
c.热稳定性:HF>HCl d.碱性:NaOH>Mg(OH)2
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】下表是元素周期表的一部分,请参照元素①-⑩在表中的位置,回答下列问题。
(1)画出①和③两种元素的原子1:2组成的化合物的电子式_______ 。
(2)元素①-⑩中化学性质最不活泼的元素是_______ (填元素符号)。
(3)⑧的离子结构示意图为_______ 。
(4)用电子式表示③与⑤形成的原子个数比为1 ∶2的化合物的形成过程_______ 。
(5)由元素③、⑤、⑨形成的一种常见的杀菌消毒剂中存在的化学键有_______ 。
(6)硒(Se)被誉为“生命元素”,科学补硒可以减少疾病的发生。周期表中元素Se的位置在⑧的下方,下列推断正确的是_______(填字母序号)
| 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(2)元素①-⑩中化学性质最不活泼的元素是
(3)⑧的离子结构示意图为
(4)用电子式表示③与⑤形成的原子个数比为1 ∶2的化合物的形成过程
(5)由元素③、⑤、⑨形成的一种常见的杀菌消毒剂中存在的化学键有
(6)硒(Se)被誉为“生命元素”,科学补硒可以减少疾病的发生。周期表中元素Se的位置在⑧的下方,下列推断正确的是_______(填字母序号)
| A.SeO2具有还原性 | B.H2Se的稳定性比H2S强 |
| C.H2SeO4的酸性强于H2SO4 | D.SeO2在一定条件下可与NaOH溶液反应 |
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】今年为“国际化学元素周期表年”,元素周期表揭示了化学元素间的内在联系。
(1)图为氟元素在元素周期表中的部分信息和氟原子及镁原子的结构示意图。
写出图中①代表的元素符号_________ ,镁属于_________ (填“金属”或“非金属”)元素。
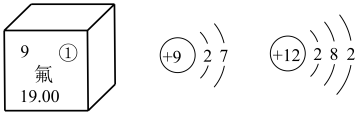
(2)由氟和镁两种元素组成化合物氟化镁的化学式为__________________
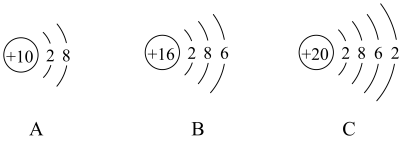
(3)A、B、C原子结构示意图中,与镁原子的化学性质最相似的是_________ (填序号)。
(4)已知原子的核外电子层数与元素所在周期表中周期的序数相同,则镁元素在元素周期表中排在第_______ 周期。
(1)图为氟元素在元素周期表中的部分信息和氟原子及镁原子的结构示意图。
写出图中①代表的元素符号

(2)由氟和镁两种元素组成化合物氟化镁的化学式为
(3)A、B、C原子结构示意图中,与镁原子的化学性质最相似的是

(4)已知原子的核外电子层数与元素所在周期表中周期的序数相同,则镁元素在元素周期表中排在第
您最近一年使用:0次



