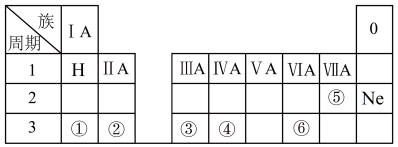
下图是元素周期表的一部分。按要求填写下列空白:

(1)元素①~⑧中原子半径最大的元素在周期表中的位置为_______ ;
(2)①~⑧元素的最高价氧化物对应的水化物中,酸性最强的是_______ (填化学式);
(3)④⑦两种元素形成的气态氢化物稳定性由大到小的顺序是_______ ;(用化学式表示);
(4)⑤和⑥两种元素的最高价氧化物对应的水化物反应的离子方程式_______ ;
(5)为了证明⑤和⑥两种元素的金属性强弱,下列说法或实验能提供证据的是________ 。
A.比较两种元素的单质的熔点、沸点高低
B.将两种元素的单质分别与冷水反应,观察反应的剧烈程度
C.比较两种元素的最高价氧化物对应的水化物的碱性强弱

(1)元素①~⑧中原子半径最大的元素在周期表中的位置为
(2)①~⑧元素的最高价氧化物对应的水化物中,酸性最强的是
(3)④⑦两种元素形成的气态氢化物稳定性由大到小的顺序是
(4)⑤和⑥两种元素的最高价氧化物对应的水化物反应的离子方程式
(5)为了证明⑤和⑥两种元素的金属性强弱,下列说法或实验能提供证据的是
A.比较两种元素的单质的熔点、沸点高低
B.将两种元素的单质分别与冷水反应,观察反应的剧烈程度
C.比较两种元素的最高价氧化物对应的水化物的碱性强弱
更新时间:2021-01-28 22:05:41
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】下表是元素周期表的一部分,除标出的元素外,表中的每个编号代表一种元素。请根据要求回答问题:
(1)②的元素符号是___________
(2)①、④的原子半径大小是①___________ ④(填“>”或“<”)
(3)②和③两种元素的简单氢化物的稳定性关系是:③___________ ②(填“>”或“<”)
(4)④和⑤的最高价氧化物对应的水化物相互反应的离子方程式是___________ 。
 | ⅠA | 0 | |||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||
| 2 | ② | ③ | |||||||
| 3 | ④ | ⑤ | Ar | ||||||
(1)②的元素符号是
(2)①、④的原子半径大小是①
(3)②和③两种元素的简单氢化物的稳定性关系是:③
(4)④和⑤的最高价氧化物对应的水化物相互反应的离子方程式是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】针对下面10种元素,完成以下各小题。
(1)地壳中含量最多的元素是_______ (填名称)。
(2)化学性质最不活泼的元素是_______ (填元素符号)。
(3)Al的原子结构示意图为_______ 。
(4)C与N相比,原子半径较小的是_______ 。
(5)最高价氧化物对应的水化物碱性最强的是_______ (填化学式)。
(6)MgO和Al2O3中,属于两性氧化物的是_______ 。
(7)S和Cl相比,元素非金属性较强的是_______ 。
(8)可用来制造光导纤维的物质是_______ ,晶体硅的主要用途是_______ (写出一种)。
(9)工业上以N2和H2为原料,在高温、高压和催化剂存在的条件下制备NH3,请写出反应的化学方程式:_______ 。
| 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | C | N | O | Ne | ||||
| 3 | Na | Mg | Al | Si | S | Cl |
(1)地壳中含量最多的元素是
(2)化学性质最不活泼的元素是
(3)Al的原子结构示意图为
(4)C与N相比,原子半径较小的是
(5)最高价氧化物对应的水化物碱性最强的是
(6)MgO和Al2O3中,属于两性氧化物的是
(7)S和Cl相比,元素非金属性较强的是
(8)可用来制造光导纤维的物质是
(9)工业上以N2和H2为原料,在高温、高压和催化剂存在的条件下制备NH3,请写出反应的化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】已知元素周期表中共有18个纵行,下图实线表示元素周期表的边界。按核外电子排布,可把元素周期表里的元素划分为 区、
区、 区、
区、 区、
区、 区等。除
区等。除 区外,其他区的名称来自按构造原理最后填入电子的能级的符号。
区外,其他区的名称来自按构造原理最后填入电子的能级的符号。
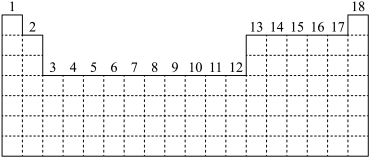
(1)请在上图中用实线画出 区、
区、 区、
区、 区、
区、 区的边界线,并分别用阴影
区的边界线,并分别用阴影 和
和 表示
表示 区和
区和 区
区________ 。
(2)有的同学受这种划分的启发,认为 区内第6、7纵行的部分元素可以排在另一区,你认为应排在
区内第6、7纵行的部分元素可以排在另一区,你认为应排在______ 区。
(3)请在上述元素周期表中用元素符号标出 轨道处于半充满状态的元素
轨道处于半充满状态的元素________ 。
 区、
区、 区、
区、 区、
区、 区等。除
区等。除 区外,其他区的名称来自按构造原理最后填入电子的能级的符号。
区外,其他区的名称来自按构造原理最后填入电子的能级的符号。
(1)请在上图中用实线画出
 区、
区、 区、
区、 区、
区、 区的边界线,并分别用阴影
区的边界线,并分别用阴影 和
和 表示
表示 区和
区和 区
区(2)有的同学受这种划分的启发,认为
 区内第6、7纵行的部分元素可以排在另一区,你认为应排在
区内第6、7纵行的部分元素可以排在另一区,你认为应排在(3)请在上述元素周期表中用元素符号标出
 轨道处于半充满状态的元素
轨道处于半充满状态的元素
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】表是元素周期表的一部分,针对表中①~⑩元素,用元素符号或化学式 填空:
(1)表中元素,化学性质最不活泼的是_______ ,只有负价而无正价的是_______ ,金属性最强的元素是_______ ,非金属性最强的元素是_______ 。
(2)在③~⑧元素中,元素的最高价氧化物对应的水化物中酸性最强的是_______ ,碱性最强的是_______ ,呈两性的氢氧化物是_______ ;写出三者之间互相反应的方程式:_______ 、_______ 、_______ 。
(3)③与④,化学性质较活泼的是③,怎样用化学实验证明?答_______ ,在⑦与⑩的单质中,化学性质较活泼的是_______ ,可用化学反应说明该事实:_______ 。
| 主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 四 | ⑨ | ⑩ |
(1)表中元素,化学性质最不活泼的是
(2)在③~⑧元素中,元素的最高价氧化物对应的水化物中酸性最强的是
(3)③与④,化学性质较活泼的是③,怎样用化学实验证明?答
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】如图是元素周期表的一部分:
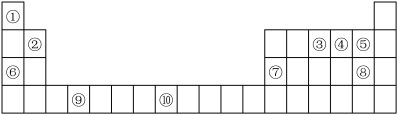
(1)表中属于s区的非金属元素是________ (用元素符号表示),元素⑩核外电子排布式为________________ ,
(2)元素③④⑤电负性由小到大___________ (用元素符号表示)
(3)若元素③用R表示,为什么可以形成RCl3分子,不可以形成RCl5分子:____________ 。
(4)元素⑤与⑧元素相比非金属性较强的是________ (写元素名称),下列表述中能证明这一事实的是__________ 。
A.气态氢化物的挥发性和稳定性 B.两元素的电负性
C.单质分子中的键能 D.含氧酸的酸性
E.氢化物中X—H键的键长 F.两单质在自然界中的存在形式
(5)元素⑦的氧化物与元素⑧的最高价氧化物的水化物反应的离子方程式为______________________ 。

(1)表中属于s区的非金属元素是
(2)元素③④⑤电负性由小到大
(3)若元素③用R表示,为什么可以形成RCl3分子,不可以形成RCl5分子:
(4)元素⑤与⑧元素相比非金属性较强的是
A.气态氢化物的挥发性和稳定性 B.两元素的电负性
C.单质分子中的键能 D.含氧酸的酸性
E.氢化物中X—H键的键长 F.两单质在自然界中的存在形式
(5)元素⑦的氧化物与元素⑧的最高价氧化物的水化物反应的离子方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】元素周期律和周期表是我们研究、预测物质性质的重要工具。下表是元素周期表中前四周期的5种元素的相关信息。
回答下列问题:
(1)D在元素周期表中的位置是___________ 。
(2)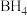 的电子式为
的电子式为___________ 。
(3)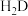 分子中含有
分子中含有___________ (填“极性共价键”或“非极性共价键”)。
(4)少量E的单质加入水中剧烈反应,反应的化学方程式是___________ ;将一块C单质加入上述形成的强碱溶液中反应的离子方程式是___________ ;元素A、E的最高价氧化物对应的水化物中,碱性更强的物质是___________ (填写化学式)。
(5)D的简单离子与的E简单离子半径较大的是___________ (填离子符号)。
(6)任意写出一个化学反应方程式证明氧元素的非金属性强于D元素___________ 。
| 元素 | 元素性质或原子结构 |
| A | 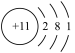 |
| B | B能形成多种单质,其中一种单质是硬度最大的物质 |
| C | 地壳中含量最高的金属元素,其合金可用于制造飞机外壳 |
| D | D的单质是一种黄色晶体 |
| E | 用E的碳酸盐做焰色试验时火焰为紫色(透过蓝色钴玻璃片) |
(1)D在元素周期表中的位置是
(2)
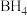 的电子式为
的电子式为(3)
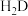 分子中含有
分子中含有(4)少量E的单质加入水中剧烈反应,反应的化学方程式是
(5)D的简单离子与的E简单离子半径较大的是
(6)任意写出一个化学反应方程式证明氧元素的非金属性强于D元素
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】下表列出了①~⑨九种元素在周期表中的位置:请按要求回答下列问题:
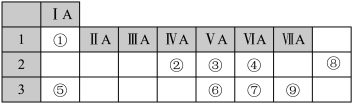
(1)元素④的名称是______ ,元素④在周期表中所处位置______ ,从元素原子得失电子的角度看,元素④形成的单质具有______ 性(填“氧化”或“还原”).
(2)元素⑦的原子结构示意图是______ .
(3)按气态氢化物的稳定性由弱到强的顺序排列,⑥④⑦的氢化物稳定性:______ (写氢化物的化学式).
(4)写出元素⑤形成的单质与水反应的化学方程式_________ .

(1)元素④的名称是
(2)元素⑦的原子结构示意图是
(3)按气态氢化物的稳定性由弱到强的顺序排列,⑥④⑦的氢化物稳定性:
(4)写出元素⑤形成的单质与水反应的化学方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】(1)下列曲线分别表示元素某种性质与核电荷数的关系(Z为核电荷数,Y为元素的有关性质),把与下面的元素有关性质相符合的曲线的标号填入相应括号中。
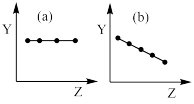
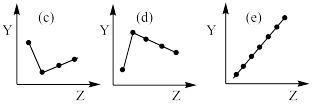
①ⅡA族元素的最外层电子数___ 。
②ⅦA族元素氢化物的沸点___ 。
③O2-、F-、Na+、Mg2+、Al3+的离子半径___ 。
④第三周期元素的最高化合价___ 。
⑤第二周期元素Be、B、C、N、O的原子半径___ 。
(2)比较下列性质(用“>”、“=”、“<”填空)
①氧化性:Cl2___ Br2
②还原性:H2S___ HCl
③碱性:Mg(OH)2___ Al(OH)3
④稳定性:H2S__ H2O
(3)元素性质呈周期性变化的决定因素是__ 。
A.元素原子半径大小呈周期性变化
B.元素的相对原子质量依次递增
C.元素原子核外电子排布呈周期性变化
D.元素的最高正化合价呈周期性变化
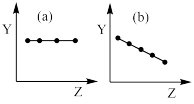

①ⅡA族元素的最外层电子数
②ⅦA族元素氢化物的沸点
③O2-、F-、Na+、Mg2+、Al3+的离子半径
④第三周期元素的最高化合价
⑤第二周期元素Be、B、C、N、O的原子半径
(2)比较下列性质(用“>”、“=”、“<”填空)
①氧化性:Cl2
②还原性:H2S
③碱性:Mg(OH)2
④稳定性:H2S
(3)元素性质呈周期性变化的决定因素是
A.元素原子半径大小呈周期性变化
B.元素的相对原子质量依次递增
C.元素原子核外电子排布呈周期性变化
D.元素的最高正化合价呈周期性变化
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】根据元素周期表1-18号元素的性质和递变规律,回答下列问题。
(1)属于金属元素的有___ 种,金属性最强的元素与氧反应生成的化合物有___ 、___ (填两种化合物的化学式)。
(2)属于稀有气体的是___ (填元素符号,下同)。
(3)第三周期中,原子半径最大的是___ (稀有气体除外)。
(4)推测Si、N最简单氢化物的稳定性:___ 大于___ (填化学式)。
(1)属于金属元素的有
(2)属于稀有气体的是
(3)第三周期中,原子半径最大的是
(4)推测Si、N最简单氢化物的稳定性:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】现有甲、乙、丙、丁四种短周期元素,甲元素M电子层上的电子数是K电子层上电子数的一半,乙元素的单质在室温下,冷的浓硫酸或空气中表面都能生成致密的氧化膜;丙元素的单质在常温下是黄绿色气体;丁元素的二价阴离子与丙元素的阴离子具有相同的电子层结构。
(1)写出甲、乙、丙、丁四种元素的符号。
甲______ 、乙_______ 、丙_______ 、丁________ 。
(2)甲元素和乙元素最高价氧化物对应的水化物碱性较强的是__________ (填化学式)。
(3)将过量的丙元素的单质通入FeBr2溶液中,发生反应的离子方程式是:_________ ,该反应的氧化剂是:______ (写物质名称)。
(1)写出甲、乙、丙、丁四种元素的符号。
甲
(2)甲元素和乙元素最高价氧化物对应的水化物碱性较强的是
(3)将过量的丙元素的单质通入FeBr2溶液中,发生反应的离子方程式是:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】2019年是化学元素周期表问世150周年,联合国宣布此年为“国际化学元素周期表年”。元素周期表在学习、研究中有很重要的作用,下表是元素周期表的一部分。
(1)e的元素符号是___ 。
(2)f、g的最高价氧化物对应的水化物中,酸性较强的物质的化学式是___ 。
(3)c的金属性强于d的金属性,用原子结构解释原因:___ ,失电子能力c大于d。
(4)下列对于a及其化合物的推断中,正确的是___ (填序号)。
①a的最高正价和最低负价绝对值相等
②a的氢化物的稳定性强于f的氢化物的稳定性
③单质a比单质b难与氢气反应
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | a | b | ||||||
| 3 | c | d | e | f | g |
(1)e的元素符号是
(2)f、g的最高价氧化物对应的水化物中,酸性较强的物质的化学式是
(3)c的金属性强于d的金属性,用原子结构解释原因:
(4)下列对于a及其化合物的推断中,正确的是
①a的最高正价和最低负价绝对值相等
②a的氢化物的稳定性强于f的氢化物的稳定性
③单质a比单质b难与氢气反应
您最近一年使用:0次