A、B、C、D、E五种元素,已知:
①A原子的最外层电子数是次外层电子数的两倍,B的阴离子与C的阳离子跟氖原子的电子层结构相同,E原子的最外层上的电子数比最内层多5。
②常温下B2是气体,它的相对分子质量是氢气的16倍。
③C的单质在B2中燃烧,生成淡黄色固体F,F与AB2反应可生成B2。
④D的单质在B2中燃烧,发出蓝紫色火焰,生成有刺激性气味的气体DB2,D在DB2中的含量为50%。根据以上情况回答:
(1)E位于第___ 周期___ 族;
(2)C的离子结构示意图是_____ ,F中的化学键为______ ;
(3)AB2的电子式为___ ; F和AB2反应的化学方程式为_______ ;
(4)C、D、E三种元素的原子半径从小到大的顺序为___ ; (用元素符号回答)
(5)常温下,E的单质与C的最高价氧化物对应水化物的水溶液反应的离子方程式为__________ 。
①A原子的最外层电子数是次外层电子数的两倍,B的阴离子与C的阳离子跟氖原子的电子层结构相同,E原子的最外层上的电子数比最内层多5。
②常温下B2是气体,它的相对分子质量是氢气的16倍。
③C的单质在B2中燃烧,生成淡黄色固体F,F与AB2反应可生成B2。
④D的单质在B2中燃烧,发出蓝紫色火焰,生成有刺激性气味的气体DB2,D在DB2中的含量为50%。根据以上情况回答:
(1)E位于第
(2)C的离子结构示意图是
(3)AB2的电子式为
(4)C、D、E三种元素的原子半径从小到大的顺序为
(5)常温下,E的单质与C的最高价氧化物对应水化物的水溶液反应的离子方程式为
更新时间:2020-07-16 07:42:56
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】x、y、z、w、u为前20号元素中的五种,在一定条件下组成的单质及其化合物有如图所示转化关系。其中H、I、G为固体,F为液体,其他为气体。G由w- 和u2+ 两种具有相同电子构型的离子构成,是实验室常用的干燥剂。 回答下列问题:
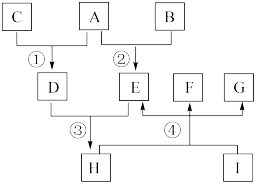
(1)G的电子式是___________
(2)在实验室中检验气体E的的简单方法是___________
(3)写出实验室中加热混合物的方法制备C的反应的离子方程式:___________
(4)写出反应④的化学方程式___________
(5)一定量E、C混合恰好完全反应且产生白烟,则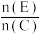 的范围为
的范围为___________

(1)G的电子式是
(2)在实验室中检验气体E的的简单方法是
(3)写出实验室中加热混合物的方法制备C的反应的离子方程式:
(4)写出反应④的化学方程式
(5)一定量E、C混合恰好完全反应且产生白烟,则
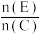 的范围为
的范围为
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】M、N、X、Y、Z五种元素(不含稀有气体)核电荷数依次增大,且均小于18。其中只有Y是金属元素且M、Y元素原子最外层都只有一个电子,N、Z元素原子的最外层电子数是电子层数的2倍,X、Z元素原子的最外层电子数相等。
(1)由此可以推知(填元素符号):M是_________ ,N是_________ ,X是_______ ,Y是______ ,Z是_______
(2)用不同的化学符号表示下列离子的核外电子排布:
①Y离子的电子式:_____ ;
②Z离子的结构示意图:_____
(3)由M、X、Y三种元素组成的化合物可通过电解饱和食盐水制得,该反应的化学方程式为_______ 。该化合物含有的化学键为________ ,属于_______ (填“离子”或“共价”)化合物,它的电子式为______
(1)由此可以推知(填元素符号):M是
(2)用不同的化学符号表示下列离子的核外电子排布:
①Y离子的电子式:
②Z离子的结构示意图:
(3)由M、X、Y三种元素组成的化合物可通过电解饱和食盐水制得,该反应的化学方程式为
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】现有A、B、C、D、E、F六种短周期元素,它们的原子序数依次增大,A、D同主族,C与E同主族,D、E、F同周期,A、B的最外层电子数之和与C的最外层电子数相等, A能分别与B、C形成电子总数相等的分子,且A与C形成的化合物常温下为液态,A能分别与E、F形成电子总数相等的气体分子。请回答下列问题:
(1)F的元素符号为_________ ,E、F的简单离子中半径较大的是______ (填离子符号)。
(2)A、C、D三种元素组成的一种常见化合物,是氯碱工业的重要产品,该化合物电子式为__________ 。
(3)B、C简单氢化物中稳定性较强的是__________ (填分子式)。
(4)B与F两种元素形成的一种化合物分子,各原子均达8电子稳定结构,则该化合物的化学式为___________ ;B的简单氢化物与F的单质常温下可发生置换反应,请写出该反应的化学方程式:______________________ 。
(1)F的元素符号为
(2)A、C、D三种元素组成的一种常见化合物,是氯碱工业的重要产品,该化合物电子式为
(3)B、C简单氢化物中稳定性较强的是
(4)B与F两种元素形成的一种化合物分子,各原子均达8电子稳定结构,则该化合物的化学式为
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】X、Y、Z、D、E、F是原子序数依次增大的六种常见元素。E的单质在Z2中燃烧的产物可使品红溶液褪色。F和Z元素形成的化合物F3Z4具有磁性。X的单质在Z2中燃烧可生成XZ和XZ2两种气体。D的单质是一种金属,该金属在XZ2中剧烈燃烧生成黑、白两种固体。请回答下列问题:
(1)F元素在周期表中的位置是________ ,Y的单质分子的结构式为__________ ,DZ的电子式为________ ,DZ化合物中离子半径较大的是________ (填离子符号)。
(2)X元素形成的同素异形体的晶体类型可能是________ (填序号)。
①原子晶体 ②离子晶体 ③金属晶体 ④分子晶体
(3)X、Y、Z形成的10电子氢化物中,X、Y的氢化物沸点较低的是(写化学式):__________ ;Y、Z的氢化物分子结合H+能力较强的是(写化学式)________ 。
(4)下列可作为比较D和Na金属性强弱的依据是________ 。(填序号)
a.测两种元素单质的硬度和熔、沸点
b.比较两元素最高价氧化物对应的水化物溶液的碱性强弱
c.比较两种元素在氯化物中化合价的高低
d.比较单质与同浓度盐酸反应的剧烈程度
(5)Y的氢化物和Z的单质在一定条件下反应生成Z的氢化物(产物之一),该反应的方程式为___________ 。
(6)有人建议将氢元素排在元素周期表的ⅣA族,请你从化合价的角度给出一个理由__________ 。
(1)F元素在周期表中的位置是
(2)X元素形成的同素异形体的晶体类型可能是
①原子晶体 ②离子晶体 ③金属晶体 ④分子晶体
(3)X、Y、Z形成的10电子氢化物中,X、Y的氢化物沸点较低的是(写化学式):
(4)下列可作为比较D和Na金属性强弱的依据是
a.测两种元素单质的硬度和熔、沸点
b.比较两元素最高价氧化物对应的水化物溶液的碱性强弱
c.比较两种元素在氯化物中化合价的高低
d.比较单质与同浓度盐酸反应的剧烈程度
(5)Y的氢化物和Z的单质在一定条件下反应生成Z的氢化物(产物之一),该反应的方程式为
(6)有人建议将氢元素排在元素周期表的ⅣA族,请你从化合价的角度给出一个理由
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】已知X、Y、Z、M、G、Q是六种短周期主族元素,原子序数依次增大。X、Z、Q的单质在常温下呈气态;Y的原子最外层电子数是其电子层数的2倍;X与M同主族;Z、G分别是地壳中含量最高的非金属元素和金属元素。请回答下列问题:
(1)Y、Z、M、G四种元素原子半径由大到小的顺序是______ (写元素符号);
(2)Z在元素周期表中的位置为____ ;
(3)上述元素的最高价氧化物对应的水化物中,酸性最强的水化物是____ (写化学式);
(4)X与Y能形成多种化合物,其中既含极性键又含非极性键,且它的产量可以用来衡量一个国家的石油化工发展水平的是______ (写名称);
(5)GQ3溶液与过量的MZX溶液反应的化学方程式为______________ ;
(6)常温下,不能与G的单质发生反应的是___ (填标号);
a CuSO4溶液 b 浓硫酸 c NaOH溶液 d 浓硝酸 e 氧化铜
(1)Y、Z、M、G四种元素原子半径由大到小的顺序是
(2)Z在元素周期表中的位置为
(3)上述元素的最高价氧化物对应的水化物中,酸性最强的水化物是
(4)X与Y能形成多种化合物,其中既含极性键又含非极性键,且它的产量可以用来衡量一个国家的石油化工发展水平的是
(5)GQ3溶液与过量的MZX溶液反应的化学方程式为
(6)常温下,不能与G的单质发生反应的是
a CuSO4溶液 b 浓硫酸 c NaOH溶液 d 浓硝酸 e 氧化铜
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】下表列出了部分前20号元素的一些性质:
下列问题用元素符号及化学式回答:
(1)②在周期表中的位置是___________ 。
(2)①与③以原子个数比1:1形成的化合物中含有
A.离子键 B.非极性键 C.极性键
(3)①②③组成的化合物电子式为___________ 。由①⑨组成的分子中,共含有18e-的化合物结构式为___________ 。
(4)⑥、⑦、⑩元素非金属性由强至弱顺序为___________ 。
(5)某元素X,原子半径为1.02×10-l0m,X的一种氧化物与⑦单质的水溶液反应生成两种强酸的离子方程式为___________ 。
元素编号 元素性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
| 原子半径(10-10m) | 0.37 | 2.27 | 0.74 | 1.52 | 0.77 | 1.10 | 0.99 | 1.86 | 0.75 | 0.71 |
| 最高价态 | +1 | +1 | - | +1 | +4 | +5 | +7 | +1 | - | |
| 最低价态 | -1 | - | -2 | - | -4 | -3 | -1 | - | -1 |
(1)②在周期表中的位置是
(2)①与③以原子个数比1:1形成的化合物中含有
A.离子键 B.非极性键 C.极性键
(3)①②③组成的化合物电子式为
(4)⑥、⑦、⑩元素非金属性由强至弱顺序为
(5)某元素X,原子半径为1.02×10-l0m,X的一种氧化物与⑦单质的水溶液反应生成两种强酸的离子方程式为
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】有A、B、C、D、E、F六种元素,原子序数依次增大,A、B、C、D、E均为短周期元素,A元素原子核内只有一个质子,元素A与B形成的气态化合物甲在标准状况下的密度为0.759g•L-1,C元素原子的最外层电子数是其电子层数的3倍,E与C同主族.均含D元素的乙(金属阳离子)、丙、丁微粒间的转化全为非氧化还原反应:均含F元素的乙(单质)、丙、丁微粒间的转化全为氧化还原反应.
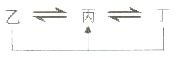
请回答下列问题:
(1)单质B的结构式:________________________ 。
(2)F元素周期表中的位置:_______________________ 。
(3)均含有F元素的乙与丁在溶液中发生反应的离子方程式___________________ ;均含有D元素的乙与丁在溶液中发生反应的离子方程式________________________ 。
(4)由A、C元素组成化合物良和A、E元素组成的化合物辛,式量均为34.其中庚的溶沸点比辛_______ (填“高”或“低”),原因是_________________ 。

请回答下列问题:
(1)单质B的结构式:
(2)F元素周期表中的位置:
(3)均含有F元素的乙与丁在溶液中发生反应的离子方程式
(4)由A、C元素组成化合物良和A、E元素组成的化合物辛,式量均为34.其中庚的溶沸点比辛
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】甲、乙、丙、丁为原子序数依次增大的短周期元素。甲、丙处于同一主族,丙、丁处于同一周期,甲的原子半径是整个周期表中最小,丁原子的最外层电子数是甲、乙、丙原子最外层电子数之和。乙的气态氢化物X与其最高价氧化物的水化物能发生反应生成化合物Y。
(1)丙离子的结构示意图为________ .甲和丙可形成化合物,该化合物为____ (填“离子”或“共价”)化合物。用电子式表示该化合物的形成过程:____________ 。
(2)写出乙单质的电子式:_____________ 。以上四种元素原子的半径从大到小的顺序为______ (填具体的元素符号)。
(3)Y中含有的化学键有_____________ 。
(4)丁所在的族各元素的氢化物中:沸点最低的是_______ (填化学式),其中的某氢化物的水溶液不能用玻璃瓶贮存,用化学方程式解释其原因_________________
(5)已知丁的单质与一定量的X在一定条件下能反应生成乙的单质,同时生成两种化合物W和Z, W是一种盐,Z是一种强酸,若W和Z的物质的量之比为2 : 4,写出丁的单质与X反应的化学方程式:_____________ 。
(1)丙离子的结构示意图为
(2)写出乙单质的电子式:
(3)Y中含有的化学键有
(4)丁所在的族各元素的氢化物中:沸点最低的是
(5)已知丁的单质与一定量的X在一定条件下能反应生成乙的单质,同时生成两种化合物W和Z, W是一种盐,Z是一种强酸,若W和Z的物质的量之比为2 : 4,写出丁的单质与X反应的化学方程式:
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】几种短周期元素的原子半径及主要化合价如下表: (请用化学用语答题)
(1) M在元素周期表中的位置为_____________ 。
(2)X与Y按原子个数比1∶1构成的物质的电子式为____ ;所含化学键类型______
(3)X+、 Y2-、M2-、R3+离子半径大小顺序为__________ 。
(4) 写出Z元素气态氢化物的形成过程___________ 。
(5)将YM2通入FeCl3溶液中的离子方程式:______
| 元素代号 | X | Y | Z | M | R |
| 原子半径/nm | 0.186 | 0.102 | 0.075 | 0.074 | 0.143 |
| 主要化合价 | +1 | +6 -2 | +5 -3 | -2 | +3 |
(2)X与Y按原子个数比1∶1构成的物质的电子式为
(3)X+、 Y2-、M2-、R3+离子半径大小顺序为
(4) 写出Z元素气态氢化物的形成过程
(5)将YM2通入FeCl3溶液中的离子方程式:
您最近半年使用:0次



