x、y、z、w、u为前20号元素中的五种,在一定条件下组成的单质及其化合物有如图所示转化关系。其中H、I、G为固体,F为液体,其他为气体。G由w- 和u2+ 两种具有相同电子构型的离子构成,是实验室常用的干燥剂。 回答下列问题:
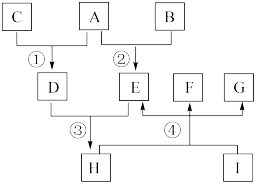
(1)G的电子式是___________
(2)在实验室中检验气体E的的简单方法是___________
(3)写出实验室中加热混合物的方法制备C的反应的离子方程式:___________
(4)写出反应④的化学方程式___________
(5)一定量E、C混合恰好完全反应且产生白烟,则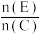 的范围为
的范围为___________

(1)G的电子式是
(2)在实验室中检验气体E的的简单方法是
(3)写出实验室中加热混合物的方法制备C的反应的离子方程式:
(4)写出反应④的化学方程式
(5)一定量E、C混合恰好完全反应且产生白烟,则
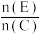 的范围为
的范围为
更新时间:2021-01-05 23:32:58
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】有关物质的转化关系如下图所示(部分物质与条件已略去)。A是最常见的无色液体,B、C是常见的金属单质,D、E是气体单质,且D在空气中的含量最多,F是一种具有磁性的化合物,H是既能与强酸反应又能与强碱反应的氧化物;I具有耐高温、抗冲击、导热性好的优良性质,广泛应用于电子工业、陶瓷工业中。
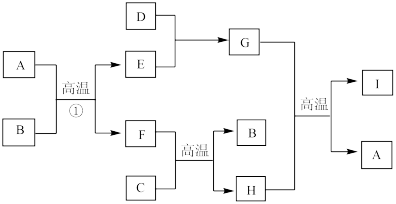
请回答下列问题:
(1) H的化学式为________________ 。
(2) D的电子式为________________ 。
(3) 写出反应①的化学方程式:________________ 。
(4) 写出G的水溶液与C的硝酸盐溶液反应的离子方程式:________________ 。

请回答下列问题:
(1) H的化学式为
(2) D的电子式为
(3) 写出反应①的化学方程式:
(4) 写出G的水溶液与C的硝酸盐溶液反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】Ⅰ.化学试剂的妥善保存十分重要,共价化合物A由三种常见的短周期元素组成,常温常压下是一种有特殊气味的无色液体,易与强氧化剂反应,实验室必须率封避光保存。按以下流程进行实验(以下反应都为充分反应,气体F溶于水部分忽略不计);

(1)组成A的元素的元素符号为___________ ;G的化学式为___________ 。
(2)液体A反应生成B和C的化学方程式为___________ 。
Ⅱ.Na2S2O3,又名大苏打、海波,可用以除去自来水中的多余氯气,在实验室可以用新制氯水模拟含多余氯气的自来水,向新制氯水中滴入Na2S2O3溶液。
(3)新制氯水与Na2S2O3溶液反应的离子方程式为___________ 。
(4)新制氯水中的氯气被全部除尽后,如果继续滴入Na2S2O3溶液有可能发生反应的离子方程式为___________ 。

(1)组成A的元素的元素符号为
(2)液体A反应生成B和C的化学方程式为
Ⅱ.Na2S2O3,又名大苏打、海波,可用以除去自来水中的多余氯气,在实验室可以用新制氯水模拟含多余氯气的自来水,向新制氯水中滴入Na2S2O3溶液。
(3)新制氯水与Na2S2O3溶液反应的离子方程式为
(4)新制氯水中的氯气被全部除尽后,如果继续滴入Na2S2O3溶液有可能发生反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】已知B为淡黄色的固体,M为生活中最常见的液体,气体乙为空气中的主要成分,物质A、B、C、D、E的焰色试验颜色都为黄色,回答下列问题

(1)用化学式表示下列物质:物质C为___________ ,气体甲为___________ ,气体丙为___________ 。
(2)物质E转化为D的化学方程式为___________ ,物质A和物质M反应的化学方程式为___________ ,物质B可以作为呼吸面具所用的药品,其反应原理为(用化学方程式表示)___________ 。
(3)C的水溶液可以和硫酸铜溶液反应,其离子方程式为___________ 。
(4)下列方法或试剂可以用来鉴别物质D和物质E的是___________ :
A.氯化钙溶液 B.澄清石灰水 C.加热

(1)用化学式表示下列物质:物质C为
(2)物质E转化为D的化学方程式为
(3)C的水溶液可以和硫酸铜溶液反应,其离子方程式为
(4)下列方法或试剂可以用来鉴别物质D和物质E的是
A.氯化钙溶液 B.澄清石灰水 C.加热
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】四种短周期元素的性质或结构信息如下表。请根据信息回答下列问题。
(1)写出元素T的离子结构示意图____________ ;写出元素X的气态氢化物的电子式________ ;写出Z元素原子的原子结构示意图:____________ ;元素Y的最高价氧化物对应水化物的电子式______ 。
(2)Z单质与Y最高价氧化物的水化物的水溶液反应的离子方程式__________________ 。
(3) 元素T与氟元素相比,非金属性较强的是___________ (用元素符号表示),下列表述中能证明这一事实的是______ 。
a.常温下氟气的颜色比T单质的颜色深
b.氟气与T的氢化物剧烈反应,产生T的单质
c.氟与T形成的化合物中T元素呈正价态
d.比较两元素的单质与氢气化合时得电子的数目
| 元素 | T | X | Y | Z |
| 性质结构信息 | 人体内含量最多的元素,且其单质是常见的助燃剂。 | 单质为双原子分子,分子中含有3对共用电子对,常温下单质气体性质稳定,但其原子较活泼 | 单质质软、银白色固体、导电性强。单质在空气中燃烧发出黄色的火焰。 | 第三周期元素的简单离子中半径最小 |
(1)写出元素T的离子结构示意图
(2)Z单质与Y最高价氧化物的水化物的水溶液反应的离子方程式
(3) 元素T与氟元素相比,非金属性较强的是
a.常温下氟气的颜色比T单质的颜色深
b.氟气与T的氢化物剧烈反应,产生T的单质
c.氟与T形成的化合物中T元素呈正价态
d.比较两元素的单质与氢气化合时得电子的数目
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】原子序数由小到大排列的四种短周期元素X、Y、Z、W,其中X、Z、W与氢元素可组成XH3、H2Z和HW型共价化合物;Y与氧元素可组成Y2O和Y2O2型离子化合物。
(1)写出Y2O2的电子式:________ ,其中含有的化学键是________ 。
(2)用电子式表示Y2O的形成过程:____________________________ 。
(3)X、Z、W三种元素的最高价氧化物对应的水化物中,酸性最强的是________ (填化学式)。
(4)由X、W组成的化合物分子中,X、W原子的最外层均达到8电子稳定结构,该化合物的化学式为_________________________________________
(1)写出Y2O2的电子式:
(2)用电子式表示Y2O的形成过程:
(3)X、Z、W三种元素的最高价氧化物对应的水化物中,酸性最强的是
(4)由X、W组成的化合物分子中,X、W原子的最外层均达到8电子稳定结构,该化合物的化学式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】下表列出了 九种元素在周期表中的位置。
九种元素在周期表中的位置。
请按要求回答下列问题:
(1)由 和
和 两种元素组成的相对分子质量为
两种元素组成的相对分子质量为 的化合物的电子式为
的化合物的电子式为_______ ;由 和
和 两种元素组成的化合物中化学键类型
两种元素组成的化合物中化学键类型_______ 。
(2) 、
、 、
、 三种元素的原子半径由大到小的顺序是
三种元素的原子半径由大到小的顺序是_______  填元素符号
填元素符号 。
。
(3)元素 、
、 、
、 分别与元素
分别与元素 组成含
组成含 个电子的分子化学式为
个电子的分子化学式为_______ 、_______ 、_______ 。
(4) 和
和 两种元素的最高价氧化物对应的水化物中碱性强的是
两种元素的最高价氧化物对应的水化物中碱性强的是_______  填化学式
填化学式 。
。
(5)元素 的气态氢化物比元素
的气态氢化物比元素 的气态氢化物的稳定性
的气态氢化物的稳定性_______  填“强”或“弱”
填“强”或“弱” 。
。
(6)元素 的最高价氧化物对应的水化物与元素
的最高价氧化物对应的水化物与元素 的最高价氧化物反应,其离子方程式
的最高价氧化物反应,其离子方程式_______ 。
 九种元素在周期表中的位置。
九种元素在周期表中的位置。Ⅰ |  | |||||||
 |  | Ⅱ | Ⅲ | Ⅳ | Ⅴ | Ⅵ | Ⅶ | |
 |  |  |  | |||||
 |  |  |  |  |  | |||
(1)由
 和
和 两种元素组成的相对分子质量为
两种元素组成的相对分子质量为 的化合物的电子式为
的化合物的电子式为 和
和 两种元素组成的化合物中化学键类型
两种元素组成的化合物中化学键类型(2)
 、
、 、
、 三种元素的原子半径由大到小的顺序是
三种元素的原子半径由大到小的顺序是 填元素符号
填元素符号 。
。(3)元素
 、
、 、
、 分别与元素
分别与元素 组成含
组成含 个电子的分子化学式为
个电子的分子化学式为(4)
 和
和 两种元素的最高价氧化物对应的水化物中碱性强的是
两种元素的最高价氧化物对应的水化物中碱性强的是 填化学式
填化学式 。
。(5)元素
 的气态氢化物比元素
的气态氢化物比元素 的气态氢化物的稳定性
的气态氢化物的稳定性 填“强”或“弱”
填“强”或“弱” 。
。(6)元素
 的最高价氧化物对应的水化物与元素
的最高价氧化物对应的水化物与元素 的最高价氧化物反应,其离子方程式
的最高价氧化物反应,其离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】A、B、C、D、E五种短周期主族元素的原子序数依次增大。A原子的最外层电子数比B原子的最外层电子数少2,B原子的质子数是其电子层数的4倍;A、B、C三种元素能结合成化合物 ,在
,在
 中共有
中共有 电子。
电子。 D的单质与足量酸完全反应时,转移
D的单质与足量酸完全反应时,转移 个电子。E的单质是一种黄绿色气体,且其水溶液具有漂白性。试填写下列空白:
个电子。E的单质是一种黄绿色气体,且其水溶液具有漂白性。试填写下列空白:
(1)B在周期表中的位置为________________ 。
(2)C、D、E形成的简单离子的半径由大到小的顺序为________ (用离子符号表示)。
(3)门捷列夫在研究周期表时曾预言了包括“类铝”“类硅”在内的11种元素。门捷列夫曾预言的“类硅”,多年后被德国化学家文克勒发现,命名为Ge。已知主族元素Ge的最高化合价为+4,其最高价氧化物的水化物为两性氢氧化物。若Ge位于Si的下一周期,根据Ge在周期表中处于金属和非金属分界线附近,预测锗单质的一种可能的用途是________ ;硅和锗单质分别与 反应时反应较难进行的是
反应时反应较难进行的是________ (填“硅单质”或“锗单质”)。
 ,在
,在
 中共有
中共有 电子。
电子。 D的单质与足量酸完全反应时,转移
D的单质与足量酸完全反应时,转移 个电子。E的单质是一种黄绿色气体,且其水溶液具有漂白性。试填写下列空白:
个电子。E的单质是一种黄绿色气体,且其水溶液具有漂白性。试填写下列空白:(1)B在周期表中的位置为
(2)C、D、E形成的简单离子的半径由大到小的顺序为
(3)门捷列夫在研究周期表时曾预言了包括“类铝”“类硅”在内的11种元素。门捷列夫曾预言的“类硅”,多年后被德国化学家文克勒发现,命名为Ge。已知主族元素Ge的最高化合价为+4,其最高价氧化物的水化物为两性氢氧化物。若Ge位于Si的下一周期,根据Ge在周期表中处于金属和非金属分界线附近,预测锗单质的一种可能的用途是
 反应时反应较难进行的是
反应时反应较难进行的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】X、Y、Z、Q、R是五种短周期元素,原子序数依次增大,X元素的一种核素核内无中子,Y元素最高正价与最低负价之和为0,Q与X同主族,Z、R分别是地壳中含量最高的非金属元素和金属元素,请回答下列问题:
(1)五种元素原子半径由大到小的顺序是(写元素符号):_____ ;
(2)由以上某些元素组成的化合物A、B、C、D有如下转化关系: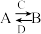 (在水溶液中进行)其中C是溶于水显酸性的气体;D是淡黄色固体。
(在水溶液中进行)其中C是溶于水显酸性的气体;D是淡黄色固体。
①写出C的结构式_____ ;D的电子式_____ ;
②如果A、B均由三种元素组成,B为两性不溶物,则A的化学式为_____ ;由A转化为B的离子方程式_________________ ;
③如果A由三种元素组成,B由四种元素组成,则相同条件下,同浓度的溶液碱性更强的是________________ (填化学式)。
(1)五种元素原子半径由大到小的顺序是(写元素符号):
(2)由以上某些元素组成的化合物A、B、C、D有如下转化关系:
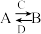 (在水溶液中进行)其中C是溶于水显酸性的气体;D是淡黄色固体。
(在水溶液中进行)其中C是溶于水显酸性的气体;D是淡黄色固体。①写出C的结构式
②如果A、B均由三种元素组成,B为两性不溶物,则A的化学式为
③如果A由三种元素组成,B由四种元素组成,则相同条件下,同浓度的溶液碱性更强的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图所示。已知W的一种核素的质量数为18,中子数为10;X和Ne的核外电子数相差1;在Z所在的周期中,Z元素的原子得电子能力最强;四种元素的最外层电子数之和为18。请回答:

(1)Y元素位于元素周期表中位置为___________ 。
(2)X的单质和Y的单质相比,熔点较低的是___________ (写化学式)。Z所在族的简单氢化物中,沸点最高的是___________ (写化学式),原因为___________ 。
(3)W、X、Z三种元素1:1:1形成的化合物的电子式为___________ 。
(4)Y与Z形成的化合物在常温下是一种液态,它和足量水反应,生成一种弱酸和一种强酸,该反应的化学方程式为___________ 。
(5)Z的氧化物很多,其中一种黄绿色气体M,其氧含量为47.41%,可用于水处理,M在液态和浓缩气态时具有爆炸性,则M的化学式为___________ 。M可与NaOH溶液反应生成两种稳定的盐,它们的物质的量之比为1︰5,该反应的化学方程式为___________ 。

(1)Y元素位于元素周期表中位置为
(2)X的单质和Y的单质相比,熔点较低的是
(3)W、X、Z三种元素1:1:1形成的化合物的电子式为
(4)Y与Z形成的化合物在常温下是一种液态,它和足量水反应,生成一种弱酸和一种强酸,该反应的化学方程式为
(5)Z的氧化物很多,其中一种黄绿色气体M,其氧含量为47.41%,可用于水处理,M在液态和浓缩气态时具有爆炸性,则M的化学式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】如表是a~m九种元素在周期表中的位置,请回答下列问题:

(1)m的阴离子结构示意图为____________ 。
(2)b的最高价氧化物的电子式为____________ ;用电子式表示f2 d2的形成过程_______________________ 。
(3)d、g、n形成的简单离子的半径由大到小的顺序为___________ (用离子符号填写)。
(4)f、g、p的最高价氧化物的水化物碱性从强到弱的顺序为__________ (填化学式)。
(5)p和n两种元素最高价氧化物的水化物相互反应的化学反应方程式为___________ 。
(6)c的氢化物和c的最高价氧化物对应水化物之间反应的化学方程式为__________ 。
(7)k的氧化物与氢氧化钠溶液反应的离子方程式为________________________ 。
(8)以上元素组成的物质有下列框图中的转化关系,其中甲为10电子微粒。
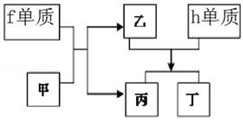
①丁属于_____________ (选填“离子化合物”或“共价化合物”)。
②请写出h单质与乙反应的化学方程式_____________ 。

(1)m的阴离子结构示意图为
(2)b的最高价氧化物的电子式为
(3)d、g、n形成的简单离子的半径由大到小的顺序为
(4)f、g、p的最高价氧化物的水化物碱性从强到弱的顺序为
(5)p和n两种元素最高价氧化物的水化物相互反应的化学反应方程式为
(6)c的氢化物和c的最高价氧化物对应水化物之间反应的化学方程式为
(7)k的氧化物与氢氧化钠溶液反应的离子方程式为
(8)以上元素组成的物质有下列框图中的转化关系,其中甲为10电子微粒。

①丁属于
②请写出h单质与乙反应的化学方程式
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】A、B、C、D四种元素处于同一短周期,在同族元素中,A的气态氢化物的沸点最高,B的最高价氧化物对应的水化物的酸性在同周期中是最强的,C的电负性介于A、B之间,D与B相邻。
(1)C的原子的价电子排布式为___________ 。
(2)在B的单质分子中存在___________ 个π键,___________ 个σ键。
(3)已知B的气态氢化物很容易与H+结合,B的气态氢化物分子与 H+形成的离子立体构型为___________ 。
(4)在A、B、C、D四种元素形成的电子数相同的四种氢化物中沸点最低的是___________ (写分子式),其沸点显著低于其他三种氢化物的原因是: ___________ 。
(1)C的原子的价电子排布式为
(2)在B的单质分子中存在
(3)已知B的气态氢化物很容易与H+结合,B的气态氢化物分子与 H+形成的离子立体构型为
(4)在A、B、C、D四种元素形成的电子数相同的四种氢化物中沸点最低的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】四种短周期元素A、B、C、D,原子序数依次增大,A原子的最外电子层上有4个电子;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体E;D的L层电子数等于K、M两个电子层上电子数之和。
(1)A元素最高价氧化物的电子式为_________ ,D元素的某种核素中质子数和中子数相等,该核素组成符号为_______ 。
(2)化合物E中存在的化学键类型为_________ 。
(3)A、B、C的原子半径从大到小的顺序__________________ 。(用对应原子符号表示);B、C、D 的简单离子的半径从大到小的顺序__________________ 。(用对应的离子符号表示)
(1)A元素最高价氧化物的电子式为
(2)化合物E中存在的化学键类型为
(3)A、B、C的原子半径从大到小的顺序
您最近一年使用:0次



