海洋是巨大的资源宝库。大连市充分利用沿海优势,优先发展海水淡化生 产与综合利用一体化绿色循环经济产业,逐步建立起较为完善的海水淡化产业链,全 面推动海水淡化相关技术研发、装备制造、原材料生产和盐化工等产业集聚发展。
Ⅰ.从海水中提取食盐和溴的过程如下:

(1)海水淡化的方法主要有蒸馏法、_________________ 等(写出一种即可)。
(2)步骤Ⅰ中已获得 Br2,步骤Ⅱ中又将 Br2 还原为 Br-,其目的为_____________ 。
(3)步骤Ⅱ用 SO2水溶液吸收 Br2,吸收率可达 95%,有关反应的离子方程式为_____ ;由此反应可知,除环境保护外,在该工业生产中应解决的主要问题是________ 。
(4)步骤Ⅲ蒸馏过程中,温度应控制在 80~90 ℃。温度过高或过低都不利于生产, 若温度过高,大量水蒸气随溴排出,溴蒸气中水分增加;若温度过低,则_____________________________ 。
Ⅱ.某化学研究性学习小组模拟工业上从浓缩的海水中提取液溴的过程,设计了如下 实验装置(夹持装置略去)和操作流程。已知:Br2的沸点为 59 ℃,微溶于水,有毒。
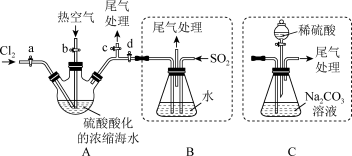
①连接 A 与 B,关闭活塞 b、d,打开活塞 a、c,向 A 中缓慢通入 Cl2 至反应完全;
②关闭活塞 a、c,打开活塞 b、d,向 A 中鼓入足量热空气;
③进行步骤②的同时,向 B 中通入足量 SO2;
④关闭活塞 b,打开活塞 a,再通过 A 向 B 中缓慢通入足量 Cl2;
⑤将 B 中所得液体进行萃取、分液,蒸馏并收集液溴。 请回答下列问题:
(1)步骤②中鼓入热空气的作用是_______________________________ 。
(2)进行步骤③时,B 中尾气可用___________________ (填字母)吸收处理。
a.水 b.浓硫酸 c.NaOH 溶液 d.饱和 NaCl 溶液
(3)若直接连接 A 与 C,进行步骤①和②,充分反应后,向锥形瓶中滴加稀硫酸, 再经步骤⑤,也能制得液溴。滴加稀硫酸之前,C 中反应生成了 NaBrO3、NaBr、CO2,则该反应的化学方程式为____________________ 。
(4)与 B 装置相比,采用 C 装置的优点为___________________________ 。
Ⅰ.从海水中提取食盐和溴的过程如下:

(1)海水淡化的方法主要有蒸馏法、
(2)步骤Ⅰ中已获得 Br2,步骤Ⅱ中又将 Br2 还原为 Br-,其目的为
(3)步骤Ⅱ用 SO2水溶液吸收 Br2,吸收率可达 95%,有关反应的离子方程式为
(4)步骤Ⅲ蒸馏过程中,温度应控制在 80~90 ℃。温度过高或过低都不利于生产, 若温度过高,大量水蒸气随溴排出,溴蒸气中水分增加;若温度过低,则
Ⅱ.某化学研究性学习小组模拟工业上从浓缩的海水中提取液溴的过程,设计了如下 实验装置(夹持装置略去)和操作流程。已知:Br2的沸点为 59 ℃,微溶于水,有毒。

①连接 A 与 B,关闭活塞 b、d,打开活塞 a、c,向 A 中缓慢通入 Cl2 至反应完全;
②关闭活塞 a、c,打开活塞 b、d,向 A 中鼓入足量热空气;
③进行步骤②的同时,向 B 中通入足量 SO2;
④关闭活塞 b,打开活塞 a,再通过 A 向 B 中缓慢通入足量 Cl2;
⑤将 B 中所得液体进行萃取、分液,蒸馏并收集液溴。 请回答下列问题:
(1)步骤②中鼓入热空气的作用是
(2)进行步骤③时,B 中尾气可用
a.水 b.浓硫酸 c.NaOH 溶液 d.饱和 NaCl 溶液
(3)若直接连接 A 与 C,进行步骤①和②,充分反应后,向锥形瓶中滴加稀硫酸, 再经步骤⑤,也能制得液溴。滴加稀硫酸之前,C 中反应生成了 NaBrO3、NaBr、CO2,则该反应的化学方程式为
(4)与 B 装置相比,采用 C 装置的优点为
更新时间:2020-07-22 18:52:34
|
相似题推荐
解答题-实验探究题
|
较难
(0.4)
名校
【推荐1】海带中含有丰富的碘,为了从海带中提取碘,某研究性学习小组设计并进行以下实验:

请填写下列空白:
(1)步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器是__________ (从下列仪器中选出所需仪器,用标号字母填写在空白处);
A.烧杯 B.坩埚 C.表面皿 D.泥三角 E.酒精灯 F.干燥器
(2)步骤③的实验操作名称是_____________ ;
(3)写出步骤④的离子反应方程式(已知MnO2生成Mn2+和H2O )__________________ ;
(4)步骤⑤中,某学生选择用苯来提取碘的理由是______________________________ , 还可选用_____________________ (写试剂的化学式)来提取碘,该步骤所用主要玻璃仪器的名称是__________________________ 。
(5)步骤⑥的目的是从含碘苯溶液中分离出单质碘,同时回收苯,该步骤的实验操作名称是__________________ 。

请填写下列空白:
(1)步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器是
A.烧杯 B.坩埚 C.表面皿 D.泥三角 E.酒精灯 F.干燥器
(2)步骤③的实验操作名称是
(3)写出步骤④的离子反应方程式(已知MnO2生成Mn2+和H2O )
(4)步骤⑤中,某学生选择用苯来提取碘的理由是
(5)步骤⑥的目的是从含碘苯溶液中分离出单质碘,同时回收苯,该步骤的实验操作名称是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐2】海洋约占地球表面积的71%,海水化学资源的利用具有非常广阔的前景.
(1)海水晒盐可获得粗盐,在实验室中粗盐经过溶解、________ 、________ 可制得精盐。(填具体操作名称)
(2)镁及其合金是一种用途很广的金属材料,目前世界上60%的镁是从海水中提取的,其主要步骤如下:
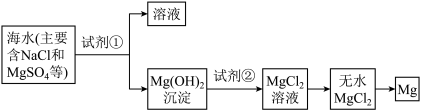
①为了使MgSO4转化为Mg(OH)2 , 试剂①可以选用________ 。
②试从节约能源、提高金属镁的纯度分析,以下适宜的冶镁方法是________ 。
A.Mg(OH)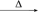 MgO
MgO Mg B.Mg(OH)
Mg B.Mg(OH)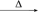 MgO
MgO Mg
Mg
C.Mg(OH)2 MgCl2
MgCl2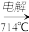 Mg D.Mg(OH)2
Mg D.Mg(OH)2 MgCl2
MgCl2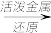 Mg
Mg
(3)溴及其化合物用途十分广泛,我国正在大力开展海水提溴的研究和开发工作。工业以浓缩海水为原料提取溴的部分过程如下:
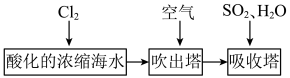
某课外小组在实验室模拟上述过程设计以下装置进行实验(所有橡胶制品均已被保护,夹持装置已略去):

①A装置中通入a气体的目的是(用离子方程式表示)______________________________ ;
②A装置中通入a气体一段时间后,停止通入,改通热空气.通入热空气的目的是___________ ;
③反应过程中,B装置中有SO42﹣生成,检验SO42﹣的方法是____________________________ ;
④C装置的作用是______________________________________________ 。
(1)海水晒盐可获得粗盐,在实验室中粗盐经过溶解、
(2)镁及其合金是一种用途很广的金属材料,目前世界上60%的镁是从海水中提取的,其主要步骤如下:

①为了使MgSO4转化为Mg(OH)2 , 试剂①可以选用
②试从节约能源、提高金属镁的纯度分析,以下适宜的冶镁方法是
A.Mg(OH)
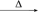 MgO
MgO Mg B.Mg(OH)
Mg B.Mg(OH)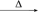 MgO
MgO Mg
MgC.Mg(OH)2
 MgCl2
MgCl2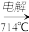 Mg D.Mg(OH)2
Mg D.Mg(OH)2 MgCl2
MgCl2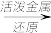 Mg
Mg(3)溴及其化合物用途十分广泛,我国正在大力开展海水提溴的研究和开发工作。工业以浓缩海水为原料提取溴的部分过程如下:

某课外小组在实验室模拟上述过程设计以下装置进行实验(所有橡胶制品均已被保护,夹持装置已略去):

①A装置中通入a气体的目的是(用离子方程式表示)
②A装置中通入a气体一段时间后,停止通入,改通热空气.通入热空气的目的是
③反应过程中,B装置中有SO42﹣生成,检验SO42﹣的方法是
④C装置的作用是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐3】海洋约占地球表面积的71%,海水中化学资源的利用具有非常广阔的前景。
(1)目前世界上60%的镁是从海水中提取的,其主要步骤如下:

① 试剂①宜选用石灰乳且必须过量,过量的目的是___________ 。
② 镁蒸气宜在___________ (填序号)气体冷却后得到镁锭
a.N2 B.CO2 C.Ar D.空气)
(2)工业以浓缩海水为原料提取溴的部分过程如下:

某课外小组在实验室模拟上述过程设计以下装置进行实验(所有橡胶制品均已被保护,夹持装置已略去):

③A装置中通入a气体时,反应的离子方程式表示为:___________ 。
④A装置中通入a气体一段时间后,停止通入,改通热空气。通入热空气的目的是:___________ 。
⑤反应过程中,B装置中产生的两种主要阴离子为___________ 。
⑥C装置的作用是___________ 。
(1)目前世界上60%的镁是从海水中提取的,其主要步骤如下:

① 试剂①宜选用石灰乳且必须过量,过量的目的是
② 镁蒸气宜在
a.N2 B.CO2 C.Ar D.空气)
(2)工业以浓缩海水为原料提取溴的部分过程如下:

某课外小组在实验室模拟上述过程设计以下装置进行实验(所有橡胶制品均已被保护,夹持装置已略去):

③A装置中通入a气体时,反应的离子方程式表示为:
④A装置中通入a气体一段时间后,停止通入,改通热空气。通入热空气的目的是:
⑤反应过程中,B装置中产生的两种主要阴离子为
⑥C装置的作用是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐1】液溴是中学化学中重要的化工原料,可用于制备溴苯等。以含NaBr的废液为原料回收溴的流程如下,回答下列问题:

已知:液溴的沸点为58.8℃。
(1)“氧化1”的还原剂是___________ (填离子符号)。从原子结构角度解释氯的非金属性比溴的强的原因:___________ 。
(2)“酸化”的目的是___________ 。
(3)“吸收”中发生反应的离子方程式为___________ 。
(4)“蒸馏”操作中的加热方式宜选择___________ 加热。
(5)除去粗溴中 的方法是___________(填标号)。
的方法是___________(填标号)。
(6)已知天然橡胶的主要成分为聚异戊二烯,结构为 。在实验室提纯溴时,用铝箔(或锡箔)包裹橡胶塞、玻璃管接口的橡胶管,这样做的目的是
。在实验室提纯溴时,用铝箔(或锡箔)包裹橡胶塞、玻璃管接口的橡胶管,这样做的目的是___________ 。

已知:液溴的沸点为58.8℃。
(1)“氧化1”的还原剂是
(2)“酸化”的目的是
(3)“吸收”中发生反应的离子方程式为
(4)“蒸馏”操作中的加热方式宜选择
(5)除去粗溴中
 的方法是___________(填标号)。
的方法是___________(填标号)。| A.加入NaOH溶液,过滤 | B.加入NaBr溶液,蒸馏 |
C.加入 ,萃取、分液 ,萃取、分液 | D.加入KI溶液,蒸馏 |
(6)已知天然橡胶的主要成分为聚异戊二烯,结构为
 。在实验室提纯溴时,用铝箔(或锡箔)包裹橡胶塞、玻璃管接口的橡胶管,这样做的目的是
。在实验室提纯溴时,用铝箔(或锡箔)包裹橡胶塞、玻璃管接口的橡胶管,这样做的目的是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】以下为工业从海水中提取液溴的流程图:

已知:溴的沸点为59℃,微溶于水.有毒性。请回答:
(1)某同学利用“图1”装置进行步骤①至步骤④的实验,当进行步骤①时,应关闭活塞_________ ,打开活塞_______ ,(a、b、c、d均为活塞)


图1 图2
(2)步骤③中当出现________ (填现象)时:判断反应完全。B中主要反应的离子方程式为_______
(3)从从“溴与水混合物Ⅰ”到“溴与水混合物Ⅱ”的目的是_______
(4)步骤⑤用"图2”装置进行蒸馏,该装置缺少的仪器是________ ,装置C中直接加热不合理,应改为_____ ,蒸馏时冷凝水应从_____ 端进入(填“e"或"f")。
(5)从海水中可以提取溴,但得到的液溴中常溶有少量氯气,除去氯气应该采用的方法是_______
A 加入适量的KI溶液 B 加入溴蒸气
C 加入适量的氢氧化钠溶液 D 加入适量的溴化钠溶液.

已知:溴的沸点为59℃,微溶于水.有毒性。请回答:
(1)某同学利用“图1”装置进行步骤①至步骤④的实验,当进行步骤①时,应关闭活塞


图1 图2
(2)步骤③中当出现
(3)从从“溴与水混合物Ⅰ”到“溴与水混合物Ⅱ”的目的是
(4)步骤⑤用"图2”装置进行蒸馏,该装置缺少的仪器是
(5)从海水中可以提取溴,但得到的液溴中常溶有少量氯气,除去氯气应该采用的方法是
A 加入适量的KI溶液 B 加入溴蒸气
C 加入适量的氢氧化钠溶液 D 加入适量的溴化钠溶液.
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐3】海洋中有丰富的食品、矿产、能源、药物和水产等资源,下图为海水综合利用的部分流程。

回答下列问题:
(1)为了除去粗盐中的 及泥沙,可将粗盐溶于水,然后进行下列五项操作: a.过滤;b.加过量
及泥沙,可将粗盐溶于水,然后进行下列五项操作: a.过滤;b.加过量 溶液;c.加适量盐酸;d.加过量
溶液;c.加适量盐酸;d.加过量 溶液;e.加过量
溶液;e.加过量 溶液。正确的操作顺序是_______→_______→_______→a→c
溶液。正确的操作顺序是_______→_______→_______→a→c___ 。(填字母)
(2)步骤③加入的试剂A是_______ ,然后进行的操作I是_______ 。
(3)步骤①~⑦中,涉及氧化还原反应的步骤有_______ 。
(4)步骤⑥的化学方程式为_______ 。
(5)步骤⑦的离子方程式为_______ 。
(6)将 海水浓缩至
海水浓缩至 ,使用上述流程中的生产方法最终得到
,使用上述流程中的生产方法最终得到 ,若
,若 的提取率为55%,则海水中溴的浓度为
的提取率为55%,则海水中溴的浓度为_______ 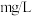 。(计算结果保留两位有效数字)
。(计算结果保留两位有效数字)

回答下列问题:
(1)为了除去粗盐中的
 及泥沙,可将粗盐溶于水,然后进行下列五项操作: a.过滤;b.加过量
及泥沙,可将粗盐溶于水,然后进行下列五项操作: a.过滤;b.加过量 溶液;c.加适量盐酸;d.加过量
溶液;c.加适量盐酸;d.加过量 溶液;e.加过量
溶液;e.加过量 溶液。正确的操作顺序是_______→_______→_______→a→c
溶液。正确的操作顺序是_______→_______→_______→a→c(2)步骤③加入的试剂A是
(3)步骤①~⑦中,涉及氧化还原反应的步骤有
(4)步骤⑥的化学方程式为
(5)步骤⑦的离子方程式为
(6)将
 海水浓缩至
海水浓缩至 ,使用上述流程中的生产方法最终得到
,使用上述流程中的生产方法最终得到 ,若
,若 的提取率为55%,则海水中溴的浓度为
的提取率为55%,则海水中溴的浓度为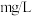 。(计算结果保留两位有效数字)
。(计算结果保留两位有效数字)
您最近一年使用:0次



