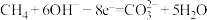有人设计出利用CH4和O2的反应,用铂电极在KOH溶液中构成原电池。电池的总反应类似于CH4在O2中燃烧,则下列说法不正确 的是
①每消耗1molCH4可以向外电路提供8mole-
②负极通CH4,电极反应式CH4+10OH--8e-= +7H2O
+7H2O
③正极上O2失去电子,电极反应式为O2+2H2O+4e-===4OH-
④电池放电后,溶液pH不断升高
①每消耗1molCH4可以向外电路提供8mole-
②负极通CH4,电极反应式CH4+10OH--8e-=
 +7H2O
+7H2O③正极上O2失去电子,电极反应式为O2+2H2O+4e-===4OH-
④电池放电后,溶液pH不断升高
| A.①② | B.①③ | C.①④ | D.③④ |
更新时间:2020-07-24 21:10:37
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】 电池在新能源汽车、航空航天、电子电气、轨道交通等领域应用前景非常广阔。一种
电池在新能源汽车、航空航天、电子电气、轨道交通等领域应用前景非常广阔。一种 电池模拟装置如图所示。下列说法正确的是
电池模拟装置如图所示。下列说法正确的是

 电池在新能源汽车、航空航天、电子电气、轨道交通等领域应用前景非常广阔。一种
电池在新能源汽车、航空航天、电子电气、轨道交通等领域应用前景非常广阔。一种 电池模拟装置如图所示。下列说法正确的是
电池模拟装置如图所示。下列说法正确的是
| A.离子交换膜M为阴离子交换膜 |
B.放电时, 极的还原产物为 极的还原产物为 |
C.充电时,电池的总反应为 |
| D.电解质溶液中溶剂可以是水、醇、羧酸等 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】铅蓄电池的工作原理为Pb+PbO2+2H2SO4 2PbSO4+2H2O。下图中a、b、c、d四个电极均为表面有覆盖层的石墨电极,下列判断错误的是
2PbSO4+2H2O。下图中a、b、c、d四个电极均为表面有覆盖层的石墨电极,下列判断错误的是
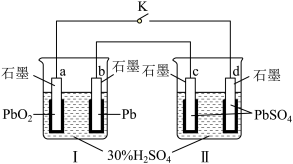
 2PbSO4+2H2O。下图中a、b、c、d四个电极均为表面有覆盖层的石墨电极,下列判断错误的是
2PbSO4+2H2O。下图中a、b、c、d四个电极均为表面有覆盖层的石墨电极,下列判断错误的是 
A.K闭合时,d极的电极反应式:PbSO4+2H2O-2e-=PbO2+4H++ |
| B.K闭合一段时间后,Ⅱ可单独作为原电池,c极为正极 |
C.K闭合时,Ⅱ中 向d极迁移 向d极迁移 |
| D.当电路中转移0.2 mol电子时,Ⅰ中消耗的H2SO4为0.2mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】羟胺(NH2OH)常用于有机合成。一种电化学法制取盐酸羟胺(NH3OHCl)的装置原理如下图所示,已知铁可作NO反应的催化剂。下列说法正确的是


| A.放电时Pt电极有Cl2生成 |
| B.放电时的正极反应式为NO+3e-+4H+=NH3OH+ |
| C.放电时,电路中每转移1mol eˉ,负极区将增加1mol H+ |
| D.将质子交换膜改成阴离子交换膜,放电时的电极反应将发生变化 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】一种新型太阳光电化学电池贮能时电解质溶液中离子在两极发生如图所示的转化。下列说法正确的是


| A.贮能时,电能转变为化学能和光能 |
| B.贮能和放电时,电子在导线中流向相同 |
| C.贮能时,氢离子由a极区迁移至b极区 |
D.放电时,b极发生:VO +2H++e-=VO2++H2O +2H++e-=VO2++H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】一种新型燃料电池,一极通入空气,另一极通入丁烷气体;电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在熔融状态下能传导O2-。下列有关该燃料电池的说法正确的是( )
| A.在熔融电解质中,O2-移向正极 |
| B.电池总反应式:2C4H10+13O2=8CO2+10H2O |
| C.通入空气的一极是负极,电极反应式为O2+4e-=2O2- |
| D.通入丁烷的一极是正极,电极反应式为C4H10+26e-+13O2-=4CO2+5H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】燃料电池一直是近年电池研究的热点,可作为汽车的能源。一种碱性天然气燃料电池的简易装置如图所示。下列说法错误的是

| A.a电极是负极,该电极上发生氧化反应 |
B.b电极上的反应式为 |
C.电池工作时,溶液中的 向a极移动 向a极移动 |
D.该电池能提高能量的利用率,且几乎不排放温室气体 |
您最近一年使用:0次



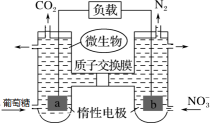
 +10e—+12H+=N2↑+6H2O
+10e—+12H+=N2↑+6H2O