(1)如图所示装置:
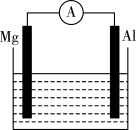
若烧杯中溶液为稀硫酸,则观察到的现象为_____________ 。
若烧杯中溶液为氢氧化钠溶液,则负极电极式是_____________ 。
(2)油脂在人体内的化学变化主要是在脂肪酶的催化下,进行水解,生成____________________ 。
(3)蛋白质的鉴别方法是_____________________________ 。
(4)淀粉的水解反应方程式是________________________ ,欲检验淀粉水解情况所需试剂是(水解液已调至碱性)_____________________ 。

若烧杯中溶液为稀硫酸,则观察到的现象为
若烧杯中溶液为氢氧化钠溶液,则负极电极式是
(2)油脂在人体内的化学变化主要是在脂肪酶的催化下,进行水解,生成
(3)蛋白质的鉴别方法是
(4)淀粉的水解反应方程式是
更新时间:2020-07-24 21:10:37
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
【推荐1】酸性锌锰干电池是一种一次电池,其结构如图所示。该电池在放电过程产生MnOOH和Zn(NH3)2Cl2。回答下列问题:

(1)电池反应的化学方程式为____ 。
(2)如图为电解500mL1mol/LCuSO4溶液的装置,该装置的电源为上述酸性锌锰干电池。当电池负极消耗16.25gZn时,电解后溶液的pH=____ (忽略电解前后溶液体积变化)。将电解后的溶液恢复至原溶液时,应加入的试剂是____ ,其质量为____ 。

(3)用该废电池的锌皮(含少量杂质铁)可制备化工原料ZnSO4•7H2O。其流程如图:

已知部分物质的Ksp如表:
①氧化时的离子方程式____ 。
②试剂X最好选用____ (填化学式),调pH的范围是____ (假定Zn2+浓度为0.1mol/L,离子浓度小于1×10-5mol/L时,即可认为该离子沉淀完全)。
③若上述流程中不加H2O2氧化的后果是____ ,原因是____ 。

(1)电池反应的化学方程式为
(2)如图为电解500mL1mol/LCuSO4溶液的装置,该装置的电源为上述酸性锌锰干电池。当电池负极消耗16.25gZn时,电解后溶液的pH=

(3)用该废电池的锌皮(含少量杂质铁)可制备化工原料ZnSO4•7H2O。其流程如图:

已知部分物质的Ksp如表:
| 化合物 | Zn(OH)2 | Fe(OH)2 | Fe(OH)3 |
| Ksp近似值 | 10-17 | 10-17 | 10-39 |
②试剂X最好选用
③若上述流程中不加H2O2氧化的后果是
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐2】I.铁是生产生活、科学研究中的重要物质,研究与Fe相关的反应时要关注反应的快慢和程度,某些有铁参与的反应可设计成原电池。
(1)以下是相同条件下,等体积等浓度的 溶液分解的对比实验时,放出
溶液分解的对比实验时,放出 的体积随时间的变化关系示意图(线a为使用
的体积随时间的变化关系示意图(线a为使用 作催化剂,线b为不使用催化剂),其中正确的图像是_______(填字母)。
作催化剂,线b为不使用催化剂),其中正确的图像是_______(填字母)。
Ⅱ.一定条件下铁可以和 发生反应
发生反应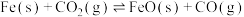 。一定温度下,向某密闭容器中加入足量铁粉并充入一定量的
。一定温度下,向某密闭容器中加入足量铁粉并充入一定量的 气体,反应过程中
气体,反应过程中 气体和CO气体的浓度变化与时间的关系如图所示。
气体和CO气体的浓度变化与时间的关系如图所示。
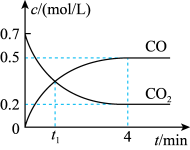
(2) min时,反应速率的大小关系为
min时,反应速率的大小关系为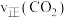
_______  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(3)0~4min内, 的转化率为
的转化率为_______ ,CO的平均反应速率
_______ 。
(4)仅改变下列条件,化学反应速率减小的_______(填字母)。
(5)下列选项能说明上述反应已达平衡状态的是_______(填字母)。
Ⅲ.某化学兴趣小组利用反应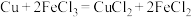 ,设计了如图所示的原电池装置。
,设计了如图所示的原电池装置。

(6)a是_______ 极(填“正”或“负”),发生_______ 反应(填“氧化”或“还原”),,可选_______ 作a极材料。
(7)外电路中,电流从_______ 极流出(填“a”或“b”)。
(8)写出b电极上的电极反应式_______ 。
(1)以下是相同条件下,等体积等浓度的
 溶液分解的对比实验时,放出
溶液分解的对比实验时,放出 的体积随时间的变化关系示意图(线a为使用
的体积随时间的变化关系示意图(线a为使用 作催化剂,线b为不使用催化剂),其中正确的图像是_______(填字母)。
作催化剂,线b为不使用催化剂),其中正确的图像是_______(填字母)。A.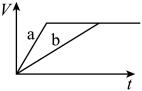 | B. |
C.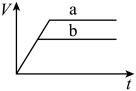 | D.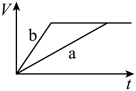 |
Ⅱ.一定条件下铁可以和
 发生反应
发生反应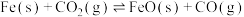 。一定温度下,向某密闭容器中加入足量铁粉并充入一定量的
。一定温度下,向某密闭容器中加入足量铁粉并充入一定量的 气体,反应过程中
气体,反应过程中 气体和CO气体的浓度变化与时间的关系如图所示。
气体和CO气体的浓度变化与时间的关系如图所示。
(2)
 min时,反应速率的大小关系为
min时,反应速率的大小关系为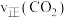
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(3)0~4min内,
 的转化率为
的转化率为
(4)仅改变下列条件,化学反应速率减小的_______(填字母)。
| A.减少铁粉的质量 | B.降低温度 |
| C.保持压强不变,充入He使容器的体积增大 | D.保持体积不变,充入He使体系压强增大 |
A. |
| B.单位时间内生成n mol Fe的同时生成n mol FeO |
| C.容器中气体压强不随时间的变化而变化 |
D.容器中 浓度不随时间的变化而变化 浓度不随时间的变化而变化 |
Ⅲ.某化学兴趣小组利用反应
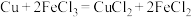 ,设计了如图所示的原电池装置。
,设计了如图所示的原电池装置。
(6)a是
(7)外电路中,电流从
(8)写出b电极上的电极反应式
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】氯化钠在自然界中的储量丰富,生活上可用作调味品,也广泛应用于工业、医疗、农业等。
(1)工业上通过电解饱和食盐水可制得氯气、氢气和烧碱。
①电解饱和食盐水的离子方程式为_______ 。
②氢气直接燃烧的能量转换率远低于燃料电池,氢气从燃料电池的_______ (填“正极”或“负极”)通入。
(2)以氯化钠为原料制钠单质的化学方程式为_______ ;利用反应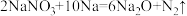 制取
制取 ,当该反应转移
,当该反应转移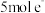 时,生成的
时,生成的 在标准状况下的体积为
在标准状况下的体积为_______ L,参与反应的氧化剂与还原剂的质量之比为_______ 。
(3)医疗上所用的生理盐水是质量分数为0.9%的氯化钠溶液。某化学兴趣小组用表中装置配制 生理盐水(密度约为
生理盐水(密度约为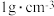 )。
)。
①用托盘天平(最小砝码为1g)称量_______ 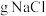 固体。
固体。
②操作顺序为f→_______ (除f外,部分操作可重复,填标号);进行b操作时,若俯视容量瓶刻度线,则配得的氯化钠溶液的浓度_______ (填“偏高”、“偏低”或“无影响”)。
(1)工业上通过电解饱和食盐水可制得氯气、氢气和烧碱。
①电解饱和食盐水的离子方程式为
②氢气直接燃烧的能量转换率远低于燃料电池,氢气从燃料电池的
(2)以氯化钠为原料制钠单质的化学方程式为
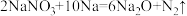 制取
制取 ,当该反应转移
,当该反应转移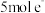 时,生成的
时,生成的 在标准状况下的体积为
在标准状况下的体积为(3)医疗上所用的生理盐水是质量分数为0.9%的氯化钠溶液。某化学兴趣小组用表中装置配制
 生理盐水(密度约为
生理盐水(密度约为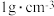 )。
)。①用托盘天平(最小砝码为1g)称量
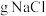 固体。
固体。②操作顺序为f→
 |  |  |  |  |  |
| a | b | c | d | e | f |
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】某同学取一定量淀粉进行水解实验,其实验步骤如下所示:

请回答下列问题:
① 所加入的试剂分别是
A_______ ,B________ ,C________ ;
② 加B的原因是_____________________________________________________ ;
③由此可知淀粉是________ (填“部分”、“完全”或“没有”)水解。

请回答下列问题:
① 所加入的试剂分别是
A
② 加B的原因是
③由此可知淀粉是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】为了检验淀粉水解产物,某学生设计了如下实验方案:
淀粉液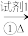 水解液
水解液 混合液
混合液 红色沉淀
红色沉淀
回答下列问题:
(1)试剂1是________ ,作用是___________________________ 。
(2)试剂2是________ ,作用是___________________________ 。
如果实验过程中没有加入试剂2而直接加入试剂3,能否实现实验目的________ (填“能”或“不能”)。
淀粉液
 水解液
水解液 混合液
混合液 红色沉淀
红色沉淀回答下列问题:
(1)试剂1是
(2)试剂2是
如果实验过程中没有加入试剂2而直接加入试剂3,能否实现实验目的
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐1】无机框图推断题。A、B、C三种化合物有如下转化关系:
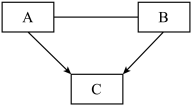
已知A是初中熟知的一元强酸,B是一元强碱,C是我们日常生活常用的调味品、是一种有咸味溶于水的白色固体。回答下列问题:
(1)将A的稀溶液中滴入紫色的石蕊试液,溶液变______ 色;将B的稀溶液中滴入无色的酚酞试液,溶液变______ 色;A是_____________ 、B是______________ (写名称)。
(2)向A中加入锌粉,该反应的离子方程式_______________ ,用单线桥法表示该反应电子转移方向和数目____________________ 。
(3)向B中通入少量的二氧化碳,该反应的离子方程式__________________________ 。
(4)将AB两物质混合,恰好完全反应。该反应的离子方程式____________________ 。
(5)检验A中阴离子的方法________________________________________________________ 。

已知A是初中熟知的一元强酸,B是一元强碱,C是我们日常生活常用的调味品、是一种有咸味溶于水的白色固体。回答下列问题:
(1)将A的稀溶液中滴入紫色的石蕊试液,溶液变
(2)向A中加入锌粉,该反应的离子方程式
(3)向B中通入少量的二氧化碳,该反应的离子方程式
(4)将AB两物质混合,恰好完全反应。该反应的离子方程式
(5)检验A中阴离子的方法
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】某无色废水中可能含有Fe3+、Al3+、Na+、Cl﹣、OH﹣、 、中的几种离子.分别取三份废水进行如下实验:
、中的几种离子.分别取三份废水进行如下实验:
I.进行焰色反应实验,火焰为无色.
Ⅱ.取100mL废水,加入足量的BaCl2溶液,生成2.33g白色沉淀.
Ⅲ.取100mL废水,逐滴加入1.0mol/L的NaOH溶液,消耗NaOH溶液的体积与生成沉淀的质量如图所示.
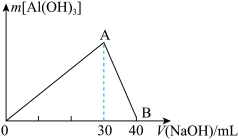
请根据上述信息回答下列问题:
(1)该废水中一定不含有的离子是_______________ .
(2)实验中需配制1.0mol/L的NaOH溶液100mL,所需仪器除了玻璃棒、托盘天平、量筒、药匙、烧杯、胶头滴管,还缺少的仪器有:___________________ .
(3)写出图中A→B反应的离子方程式:___________________ .
(4)通过计算,该废水中_____________ Cl﹣(填“含有”或“不含有”);
若含有,则c(Cl﹣)=_____________ (若不含有,此问不必作答)。
 、中的几种离子.分别取三份废水进行如下实验:
、中的几种离子.分别取三份废水进行如下实验:I.进行焰色反应实验,火焰为无色.
Ⅱ.取100mL废水,加入足量的BaCl2溶液,生成2.33g白色沉淀.
Ⅲ.取100mL废水,逐滴加入1.0mol/L的NaOH溶液,消耗NaOH溶液的体积与生成沉淀的质量如图所示.

请根据上述信息回答下列问题:
(1)该废水中一定不含有的离子是
(2)实验中需配制1.0mol/L的NaOH溶液100mL,所需仪器除了玻璃棒、托盘天平、量筒、药匙、烧杯、胶头滴管,还缺少的仪器有:
(3)写出图中A→B反应的离子方程式:
(4)通过计算,该废水中
若含有,则c(Cl﹣)=
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】某固体混合物可能由NaCl、KNO3、K2SO4、CuCl2、CaCl2、K2CO3中的一种或几种混合而成,为鉴定其组成,依次进行如下实验:
(1)取适量混合物加入足量蒸馏水,得到无色透明溶液
(2)向上述溶液中滴加足量BaCl2溶液,有白色沉淀产生
(3)过滤,取上述白色沉淀中加足量盐酸,产生无色气体,沉淀部分溶解
(4)往滤液中加AgNO3溶液,有白色沉淀产生,且白色沉淀不溶于稀硝酸
试判断:
肯定存在的物质有______ ;肯定不存在的物质有_________ ;可能存在的物质有_______ 。
(1)取适量混合物加入足量蒸馏水,得到无色透明溶液
(2)向上述溶液中滴加足量BaCl2溶液,有白色沉淀产生
(3)过滤,取上述白色沉淀中加足量盐酸,产生无色气体,沉淀部分溶解
(4)往滤液中加AgNO3溶液,有白色沉淀产生,且白色沉淀不溶于稀硝酸
试判断:
肯定存在的物质有
您最近一年使用:0次


 。
。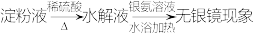 。
。


