如图为铜锌原电池工作示意图,下列有关该原电池的说法不正确的是
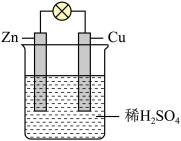

| A.溶液由无色逐渐变蓝 |
B.电子从 电极流出,经外电路回到 电极流出,经外电路回到 电极 电极 |
C. 电极质量减轻, 电极质量减轻, 电极上产生气泡 电极上产生气泡 |
D. 不断减小, 不断减小, 保持不变 保持不变 |
更新时间:2020-07-29 10:27:47
|
相似题推荐
单选题
|
较易
(0.85)
【推荐1】下列说法正确的是
| A.构成原电池正极和负极的材料必须是金属 |
| B.在原电池中,电子流出的一极是负极,该电极被还原 |
| C.原电池的正极一定是化学性质较不活泼的金属 |
| D.原电池可以把物质内部的能量部分转化为电能 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】锌铜原电池装置如图所示(盐桥是装有琼脂的KNO3溶液),下列说法正确的是


| A.锌为负极,发生氧化反应,其电极的反应式:Zn-2e-=Zn2+ |
| B.盐桥中的NO3-移向CuSO4溶液 |
| C.电子从锌片流向铜片,再从硫酸铜溶液流向硫酸锌 |
| D.铜片冒气泡,作正极,发生还原反应 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐3】镁燃料电池具有比能量高、使用安全方便、原材料来源丰富、成本低、燃料易于贮运等特点。研究的燃料电池可分为镁—空气燃料电池、镁—海水燃料电池、镁—过氧化氢燃料电池、镁—次氯酸盐燃料电池。如图为镁—次氯酸盐燃料电池的工作原理图,下列有关说法正确的是


| A.放电过程中OH-移向正极 |
| B.电池的总反应式为Mg+ClO-+H2O=Mg(OH)2↓+Cl- |
| C.镁燃料电池中镁均为负极,发生还原反应 |
| D.镁—过氧化氢燃料电池,酸性电解质中正极反应为H2O2+2H+-2e-=2H2O |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】关于下图所示原电池装置的说法错误的是( )


| A.Zn为负极,反应为Zn-2e-=Zn2+ | B.铜棒上发生还原反应 |
| C.电子从锌片经导线流向铜片 | D.溶液中氢离子浓度保持不变,溶液中SO42-向正极移动 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】如图所示铜锌原电池工作装置图,下列叙述不正确的是
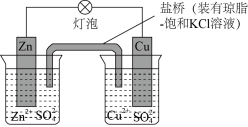
A.负极反应为 |
| B.铜电极上发生还原反应 |
C.盐桥中的 移向 移向 溶液 溶液 |
| D.在外电路中,电子从负极流向正极 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】原电池的应用促进了人类社会的发展。某种铜锌原电池示意图如图,关于该原电池的说法正确的是
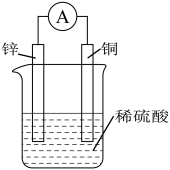

| A.铜是负极 | B.工作时,电流由铜电极经导线流向锌电极 |
| C.溶液中H+发生氧化反应 | D.锌发生还原反应 |
您最近一年使用:0次
单选题
|
较易
(0.85)
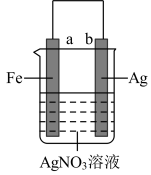
【推荐2】按如图所示装置进行实验,随着流入正极的电子增多,下列物理量按增大、减小、不变的顺序排列的是( )
① ②
②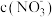 ③a棒的质量 ④b棒的质量 ⑤溶液的质量
③a棒的质量 ④b棒的质量 ⑤溶液的质量
①
 ②
②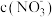 ③a棒的质量 ④b棒的质量 ⑤溶液的质量
③a棒的质量 ④b棒的质量 ⑤溶液的质量
| A.④,①③⑤,② | B.④,①⑤,②③ |
| C.①④,③⑤,② | D.④,③⑤,①② |
您最近一年使用:0次


 向左移动
向左移动
 为原电池的负极
为原电池的负极

