A、B、C、D、E、F为原子序数依次增大的短周期元素,非金属元素A最外层电子数与其周期数相同,B的最外层电子数是其所在周期数的2倍。B的单质在D的单质中充分燃烧能生成其最高价化合物BD2。E+与D2-具有相同的电子数。A的单质在F的单质中燃烧,产物溶于水得到一种强酸。回答下列问题:
(1)元素A的名称为__________ 。
(2)A、D、E组成的化合物中,D的质量分数为40%,该化合物俗名为_____ 。其水溶液与F的单质反应的化学方程式为______ 。
(3)由这些元素组成的物质,其组成和结构信息如下表:
a的化学式为______ ;b的化学式为_______ ;c的电子式为________ 。
(1)元素A的名称为
(2)A、D、E组成的化合物中,D的质量分数为40%,该化合物俗名为
(3)由这些元素组成的物质,其组成和结构信息如下表:
物质 | 组成和结构信息 |
a | 由A和D组成的化合物,且原子个数之比为1:1 |
b | 由A、C、F三种元素组成的离子化合物 |
c | 化学组成为BDF2,且所有原子均满足最外层8电子结构 |
更新时间:2020-07-30 11:53:05
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】有U、V、W、X四种前三周期元素,原子序数依次增大,其相关信息如下表:
请回答下列问题:
(1)U、V两种元素组成的一种化合物甲是重要的化工原料,常把它的产量作为衡量石油化工发展水平的标志,则甲分子的空间构型为________ 。
(2)写出W单质的结构式___________ ,其化学键为________ 性共价键:W最简单气态氢化物的电子式为___________ ,分子的空间构型是___________ ,其化学键为___________ 性共价键。
(3)X在周期表中的位置是_______ ,该主族元素的气态氢化物中,沸点最低的是__________ (填化学式)
(4)乙和丙分别是V和X的某种氢化物,这两种氢化物分子中含有有18个电子。乙和丙的化学式分别是________ 、________ 。
| 元素编号 | 相关信息 |
| U | 所处的周期数、族序数分别与其原子序数相等 |
| V | 外层电子数是最内层电子数的两倍 |
| W | 单质中有三对共用电子对 |
| X | 是地壳中含量最多的元素 |
请回答下列问题:
(1)U、V两种元素组成的一种化合物甲是重要的化工原料,常把它的产量作为衡量石油化工发展水平的标志,则甲分子的空间构型为
(2)写出W单质的结构式
(3)X在周期表中的位置是
(4)乙和丙分别是V和X的某种氢化物,这两种氢化物分子中含有有18个电子。乙和丙的化学式分别是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】现有A、B、C、D、E、F、G七种短周期主族元素,原子序数依次增大。A与C形成的化合物能使湿润的红色石蕊试纸变蓝;D是地壳中含量最多的元素;D、F原子的最外层电子数相等;E的焰色反应呈黄色;B元素的一种同位素在考古时可用于测定一些文物的年代。
请回答下列问题:(注意回答问题时均用元素符号表示)
(1)元素B在周期表中的位置:___________ 。
(2)元素D与E组成的含非极性键的化合物的电子式:___________ 。元素A与D组成的18电子分子的结构式:___________ 。
(3)写出G的简单阴离子的电子排布式___________ 。
(4)D和F的简单气态氢化物沸点比较高的是:________ (写分子式),原因:________ 。
(5)D、E、F、G的电负性小到大的顺序为___________ (用元素符号表示)。
(6)用电子式表示化合物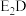 的形成过程:
的形成过程:___________ 。
请回答下列问题:(注意回答问题时均用元素符号表示)
(1)元素B在周期表中的位置:
(2)元素D与E组成的含非极性键的化合物的电子式:
(3)写出G的简单阴离子的电子排布式
(4)D和F的简单气态氢化物沸点比较高的是:
(5)D、E、F、G的电负性小到大的顺序为
(6)用电子式表示化合物
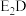 的形成过程:
的形成过程:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】前四周期的元素A、B、C、D、E原子序数依次增大;A是宇宙中含量最丰富的元素;B和C同一主族,且B的L层电子数是K层电子数的2.5倍;D和C同一周期,且D的气态氢化物可以和其最高价氧化物的水化物发生氧化还原反应;E位于第四周期,其价电子层中只有一个电子,且内层都处于全充满状态。请回答下列问题:
(1)E原子的电子排布式为________ ,C和D的第一电离能较大的是________ 。
(2)CO43-中C的杂化方式为________ ,该离子的“VSEPR”模型为________ 形。
(3)C和D的简单阴离子半径由大到小的顺序为________ ,C和D最高价含氧酸的酸性由弱到强的顺序为________ 。
(4)某分子的结构式为:A—B=B—A,则该分子中σ键和π键的数目之比为_____ ,B2分子和一氧化碳分子互为等电子体,则一氧化碳的电子式为_____ 。
(5)向EDO4溶液中加入过量稀氨水,阳离子化学式为________ ,该离子的配位体为________ 。
(6)B能量最高的电子为________ 轨道上的电子,其轨道呈________ 形。
(1)E原子的电子排布式为
(2)CO43-中C的杂化方式为
(3)C和D的简单阴离子半径由大到小的顺序为
(4)某分子的结构式为:A—B=B—A,则该分子中σ键和π键的数目之比为
(5)向EDO4溶液中加入过量稀氨水,阳离子化学式为
(6)B能量最高的电子为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】A~F是中学常见物质,其中B、D、F均为单质,它们的相互转化关系如下图所示:
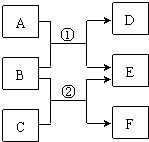
Ⅰ若A、C、E是氧化物,构成B、D的元素在同一主族,反应①②都是工业上的重要反应,通过反应②可以实现煤的气化,使煤变为清洁能源。
(1)写出反应①的化学方程式_______________________________________________ 。
(2)用化学方程式表示E在冶金工业上的一种重要用途____________________________________ 。
Ⅱ若A、C、E是氢化物,构成B和F的元素是第三周期的相邻元素,F是一种淡黄色固体,A能使湿润的红色石蕊试纸变蓝,A、E混合时有白烟生成。
(1)写出D的电子式____________ 。
(2)由A或C转化为E,每消耗1molB,转移电子的物质的量为_______ mol。
(3)同温同压下,将V1L A气体和V2L E气体通入水中,
①若所得溶液的pH=7,则V1_____ V2(填“>”或“<”或“=”)。
②若V1=2V2,反应后溶液中各离子浓度由大到小的顺序为_______________________ 。

Ⅰ若A、C、E是氧化物,构成B、D的元素在同一主族,反应①②都是工业上的重要反应,通过反应②可以实现煤的气化,使煤变为清洁能源。
(1)写出反应①的化学方程式
(2)用化学方程式表示E在冶金工业上的一种重要用途
Ⅱ若A、C、E是氢化物,构成B和F的元素是第三周期的相邻元素,F是一种淡黄色固体,A能使湿润的红色石蕊试纸变蓝,A、E混合时有白烟生成。
(1)写出D的电子式
(2)由A或C转化为E,每消耗1molB,转移电子的物质的量为
(3)同温同压下,将V1L A气体和V2L E气体通入水中,
①若所得溶液的pH=7,则V1
②若V1=2V2,反应后溶液中各离子浓度由大到小的顺序为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】位于短周期的四种主族元素A、B、C、D,原子序数依次增大,已知A、C位于同一主族,A在周期表中原子半径最小。B、D的最外层电子数相等,且B、D的原子序数之和为A、C原子序数之和的两倍。E是自然界中含量最高的金属。根据你的推断完成下列问题:
(1)E元素在周期表中的位置为_______ 。
(2)写出由上述元素形成的具有漂白作用的三种物质的化学式_______ 。
(3)用电子式表示C与D形成化合物的过程_______ 。
(4)写出E的最高价氧化物与强碱反应的离子方程式________ 。
(5)B、C两元素形成的原子个数比为1:1的化合物中的化学键为______ 。
(1)E元素在周期表中的位置为
(2)写出由上述元素形成的具有漂白作用的三种物质的化学式
(3)用电子式表示C与D形成化合物的过程
(4)写出E的最高价氧化物与强碱反应的离子方程式
(5)B、C两元素形成的原子个数比为1:1的化合物中的化学键为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】下图是部分短周期元素的常见化合价与原子序数的关系图:
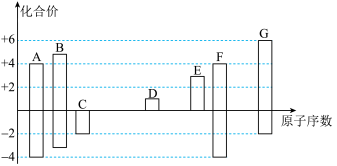
请回答下列问题:
(1)AB-离子与__________ 互为等电子体,lmolAB-离子含有___________ molπ键。
(2)用电子式表示D2G的形成过程________________________ 。
(3)由C、E、G三种元素的某盐用途广泛,请用离子方程式表示下列过程:
①该盐可做泡沫灭火器______________________________ ;
②向该盐溶液中加入Ba(OH) 2至沉淀物质的量最大时__________________________
(4)某同学设计实验证明A、B、F的非金属性强弱关系。(其中溶液b和溶液c均为足量)。
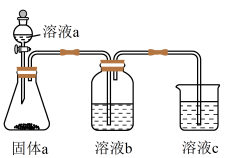
①溶液a和b分别为________________ ,________________ 。
②溶液c中的离子方程式为________________________________________________ 。
③请从原子结构的角度解释非金属性B>A的原因______________________________ 。

请回答下列问题:
(1)AB-离子与
(2)用电子式表示D2G的形成过程
(3)由C、E、G三种元素的某盐用途广泛,请用离子方程式表示下列过程:
①该盐可做泡沫灭火器
②向该盐溶液中加入Ba(OH) 2至沉淀物质的量最大时
(4)某同学设计实验证明A、B、F的非金属性强弱关系。(其中溶液b和溶液c均为足量)。

①溶液a和b分别为
②溶液c中的离子方程式为
③请从原子结构的角度解释非金属性B>A的原因
您最近一年使用:0次



