下图是部分短周期元素的常见化合价与原子序数的关系图:
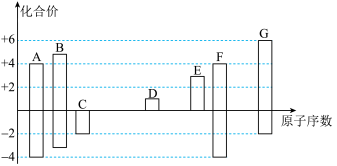
请回答下列问题:
(1)AB-离子与__________ 互为等电子体,lmolAB-离子含有___________ molπ键。
(2)用电子式表示D2G的形成过程________________________ 。
(3)由C、E、G三种元素的某盐用途广泛,请用离子方程式表示下列过程:
①该盐可做泡沫灭火器______________________________ ;
②向该盐溶液中加入Ba(OH) 2至沉淀物质的量最大时__________________________
(4)某同学设计实验证明A、B、F的非金属性强弱关系。(其中溶液b和溶液c均为足量)。
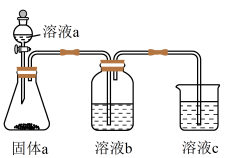
①溶液a和b分别为________________ ,________________ 。
②溶液c中的离子方程式为________________________________________________ 。
③请从原子结构的角度解释非金属性B>A的原因______________________________ 。

请回答下列问题:
(1)AB-离子与
(2)用电子式表示D2G的形成过程
(3)由C、E、G三种元素的某盐用途广泛,请用离子方程式表示下列过程:
①该盐可做泡沫灭火器
②向该盐溶液中加入Ba(OH) 2至沉淀物质的量最大时
(4)某同学设计实验证明A、B、F的非金属性强弱关系。(其中溶液b和溶液c均为足量)。

①溶液a和b分别为
②溶液c中的离子方程式为
③请从原子结构的角度解释非金属性B>A的原因
更新时间:2017-09-15 19:45:01
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
【推荐1】下图为元素周期表的一部分。根据元素①~⑦在周期表中的位置,按要求回答下列问题。
(1)元素①~⑦的单质中氧化性最强的是___________ 。(填化学式)
(2)元素③⑤⑥的原子的半径从大到小的顺序是___________ 。(用元素符号表示)
(3)元素②的简单气态氢化物的沸点高于元素⑥的,原因是___________ 。
(4)元素②④⑦按原子数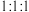 组成化合物甲,甲中所含化学键的类型是
组成化合物甲,甲中所含化学键的类型是___________ 。
(5)元素①与④组成的化合物可与水反应,写出反应的化学方程式___________ 。
(6)元款④⑥⑦的最高价氧化物对应的水化物分别为A、B、C.相同条件下。相同物质的量浓度的A、B、C的水溶液中 最大的是
最大的是___________ 。(填化学式)
(7)元素①与⑦组成的化合物为乙。用电子式表示乙的形成过程___________ 。
| 族 周期 | ⅠA | 0 | ||||||
| ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||
| ② | ③ | |||||||
| ④ | ⑤ | ⑥ | ⑦ |
(2)元素③⑤⑥的原子的半径从大到小的顺序是
(3)元素②的简单气态氢化物的沸点高于元素⑥的,原因是
(4)元素②④⑦按原子数
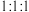 组成化合物甲,甲中所含化学键的类型是
组成化合物甲,甲中所含化学键的类型是(5)元素①与④组成的化合物可与水反应,写出反应的化学方程式
(6)元款④⑥⑦的最高价氧化物对应的水化物分别为A、B、C.相同条件下。相同物质的量浓度的A、B、C的水溶液中
 最大的是
最大的是(7)元素①与⑦组成的化合物为乙。用电子式表示乙的形成过程
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
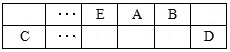
【推荐2】A、B、C、D、E、F是中学化学中常见的六种短周期元素,有关位置及信息如下:A的最高价氧化物对应的水化物与其氢化物反应生成离子化合物;C单质一般保存在煤油中;F的最高价氧化物对应的水化物既能与强酸反应又能与强碱反应,G单质是日常生活中用量最大的金属,易被腐蚀或损坏。请回答下列问题:
(1)A元素的氢化物水溶液能使酚酞变红的原因用电离方程式解释为___________ 。
(2)同温同压下,将a L A氢化物的气体和b L D的氢化物气体先后通入一盛水的烧杯中,若所得溶液的pH=7,则a___________ b(填“>"或“<”或“=”)。
(3)常温下,相同浓度F、G简单离子的溶液中滴加NaOH溶液,F、G两元素先后沉淀,F(OH)n完全沉淀的pH是4.7,G(OH)n完全沉淀的pH是2.8,则在相同条件下,溶解度较大的是:___________ (填化学式)。
(4)A与B可组成质量比为7:16的三原子分子,该分子释放在空气中其化学作用可能引发的后果有:___________ 。
①酸雨 ②温室效应 ③光化学烟雾 ④臭氧层破坏
(5)A和C组成的一种离子化合物,能与水反应生成两种碱,该反应的化学方程式是___________ 。
(6)用电子式表示B,C形成化合物C2B2的过程___________ 。
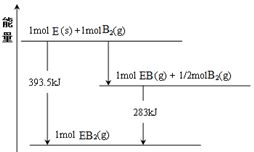
(7)已知一定量的E单质能在B2(g)中燃烧,其可能的产物及能量关系如下图所示:请写出一定条件下EB2(g) 与E(s)反应生成EB(g)的热化学方程式___________ 。

(1)A元素的氢化物水溶液能使酚酞变红的原因用电离方程式解释为
(2)同温同压下,将a L A氢化物的气体和b L D的氢化物气体先后通入一盛水的烧杯中,若所得溶液的pH=7,则a
(3)常温下,相同浓度F、G简单离子的溶液中滴加NaOH溶液,F、G两元素先后沉淀,F(OH)n完全沉淀的pH是4.7,G(OH)n完全沉淀的pH是2.8,则在相同条件下,溶解度较大的是:
(4)A与B可组成质量比为7:16的三原子分子,该分子释放在空气中其化学作用可能引发的后果有:
①酸雨 ②温室效应 ③光化学烟雾 ④臭氧层破坏
(5)A和C组成的一种离子化合物,能与水反应生成两种碱,该反应的化学方程式是
(6)用电子式表示B,C形成化合物C2B2的过程
(7)已知一定量的E单质能在B2(g)中燃烧,其可能的产物及能量关系如下图所示:请写出一定条件下EB2(g) 与E(s)反应生成EB(g)的热化学方程式

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】原子序数由小到大排列的四种短周期元素X、Y、Z、W,其中X、Z、W与氢元素可形成XH3、H2Z和HW三种分子:Y与氧元素可形成Y2O和Y2O2两种离子化合物。
(1)Y与Z形成的化合物电子式为_______ ,含有的化学键是_______ 。
(2)用电子式表示Y2O的形成过程:_______ 。
(3)X、Z、W三种元素的最高价氧化物对应的水化物中,酸性最强的是_______ (填化学式)。
(4)XH3与W2发生置换反应,生成的化合物属于离子化合物,该离子化合物是_______ (填化学式)。
(5)W2与NaOH溶液反应生成的三种物质中,属于离子化合物的是_______ 。
(1)Y与Z形成的化合物电子式为
(2)用电子式表示Y2O的形成过程:
(3)X、Z、W三种元素的最高价氧化物对应的水化物中,酸性最强的是
(4)XH3与W2发生置换反应,生成的化合物属于离子化合物,该离子化合物是
(5)W2与NaOH溶液反应生成的三种物质中,属于离子化合物的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】元素X、Y、Z、M、W在周期表中的位置如图:
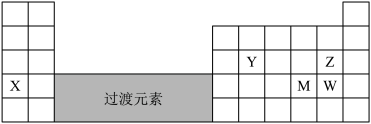
(1)X的元素符号是_________ 。
(2)YO2是玻璃的成分之一,是酸性氧化物。实验室盛装NaOH溶液的试剂瓶不能用玻璃塞的原因是:_________ +_________ OH-=_________ +_________ 。
(3)元素Z和元素W中,非金属性比较弱的是_________ (填元素符号)。在Z和W形成的原子个数比为1:1的化合物中,W的化合价是_________ 。
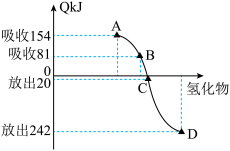
(4)元素M(Se)是人体必需的微量元素。Se能与H2反应生成H2Se,用原子结构解释原因_________ 。298K、1.01×105pa时,O2、S、Se、Te分别与H2化合生成1 mol气态氢化物时的热量的变化数据(Q)如下图所示。图中表示Se与H2化合的点是_________ (填字母)。

(1)X的元素符号是
(2)YO2是玻璃的成分之一,是酸性氧化物。实验室盛装NaOH溶液的试剂瓶不能用玻璃塞的原因是:
(3)元素Z和元素W中,非金属性比较弱的是
(4)元素M(Se)是人体必需的微量元素。Se能与H2反应生成H2Se,用原子结构解释原因

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】随原子序数的递增,八种短周期元素原子半径的相对大小、最高正价或最低负价的变化如图所示,根据判断出的元素回答问题:
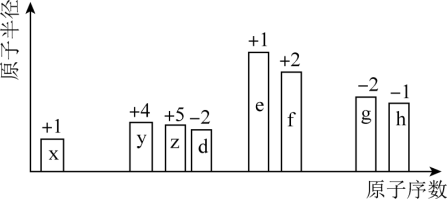
(1)g在元素周期表中的位置是_______ 。
(2)元素y的一种核素可测定文物年代,该核素的符号为_______ 。
(3)在上述元素中,原子半径最大的是_______ (填元素名称),e、f、d三元素形成的简单离子,它们的离子半径由大到小顺序是 用离子符号表示
用离子符号表示
_______ 。
(4)元素g与元素h相比,非金属性较强的是_______ (填元素符号),下列表述中能证明这一事实的是_______ (填序号)。
a.常温下g的单质和h的单质状态不同
b.h的气态氢化物比g的气态氢化物稳定
c.h的最高价氧化物的水化物酸性比g的最高价氧化物的水化物酸性强
(5)f、h 两种元素组成的化合物的电子式为:_______ 。
(6)在最高价氧化物对应的水化物中,酸性最强的化合物的化学式是_______  填化学式
填化学式 ,最高价氧化物对应的水化物是两性的元素是
,最高价氧化物对应的水化物是两性的元素是_______  填元素符号
填元素符号 ,写出它的氢氧化物与e的氢氧化物反应的离子方程式
,写出它的氢氧化物与e的氢氧化物反应的离子方程式_______ 。
(7)g、h两元素原子得电子能力较强的是_______ (元素符号),请从原子结构得角度解释其原因_______ 。

(1)g在元素周期表中的位置是
(2)元素y的一种核素可测定文物年代,该核素的符号为
(3)在上述元素中,原子半径最大的是
 用离子符号表示
用离子符号表示
(4)元素g与元素h相比,非金属性较强的是
a.常温下g的单质和h的单质状态不同
b.h的气态氢化物比g的气态氢化物稳定
c.h的最高价氧化物的水化物酸性比g的最高价氧化物的水化物酸性强
(5)f、h 两种元素组成的化合物的电子式为:
(6)在最高价氧化物对应的水化物中,酸性最强的化合物的化学式是
 填化学式
填化学式 ,最高价氧化物对应的水化物是两性的元素是
,最高价氧化物对应的水化物是两性的元素是 填元素符号
填元素符号 ,写出它的氢氧化物与e的氢氧化物反应的离子方程式
,写出它的氢氧化物与e的氢氧化物反应的离子方程式(7)g、h两元素原子得电子能力较强的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】有X、Y、Z、M、R、Q六种短周期主族元素,部分信息如下表所示:
请回答下列问题:
(1)R在元素周期表中的位置是______ 。
(2)Y的单质可用做____ 。
A.集成电路的芯片 B.光导纤维 C.是玛瑙的主要成分
(3)Y、R、Q的原子半径由大到小的顺序为_____ (用元素符号表示)。
(4)下列事实能说明R非金属性比Y强这一结论的是______ (选填字母序号)。
A.常温下Y的单质呈固态,R的单质呈气态。
B.气态氢化物稳定性R>Y。
C.R的最高价含氧酸的酸性强于Y的最高价含氧酸的酸性。
(5)X、M、Z三种元素组成的化合物中含有的化学键为_____ ;写出R的单质与上述化合物的水溶液反应的化学方程式:_____ 。
| X | Y | Z | M | R | Q | |
| 主要 化合价 | +4,-4 | -2 | +7,-1 | |||
| 其它 | 阳离子X+核外无电子 | 无机非金属材料的主角 | 短周期元素中原子半径最大 | H2M分子间存在氢键,常温下为液体 | 次外层电子数是最外层电子数的4倍 |
(1)R在元素周期表中的位置是
(2)Y的单质可用做
A.集成电路的芯片 B.光导纤维 C.是玛瑙的主要成分
(3)Y、R、Q的原子半径由大到小的顺序为
(4)下列事实能说明R非金属性比Y强这一结论的是
A.常温下Y的单质呈固态,R的单质呈气态。
B.气态氢化物稳定性R>Y。
C.R的最高价含氧酸的酸性强于Y的最高价含氧酸的酸性。
(5)X、M、Z三种元素组成的化合物中含有的化学键为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】现有A、B、C、D、E、F六种短周期元素,它们的原子序数依次增大,A与D同主族,C与E同主族,D、E、F同周期,A、B的最外层电子数之和与C的最外层电子数相等,A能分别与B、C形成电子数相等的分子,且A与C形成的化合物常温下为液态,A能分别与E、F形成电子总数相等的气体分子.请回答下列问题(题中字母只代表元素代号,与实际元素符号无关):
(1)B、F可形成三角锥形分子,其电子式为______________
(2)B、C、E的气态氢化物沸点由高到低的顺序为:___________________
(3)C、E形成的化合物通入F的单质的水溶液中,可形成两种强电解质,则该反应的离子方程式为:__________________________________________ 。
(4)A、B、C可形成常见的化合物H,足量的H的稀溶液与a g Fe完全反应,被还原的H的物质的量为:________________ 。
(1)B、F可形成三角锥形分子,其电子式为
(2)B、C、E的气态氢化物沸点由高到低的顺序为:
(3)C、E形成的化合物通入F的单质的水溶液中,可形成两种强电解质,则该反应的离子方程式为:
(4)A、B、C可形成常见的化合物H,足量的H的稀溶液与a g Fe完全反应,被还原的H的物质的量为:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】A、B、C、D、E、F是六种短周期元素,它们的原子序数依次增大;A元素的原子半径最小;B元素的一种单质是空气中含量最多的一种成分;D与A同主族;F元素原子的最外层电子数是其次外层电子数的 ;A、B、D、F这四种元素,每一种都能与C元素形成原子个数比不相同的化合物。D、E、F三种元素最高价氧化物对应的水化物两两之间皆能反应。请回答下列问题:
;A、B、D、F这四种元素,每一种都能与C元素形成原子个数比不相同的化合物。D、E、F三种元素最高价氧化物对应的水化物两两之间皆能反应。请回答下列问题:
(1)B元素的原子结构示意图_________ ;E元素在周期表中的位置是_________ 。
(2)上述6种元素中,金属性最强的元素是___________ (写元素名称,下同);非金属性最强的元素是___________ 。
(3)A、B、C和F可组成一种化合物,其原子个数之比为5:1:4:1.写出该化合物的化学式___________ 。
(4)写出含E元素的氧化物与氢氧化钠溶液反应的离子方程式___________ 。
(5)C、D、E、F四种元素的简单离子半径由大到小的顺序是___________ (用离子符号表示)。
(6)由C、D两种元素形成的原子个数之比为1:1的化合物中,所含化学键的类型有___________ 。
(7)用电子式表示D的简单氢化物的形成过程___________ 。
 ;A、B、D、F这四种元素,每一种都能与C元素形成原子个数比不相同的化合物。D、E、F三种元素最高价氧化物对应的水化物两两之间皆能反应。请回答下列问题:
;A、B、D、F这四种元素,每一种都能与C元素形成原子个数比不相同的化合物。D、E、F三种元素最高价氧化物对应的水化物两两之间皆能反应。请回答下列问题:(1)B元素的原子结构示意图
(2)上述6种元素中,金属性最强的元素是
(3)A、B、C和F可组成一种化合物,其原子个数之比为5:1:4:1.写出该化合物的化学式
(4)写出含E元素的氧化物与氢氧化钠溶液反应的离子方程式
(5)C、D、E、F四种元素的简单离子半径由大到小的顺序是
(6)由C、D两种元素形成的原子个数之比为1:1的化合物中,所含化学键的类型有
(7)用电子式表示D的简单氢化物的形成过程
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】A、X,Y、Z、R、W为六种短周期元素。A是短周期中半径最小的元素;X原子最外层电子数是核外电子层数的3倍;Y最高正价与最低负价代数和为4;Z的单质常用于漂白工业;R是短周期元素中金属性最强的元素,W是生活中的常见金属,其氧化物常作耐高温材料。回答下列问题:
(1)Y元素的名称是___________ ,在周期表中的位置是___________ 。
(2)写出化合物AZX的电子式:___________ ;化合物R2X2存在的化学键类型是___________ 。
(3)比较X、Z、R三种元素对应的简单离子半径大小:___________ (用离子符号和“>”表示)。
(4)下列事实能证明R比W金属性强的这一结论的是___________ (填序号)。
a.R的熔点低于W b.常温下,R与水剧烈反应而W不能
c.最高价氧化物对应的水化物碱性:ROH>W(OH)3 d.最外层电子数:W>R
(5)用电子式表示RZ的形成过程:___________ 。
(1)Y元素的名称是
(2)写出化合物AZX的电子式:
(3)比较X、Z、R三种元素对应的简单离子半径大小:
(4)下列事实能证明R比W金属性强的这一结论的是
a.R的熔点低于W b.常温下,R与水剧烈反应而W不能
c.最高价氧化物对应的水化物碱性:ROH>W(OH)3 d.最外层电子数:W>R
(5)用电子式表示RZ的形成过程:
您最近一年使用:0次



